Clear Sky Science · pl
Strukturalne podstawy dynamicznych konformacji AP-4 i jego sprzężenia z ARF1
Jak komórki sortują i wysyłają swoje ładunki
Każda komórka to tętniący życiem magazyn, nieustannie sortujący i wysyłający tysiące proteinowych „paczek” do właściwych miejsc. Gdy ten system dostaw zawiedzie w komórkach nerwowych, skutki mogą być poważne — zaburzenia mózgu i ruchu. W tym badaniu odsłonięto, w jaki sposób jedna z kluczowych maszyn transportowych, nazwana AP-4, zmienia kształt i współdziała z regulującą białkiem ARF1, aby załadowywać ładunek do maleńkich pęcherzyków transportowych, oraz dlaczego jej elastyczność jest tak istotna dla zdrowia neuronów.
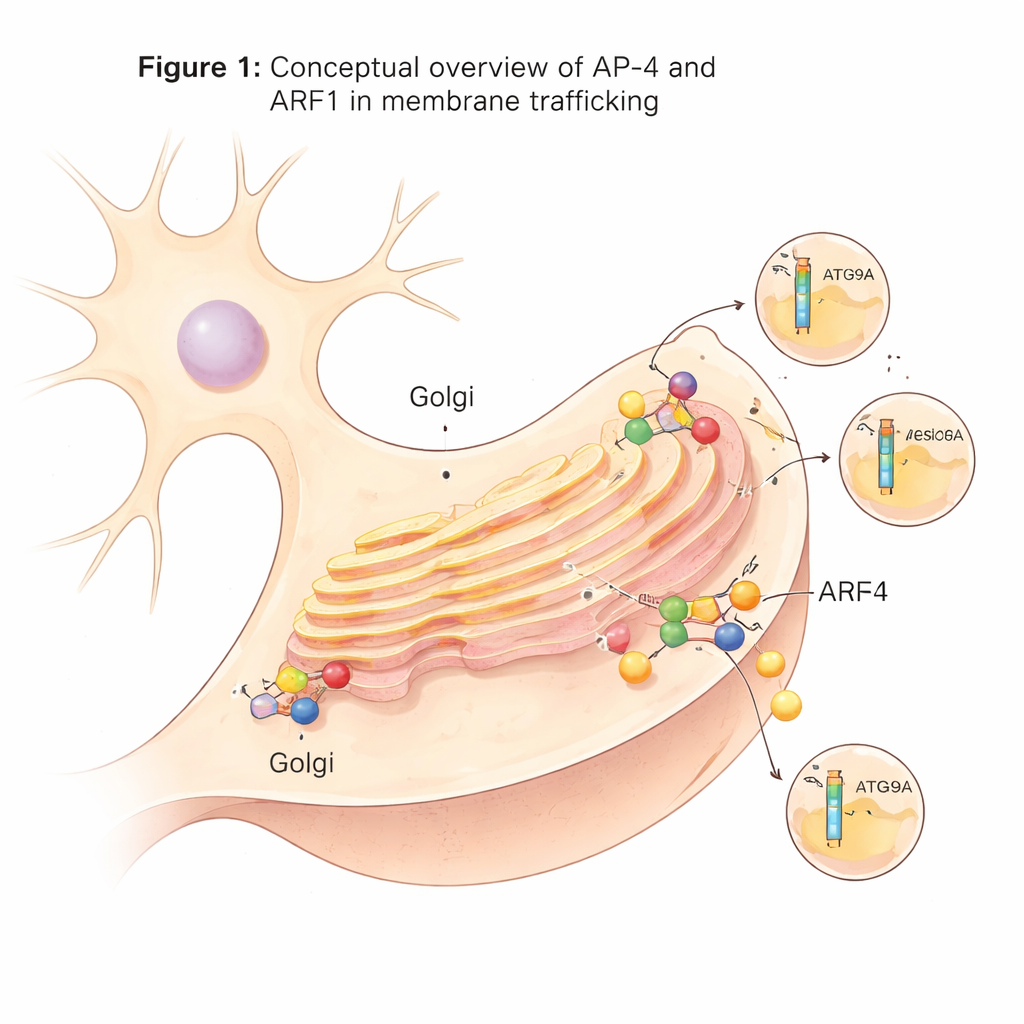
Specjalistyczna maszyna wysyłkowa w komórkach nerwowych
W komórkach wiele pęcherzyków transportowych odrywa się z centralnej stacji sortującej znanej jako sieć trans-Golgiego. Pęcherzyki te polegają na kompleksach białek adaptorowych, zwanych kompleksami AP, które działają jak doki załadunkowe: rozpoznają białka-ładunki i pomagają formować otoczone pęcherzyki. AP-4 jest jednym z tych adaptorów i wyróżnia się tym, że w przeciwieństwie do wielu innych nie korzysta z powszechnego rusztowania białkowego klatryny. Choć AP-4 występuje w wielu tkankach, pełni szczególnie istotną rolę w neuronach. Gdy AP-4 jest nieobecny lub wadliwy u ludzi, kluczowe ładunki, takie jak białko związane z autofagią ATG9A i niektóre receptory glutaminianowe, nie przemieszczają się prawidłowo, co prowadzi do ciężkiego stanu neurorozwojowego znanego jako zespół niedoboru AP-4.
Kompleks zmieniający kształt w spoczynku
Autorzy wykorzystali krioelektronową mikroskopię, potężną metodę obrazowania zdolną zwizualizować duże zespoły białkowe, by wyznaczyć trójwymiarową strukturę „rdzenia” kompleksu AP-4 w roztworze. AP-4 zbudowany jest z czterech podjednostek, które razem tworzą miseczkowatą strukturę. Odkryli, że AP-4 nie utrzymuje jednego sztywnego kształtu. Zamiast tego naturalnie przełącza się między formą „zamkniętą”, w której jedna podjednostka (C-terminalna domena podjednostki średniej) jest schowana w centrum miseczki, a formą „otwartą”, w której ten fragment wysuwa się i staje się wysoce elastyczny. Dodatkowe eksperymenty fluorescencji pojedynczych cząsteczek wykazały, że ta podjednostka faktycznie próbuje co najmniej trzech pozycji — zamkniętej, częściowo otwartej i w pełni otwartej — ujawniając, że AP-4 jest wewnętrznie dynamiczny nawet zanim przyłączy się do błon.
Rola ARF1: rekruter, nie główny przełącznik
Wiele spokrewnionych kompleksów adaptorowych przełącza się z nieaktywnego do aktywnego kształtu poprzez wiązanie małych regulatorowych białek nazwywanych ARF. Aby sprawdzić, jak to działa w przypadku AP-4, badacze wyznaczyli struktury AP-4 związane z ARF1, małym białkiem wiążącym GTP, które kotwiczy się do błon. Stwierdzili, że ARF1 przyłącza się głównie do jednej z dużych podjednostek AP-4 w pobliżu jej N-terminusa, w sposób podobny do innych kompleksów AP. Co zaskakujące, wiązanie ARF1 nie wywołuje dramatycznej przebudowy strukturalnej AP-4. Kształty zamknięte i otwarte nadal współistnieją, a ogólna architektura kompleksu pozostaje w dużej mierze niezmieniona. Testy biochemiczne potwierdziły, że określone punkty kontaktu między ARF1 a AP-4 są niezbędne do rekrutacji na błony, ale sam ARF1 nie blokuje AP-4 w jednym, jedynym stanie aktywnym.
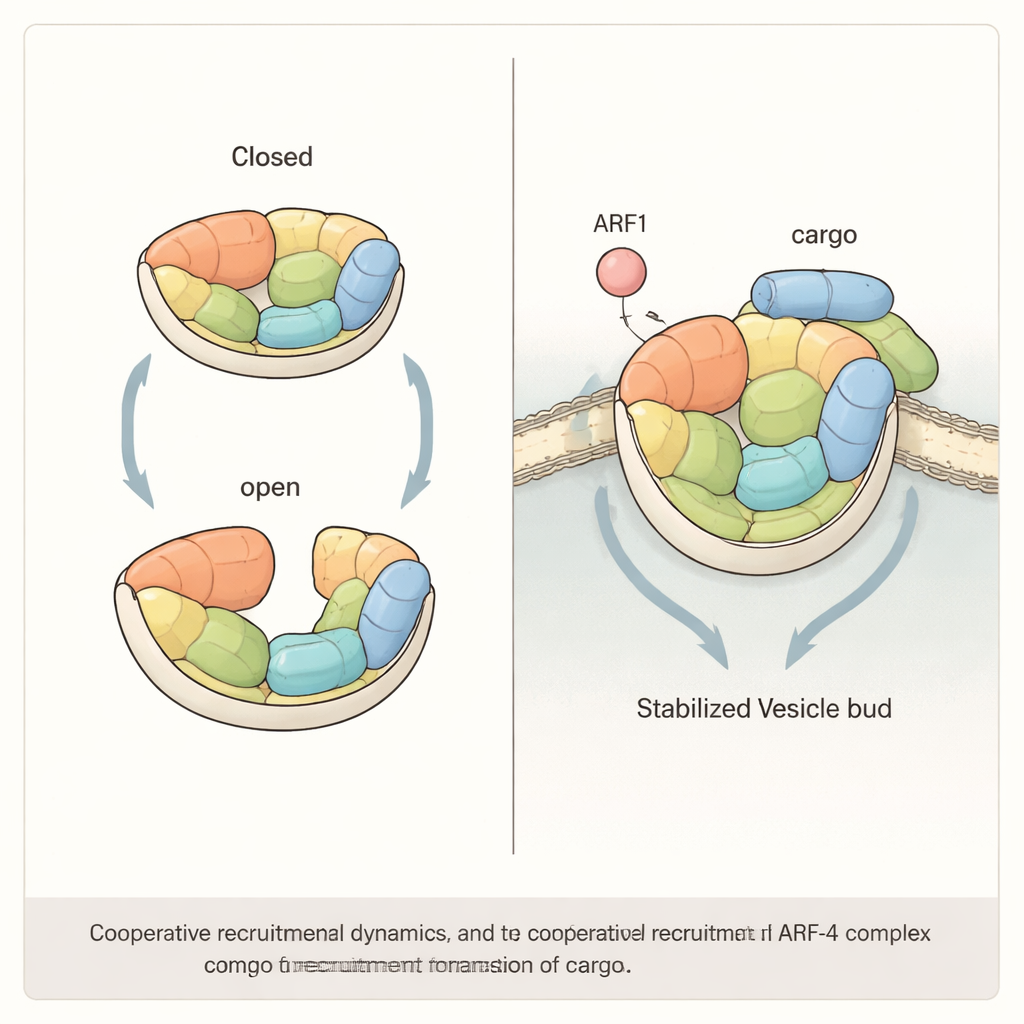
Współpraca regulatora i ładunku
Badanie wykazuje dalej, że wydajna rekrutacja AP-4 na błony prawdopodobnie wymaga współdziałania między ARF1 a samymi białkami-ładunkami. Rekonstruując układ na sztucznych kulkach i liposomach, autorzy stwierdzili, że albo ARF1, albo krótki ogon białka ładunkowego ATG9A mogą przyciągnąć AP-4, lecz gdy oba występują razem, przyciągają znacznie więcej AP-4 niż wynikałoby z prostego sumowania ich indywidualnych efektów. Gdy badacze wprowadzili mutacje, które usztywniły strukturę AP-4 — ograniczając jego zdolność do przechodzenia między stanami otwartym i zamkniętym — efekt synergii zniknął. W ludzkich komórkach pozbawionych kluczowej podjednostki AP-4, przywrócenie jedynie takich „sztywnych” mutantów kompleksu nie odtworzyło prawidłowego transportu ATG9A z Golgiego, co podkreśla, że elastyczność AP-4 nie jest jedynie ciekawostką, lecz funkcjonalnym wymaganiem.
Dlaczego elastyczność ma znaczenie dla zdrowia mózgu
Podsumowując, praca ukazuje AP-4 jako adaptor zmieniający kształt, który próbuje wielu konformacji w roztworze i na błonach. Zamiast działać jako przełącznik włącz/wyłącz, ARF1 pełni rolę rekrutera na błonach, współpracując z białkami-ładunkami, aby stabilizować AP-4 w produktywnych konfiguracjach sprzyjających formowaniu pęcherzyków. Zakłócenie tej równowagi — poprzez osłabienie wiązania ARF1 lub ładunku albo poprzez zamrożenie AP-4 w jednej formie — upośledza eksport ładunków z Golgiego i może przyczyniać się do chorób neurorozwojowych. Odkrywając strukturalne podstawy dynamicznego zachowania AP-4, badanie to dostarcza ram do zrozumienia zaburzeń związanych z AP-4 i sugeruje kierunki przyszłych strategii przywracania prawidłowego transportu w dotkniętych neuronach.
Cytowanie: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Słowa kluczowe: transport błonowy, kompleks adaptorowy AP-4, ARF1, formowanie pęcherzyków, zaburzenie neurorozwojowe