Clear Sky Science · pl
Komórki NK ZNF683+ determinują wrażliwość na chemioterapię w zaawansowanym HPSCC przez przekształcanie mikrośrodowiska immunologicznego
Dlaczego niektóre chemioterapie lepiej działają w określonych nowotworach gardła
U osób z zaawansowanym rakiem krtani dolnej (hypopharyngeal cancer) — guzem ukrytym głęboko w gardle — często stosuje się silną chemioterapię o niepewnych efektach. Czasem guzy znacząco się zmniejszają, a innym razem niemal wcale nie reagują. Badanie stawia proste, lecz istotne pytanie: co różni guzy, które dobrze reagują? Analizując pojedyncze komórki układu odpornościowego, autorzy odkrywają specyficzny typ „strażnika”, który może przesądzać o powodzeniu lub niepowodzeniu standardowej chemioterapii.
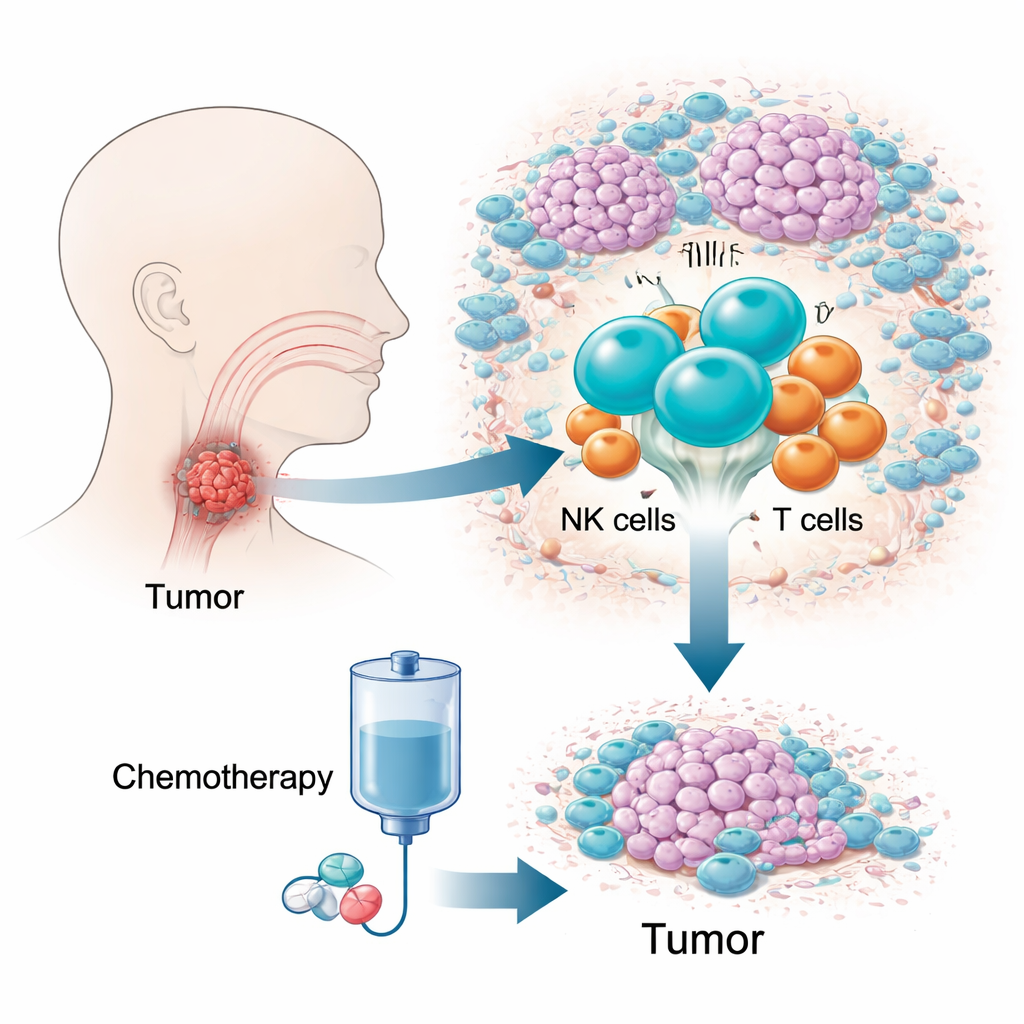
Wyzwanie ukrytego, trudnego do leczenia nowotworu
Rogowatokomórkowy rak zatoki gardłowej (hypopharyngeal squamous cell carcinoma) należy do najbardziej śmiertelnych nowotworów głowy i szyi, częściowo dlatego, że rozwija się w ciasnym, trudno dostępnym obszarze i daje niewiele objawów we wczesnym stadium. Wielu pacjentów jest diagnozowanych późno, gdy możliwości leczenia są ograniczone, a pięcioletnie przeżycie niskie. Schemat leczenia TPF jest powszechnie stosowany, bo może kontrolować chorobę przy jednoczesnym zachowaniu krtani. Mimo to u 10–20% chorych obserwuje się słabą lub brak odpowiedzi, co powoduje utratę cennego czasu. Tradycyjne testy genetyczne, uśredniające sygnały po milionach komórek, nie wyjaśniły tej różnicy, dlatego autorzy skupili się na żywym ekosystemie komórek odpornościowych w guzie.
Czytanie immunologicznego krajobrazu guza komórka po komórce
Naukowcy śledzili 12 pacjentów w czasie, pobierając próbki guza przed i po dwóch cyklach chemioterapii TPF i profilując ponad 150 000 komórek odpornościowych na poziomie pojedynczych komórek. Dodatkowo przebadali 41 pacjentów w celu potwierdzenia kluczowych odkryć za pomocą obrazowania i cytometrii przepływowej. Mapując aktywność genów i typ każdej komórki, zbudowali szczegółowy atlas mikrośrodowiska guza: komórki T, B, makrofagi, komórki dendrytyczne, mastocyty, neutrofile oraz komórki NK. Spośród tych elementów wybił się jeden wzorzec. Przed leczeniem guzy, które później się kurczyły, zawierały znacznie więcej komórek NK niż guzy oporne, a wyższy udział komórek NK korelował z większym stopniem zmniejszenia guza.
Specyficzna podgrupa komórek NK przygotowuje komórki T do działania
Wnikliwa analiza podzieliła komórki NK na trzy grupy według cech molekularnych. Tylko jedna z nich, oznaczona przez czynnik transkrypcyjny ZNF683 i występująca głównie w tkance otaczającej gniazda nowotworowe, silnie korelowała z dobrą odpowiedzią na chemioterapię. Pacjenci, których guzy zawierały więcej tych ZNF683+ komórek NK na początku, mieli znacznie większe prawdopodobieństwo korzyści z TPF. W eksperymentach na myszach usunięcie komórek NK niemal całkowicie znosiło efekt chemioterapii, co potwierdza, że aktywność NK nie jest jedynie markerem, lecz koniecznym elementem skutecznego leczenia. Co ciekawe, te komórki NK nie działały wyłącznie jako bezpośredni zabójcy nowotworu; ich programy genowe były wzbogacone o funkcje ukierunkowane na kierowanie i aktywację komórek T.
Jak komórki NK uprawniają silne zabójcze komórki T
Aby ustalić, które komórki T miały największe znaczenie, badacze śledzili poszczególne klony receptorów komórek T przed i po leczeniu. Stwierdzili, że u pacjentów odpowiadających na terapię dramatycznie rozszerzyła się specyficzna grupa komórek CD8 o fenotypie „effector memory”, bogata w cząsteczkę GZMK, po chemioterapii. Te komórki wytwarzały wysokie poziomy toksycznych cytokin TNF i interferonu gamma, nie wykazując głębokiego wyczerpania, co czyniło je potężnymi i trwałymi zabójcami. Obrazowanie przestrzenne wykazało, że po leczeniu GZMK+ komórki CD8 silnie skupiały się w guzach pacjentów odpowiadających, ale nie u nieodpowiadających. W testach współhodowli z komórek ludzkich bezpośredni kontakt z ZNF683+ komórkami NK napędzał rozrost tej podgrupy GZMK+ CD8 T, efekt który znikał, gdy komórki zostały oddzielone barierą.
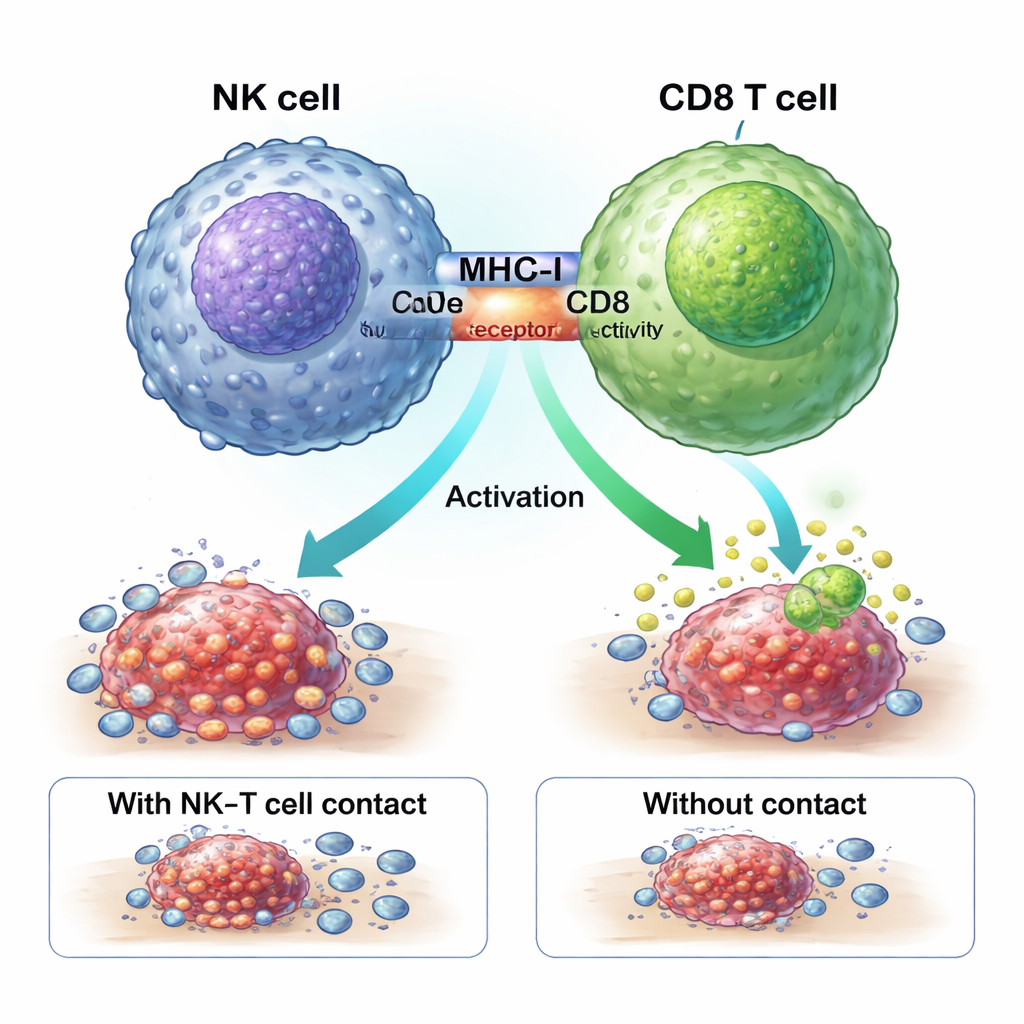
Fizyczne przybicie dłoni, które włącza bojowników przeciw nowotworowi
Badanie pokazuje, że ZNF683+ komórki NK zwiększają odpowiedź na chemioterapię poprzez fizyczne „przybicie dłoni” z komórkami CD8 T. Cząsteczki MHC-I na powierzchni komórki NK wiążą receptory CD8 na komórkach T w strefie bliskiego kontaktu, zwanej synapsą immunologiczną. Zablokowanie MHC-I powstrzymało komórki NK przed indukowaniem silnych GZMK+ komórek CD8. W specjalnie zmodyfikowanych myszach pozbawionych ZNF683 jedynie w komórkach NK, te NK wyrażały mniej MHC-I i znacznie gorzej aktywowały komórki CD8, co wzmacnia wniosek, że ZNF683 programuje komórki NK, by stały się efektywnymi trenerami komórek T, a nie prostymi egzekutorami.
Co to oznacza dla pacjentów
Dla czytelników niebędących specjalistami kluczowa wiadomość brzmi: nie wszystkie komórki odpornościowe w guzie są takie same. Praca identyfikuje specyficzną podgrupę komórek NK jako zwiadowcę, który przygotowuje pole bitwy przed rozpoczęciem chemioterapii. Guzy bogate w te komórki są gotowe do uwolnienia fal silnych komórek CD8 po zastosowaniu leków, co prowadzi do znacznie lepszego kurczenia się guza. Pomiar obfitości tej osi NK–T przed leczeniem mógłby pomóc lekarzom przewidzieć, kto skorzysta z chemioterapii TPF, a kto może potrzebować alternatywnych lub dodatkowych terapii. W przyszłości terapie zwiększające lub naśladujące działanie tych ZNF683+ komórek NK mogłyby przekształcić odporne raki zatoki gardłowej w guzy znacznie bardziej wrażliwe na standardową chemioterapię.
Cytowanie: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Słowa kluczowe: rak gardłowy, oporność na chemioterapię, komórki NK (natural killer), nowotworowe mikrośrodowisko immunologiczne, komórki CD8 T