Clear Sky Science · pl
Kombinatoryjna różnicacja ludzkich indukowanych komórek pluripotencjalnych generuje funkcjonalny nabłonek grasicy prowadzący rozwój komórek dendrytycznych oraz limfocytów T CD4/CD8
Tworzenie pola szkoleniowego dla komórek odpornościowych
Ludzki układ odpornościowy zależy od małego, delikatnego narządu zwanego grasica, w którym nowe komórki T uczą się rozpoznawać patogeny, nie atakując przy tym własnego organizmu. W miarę starzenia się lub w niektórych chorobach genetycznych grasica ulega zanikowi lub nie rozwija się prawidłowo, co pozostawia ludzi podatnych na infekcje i nowotwory. W tym badaniu naukowcy pokazują, jak odtworzyć kluczowe części grasicy w laboratorium, wykorzystując przeprogramowane komórki macierzyste, otwierając drogę do tworzenia spersonalizowanego układu odpornościowego i bezpieczniejszych, lepiej kontrolowanych terapii z udziałem komórek T.
Dlaczego grasica jest ważna
Grasica pełni funkcję „szkoły” dla komórek T, rodzaju białych krwinek patrolujących organizm w poszukiwaniu zakażonych lub nowotworowych komórek. W grasicy rozwijane komórki T są testowane: te, które prawidłowo reagują na obce cele, są zachowywane, natomiast te, które mogłyby atakować własny organizm, są eliminowane. Ten proces edukacji orchestrują wyspecjalizowane komórki wspierające zwane nabłonkowymi komórkami grasicy (TEC), które tworzą odrębne obszary znane jako kora i rdzeń. Odtworzenie tych TEC poza organizmem było trudne, a większość wcześniejszych prób dawała niedojrzałe komórki, które musiały być przeszczepione do zwierząt, by zakończyć rozwój.
Kierowanie komórkami macierzystymi krok po kroku
Aby to przezwyciężyć, badacze zaczęli od ludzkich indukowanych komórek pluripotentnych, które można uzyskać z tkanek dorosłego i następnie nakłonić do różnicowania w niemal każdy typ komórek. Opracowali starannie zaplanowaną, dwutygodniową „mapę drogową”, która naśladuje tworzenie grasicy w trakcie wczesnego rozwoju. Wykorzystując statystyczną strategię zwaną planowaniem eksperymentu, w połączeniu z szerokimi pomiarami aktywności genów, przetestowali wiele kombinacji sygnałów wzrostowych równolegle. Poprzez precyzyjne włączanie lub wyłączanie kluczowych szlaków w określonych momentach, doprowadzili komórki macierzyste przez kilka etapów pośrednich ku progenitorom nabłonkowym grasicy — niedojrzałym komórkom podobnym do TEC, które wykazują charakterystyczną ekspresję genów takich jak FOXN1 i PAX9 oraz przypominają wczesne komórki korowe grasicy.
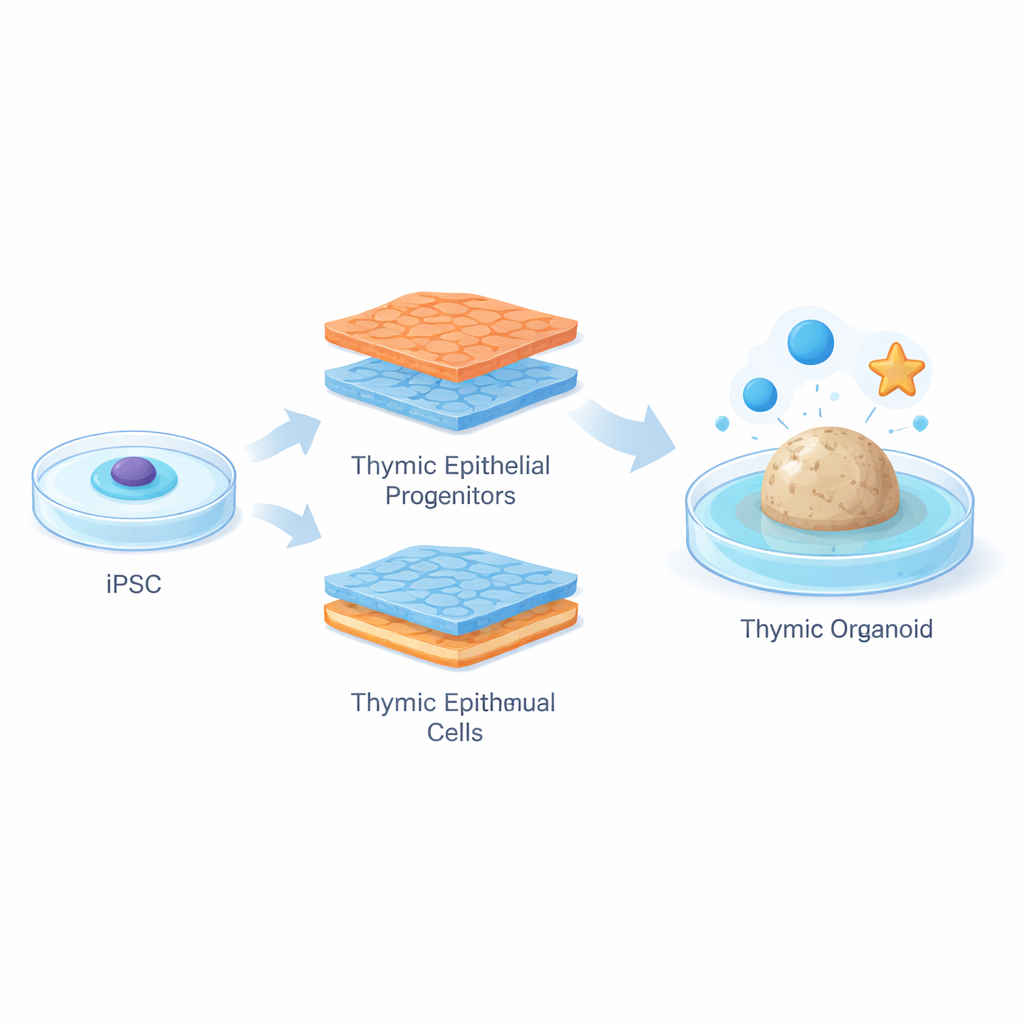
Skladanie miniaturowych organoidów grasicy
Mając duże liczby tych komórek progenitorowych, zespół wymieszał je z rzadkimi prekursorami krwiotwórczymi świeżo izolowanymi z ludzkiej tkanki grasicy. Mieszankę skompresowano w małe skupiska i osadzono w miękkim żelu fibrynowym na styku powietrze–ciecz, tworząc trójwymiarowe „ludzkie organoidy grasicy”. W ciągu kilku dni organoidy rozrosły się w złożone kule z wypustkami przebijającymi żel. Szczegółowe obrazowanie i analizy genów wykazały, że wiele komórek nabłonkowych w tych organoidach dojrzało do komórek przypominających rdzeń, które wykazywały wysoką ekspresję HLA-DR, cząsteczki niezbędnej do prezentacji antygenów własnych rozwijającym się komórkom T. Organoidy zaczęły także wyrażać szeroki zestaw genów typowych dla tkanek, odzwierciedlając sposób, w jaki prawdziwe komórki rdzenia grasicy pomagają w utrwalaniu tolerancji na różne narządy.
Szkolenie wielu typów komórek odpornościowych
Organoidy zrobiły nie tylko „na wygląd” jak tkanka grasicy — funkcjonowały jak ona. Po kilku tygodniach, gdy naukowcy zbadali komórki pochodzące z krwi, stwierdzili, że wczesne progenitory utraciły tożsamość komórek macierzystych i rozwinęły się w limfocyty T posiadające kompletne receptory TCR. Pojawiły się obie główne gałęzie komórek T: konwencjonalne limfocyty alfa–beta oraz gamma–delta. Wśród nich znaleziono dojrzałe pojedynczo pozytywne komórki T CD4 i CD8 z markerami powierzchniowymi (CCR7 i CD62L) typowymi dla niedawno opuszczających grasicę limfocytów gotowych wejść do krążenia. Profilowanie pojedynczych komórek wykazało również, że część progenitorów w organoidach obrała inną ścieżkę, różnicując się w komórki dendrytyczne — kolejny kluczowy typ komórek odpornościowych, który współpracuje z TEC w kształtowaniu bezpiecznego repertuaru limfocytów T.
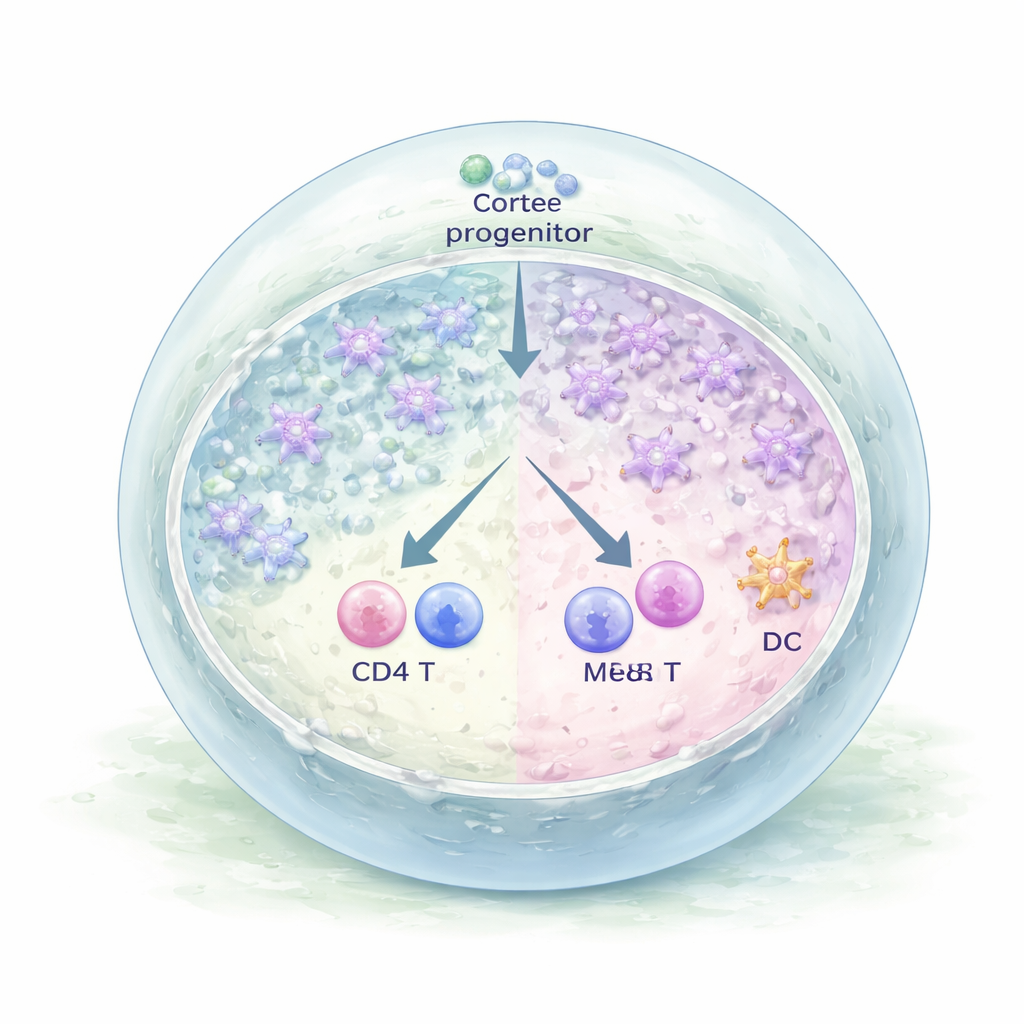
Od modelu laboratoryjnego do przyszłych terapii
Podsumowując, praca ta dostarcza w pełni in vitro ludzkopodobny organoid grasicy zbudowany z komórek pluripotentnych, który potrafi kierować niedojrzałymi komórkami krwi ku różnorodnym, funkcjonalnym limfocytom T i komórkom dendrytycznym. Dla czytelnika popularnonaukowego najważniejszy wniosek jest taki, że badacze uczą się odbudowywać grasicę w naczyniu — zarówno jej strukturę, jak i funkcję edukacyjną. Przy dalszych udoskonaleniach takie organoidy mogłyby pomóc naprawiać uszkodzone układy odpornościowe u dzieci urodzonych bez działającej grasicy, odmłodzić produkcję komórek T u starszych osób oraz zapewnić kontrolowaną „fabrykę” do wytwarzania spersonalizowanych komórek T do immunoterapii przeciwko nowotworom i innym terapiom opartym na komórkach.
Cytowanie: Provin, N., d’Arco, M., Le Bozec, A. et al. Combinatory differentiation of human induced pluripotent stem cells generates functional thymic epithelium driving dendritic cell and CD4/CD8 T cell development. Nat Commun 17, 1969 (2026). https://doi.org/10.1038/s41467-026-68675-y
Słowa kluczowe: organoidy grasicy, indukowane komórki pluripotentne, rozwój limfocytów T, nabłonkowe komórki grasicy, immunologia regeneracyjna