Clear Sky Science · pl
Fotosynteza glicyny poprzez sprzęganie C−N odpadów z plastiku i azotanu nad diatomicznym katalizatorem Pd−B
Przekształcanie śmieci w elementy budulcowe życia
Butelki plastikowe, pojemniki na żywność i ubrania z poliestru są wszędzie — podobnie jak pozostawiane przez nie odpady. Równocześnie wiele zakładów wypuszcza ścieki obciążone azotanami, które mogą zanieczyszczać rzeki i morza. W tym badaniu pokazano, jak można rozwiązać oba problemy naraz: wykorzystując światło słoneczne i specjalnie zaprojektowany katalizator do przekształcenia wyrzuconego plastiku i azotanu w glicynę, prosty aminokwas szeroko stosowany w przemyśle spożywczym, medycynie i rolnictwie.
Dlaczego glicyna i odpady są istotne
Glicyna jest jednym z podstawowych składników budulcowych białek i jest produkowana w ilościach rzędu setek tysięcy ton rocznie. Tradycyjne metody przemysłowe, zwłaszcza klasyczny proces Streckera, opierają się na toksycznych związkach cyjankowych i surowych warunkach reakcji, co rodzi obawy dotyczące bezpieczeństwa i środowiska. Tymczasem globalna produkcja PET — stosowanego w butelkach, tekstyliach i opakowaniach — przekracza 100 milionów ton rocznie, z czego ponad 80% trafia na składowiska lub do środowiska. Przy chemicznym rozkładzie PET powstaje m.in. glikol etylenowy, niskowartościowy płyn, którego oczyszczanie jest kosztowne. Autorzy stawiają proste pytanie: zamiast traktować glikol etylenowy i azotan jako odpady, czy można je wykorzystać jako substraty do wytwarzania wartościowej glicyny, używając tylko światła słonecznego?
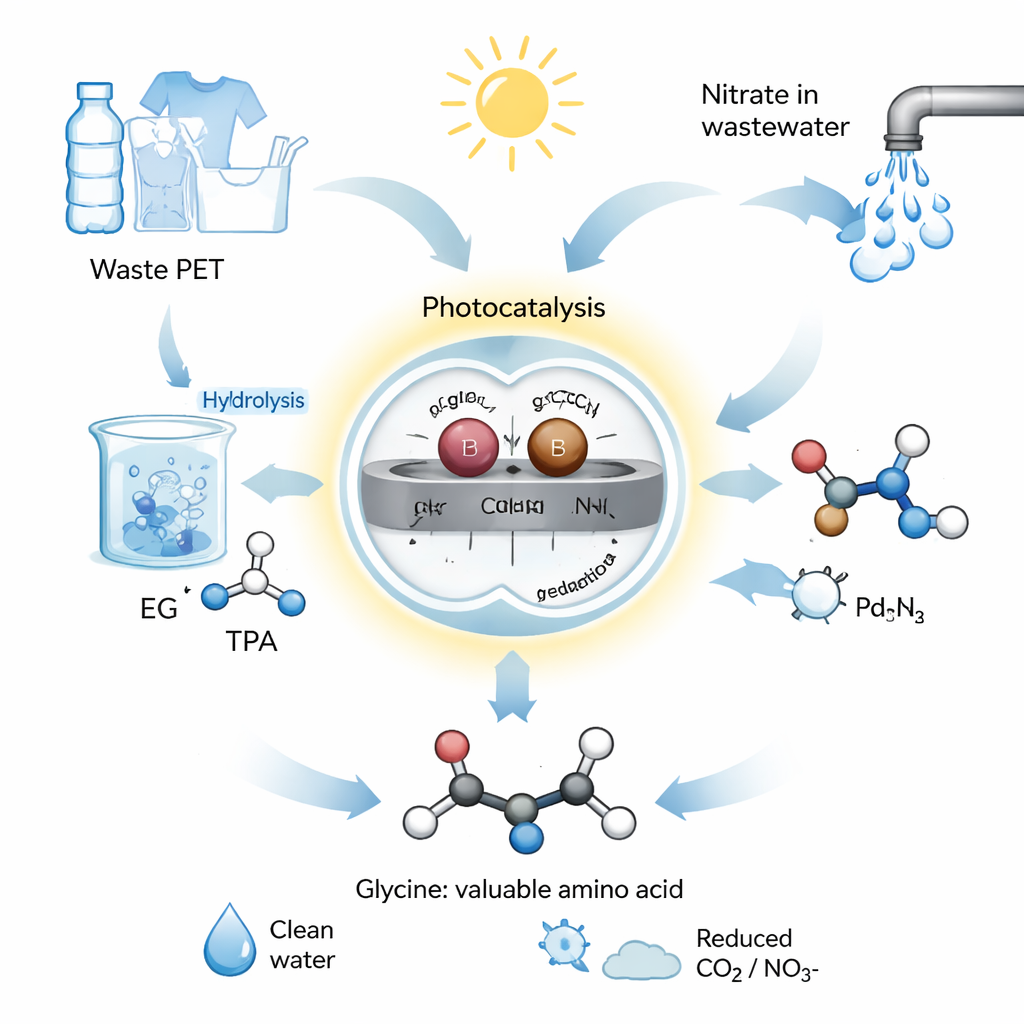
Napędzana słońcem chemiczna skrót
Zespół zaprojektował system fotokatalityczny, czyli wykorzystujący światło do napędzania reakcji chemicznych. Zbudowali katalizator z grafitowego węglika azotu, półprzewodnika, na powierzchni którego ulokowali pary pojedynczych atomów palladu (Pd) i boru (B). Te sparowane atomy działają jak mikroskopijny dwuosobowy zespół, z każdą częścią zajmującą się inną połową chemii. W ich procesie odpady PET są najpierw hydrolizowane — rozdzielane w zasadowej wodzie — co uwalnia glikol etylenowy. Ten glikol i azotan ze ścieków umieszcza się następnie w wodzie z katalizatorem Pd–B i wystawia na działanie symulowanego lub naturalnego światła słonecznego. W tych łagodnych warunkach system przekształca mieszaninę w glicynę z wysoką wydajnością i selektywnością ponad 92%, co oznacza, że powstaje bardzo mało niepożądanych produktów ubocznych.
Jak działa atomowe duo
Sukces katalizatora zależy od tego, jak zarządza on krótkotrwałymi pośrednimi produktami reakcji. Miejsca borowe na powierzchni są „bogate w dziury” — chętnie akceptują ładunek dodatni, gdy materiał absorbuje światło. W tych miejscach B glikol etylenowy jest łagodnie utleniany — pozbawiany wodoru — do glikoksyalduhydu, niestabilnej cząsteczki, która zwykle ma tendencję do nadutleniania do kwasów lub nawet dwutlenku węgla. Miejsca z palladem są natomiast „bogate w elektrony”. Wykorzystują one generowane przez światło elektrony do redukcji azotanu stopniowo do jonów amonowych lub amoniaku. Kluczowym etapem jest sprzęganie węgla z azotem między glikoksyaldehydem a tymi gatunkami azotowymi w celu powstania etanolaminy, która następnie jest dalej utleniana, głównie znów w miejscach B, do glicyny. Stabilizując glikoksyaldehyd wystarczająco długo, by zaszedł pożądany przebieg reakcji, i utrzymując elektrony oraz dziury przestrzennie rozdzielone, para Pd–B kieruje chemię z dala od marnotrawnych reakcji ubocznych ku pożądanemu aminokwasowi.
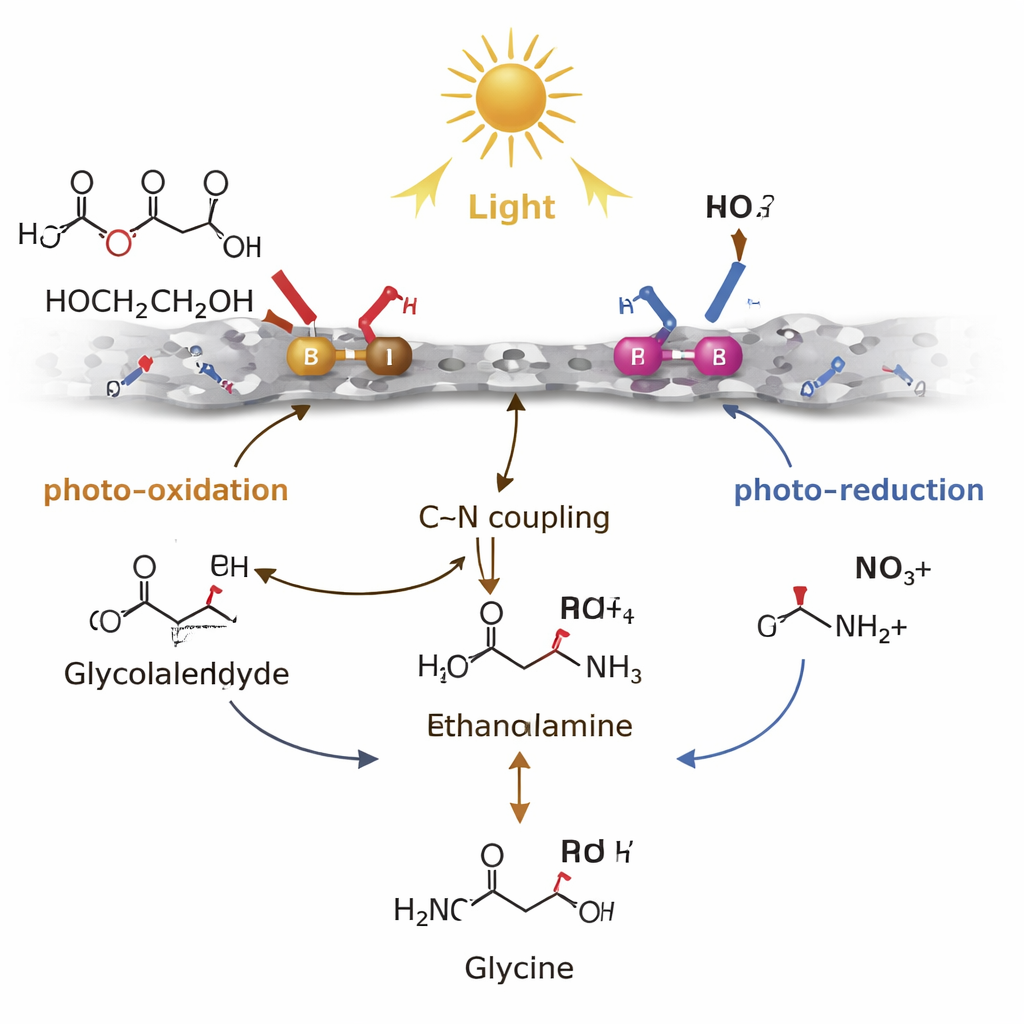
Od mechanizmu w laboratorium do rzeczywistych odpadów
Naukowcy potwierdzili każdą część tej ścieżki za pomocą zestawu technik, śledząc rodniki, pośrednie produkty i produkty azotowe w czasie rzeczywistym. Porównali różne materiały katalizatorów i metale, znajdując że podłoża g‑C3N4 z izolowanymi parami Pd–B dawały najlepsze wyniki, osiągając tempo produkcji glicyny 2,9 milimola na gram katalizatora na godzinę. Katalizator pozostawał aktywny przez powtarzane cykle i jego struktura pozostała stabilna. Co ważne, zespół wyszedł poza czyste związki laboratoryjne. Zademonstrowali produkcję glicyny w skali gramowej rozpoczynając od rzeczywistego post‑konsumenckiego PET — proszku, butelek, ubrań, toreb i innych — w połączeniu z roztworami azotanów, a nawet złożonymi ściekami. Pokażono też, że pokrewne alkohole pochodzenia biomasowego, takie jak glicerol, mogą służyć jako alternatywne źródła węgla, rozszerzając zastosowalność podejścia.
Korzyść dla odpadów i klimatu
Aby przybliżyć koncepcję do praktyki, autorzy przetestowali proces w naturalnym świetle słonecznym skupionym za pomocą prostej soczewki Fresnela. System konsekwentnie produkował glicynę o wysokiej selektywności, a modelowanie sugeruje, że jego skalowanie mogłoby zapobiec znacznym emisjom dwutlenku węgla i uniemożliwić wypływ azotanów do środowiska. Mówiąc prosto, praca ta przedstawia sposób przekształcenia stosów zużytego plastiku i zanieczyszczonej wody w użyteczny aminokwas, wykorzystując jedynie światło i precyzyjnie zaprojektowany katalizator. Choć przed wdrożeniem przemysłowym pozostają wyzwania inżynieryjne, badanie podkreśla, jak projektowanie katalizatora na poziomie atomowym może połączyć dwa główne strumienie odpadów w jeden wartościowy produkt chemiczny.
Cytowanie: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Słowa kluczowe: glicyna, recykling plastiku, fotokataliza, ściek azotanowy, katalizatory jednoatomowe