Clear Sky Science · pl
Regulacja składu adaptorowego AP1 przez dwurękowego chaperona MEA1
Dlaczego ten ukryty pomocnik komórkowy ma znaczenie
W każdej komórce ludzkiej tysiące maleńkich paczek przewożą białka tam, gdzie są potrzebne, albo do „centrum recyklingu” komórki w celu rozkładu. Ten ruch utrzymuje komórki w zdrowiu i reguluje nasze mechanizmy odpornościowe. Artykuł streszczony tutaj odsłania dotąd tajemnicze białko o nazwie MEA1, które okazuje się niezbędne do budowy jednego z kluczowych mechanizmów sortujących ładunki. Zrozumienie działania MEA1 pomaga wyjaśnić, jak komórki kontrolują istotne ładunki, w tym molekuły przełączające odpowiedzi przeciwwirusowe włącz/wyłącz.
Kontrola ruchu w centrach dystrybucji komórki
Większość aktywności transportowej komórki przebiega przez strukturę zwaną aparatem Golgiego — stos spłaszczonych pęcherzyków działający jak centralna poczta. Z Golgiego ładunki mogą być wysyłane na powierzchnię komórki albo kierowane do wnętrza komórki w celu degradacji. Kompleks białkowy znany jako AP1 znajduje się w centrum tej trasy. AP1 rozpoznaje znaczniki na białkach ładunkowych, pomaga zgiąć błonę i rekrutuje zewnętrzną osłonkę z klatryny, tworząc małe pęcherzyki transportowe. Bez prawidłowo złożonego AP1 kluczowe ładunki gromadzą się w niewłaściwych miejscach, a normalne szlaki sygnalizacyjne, w tym powiązane z odpornością, mogą działać nieprawidłowo. 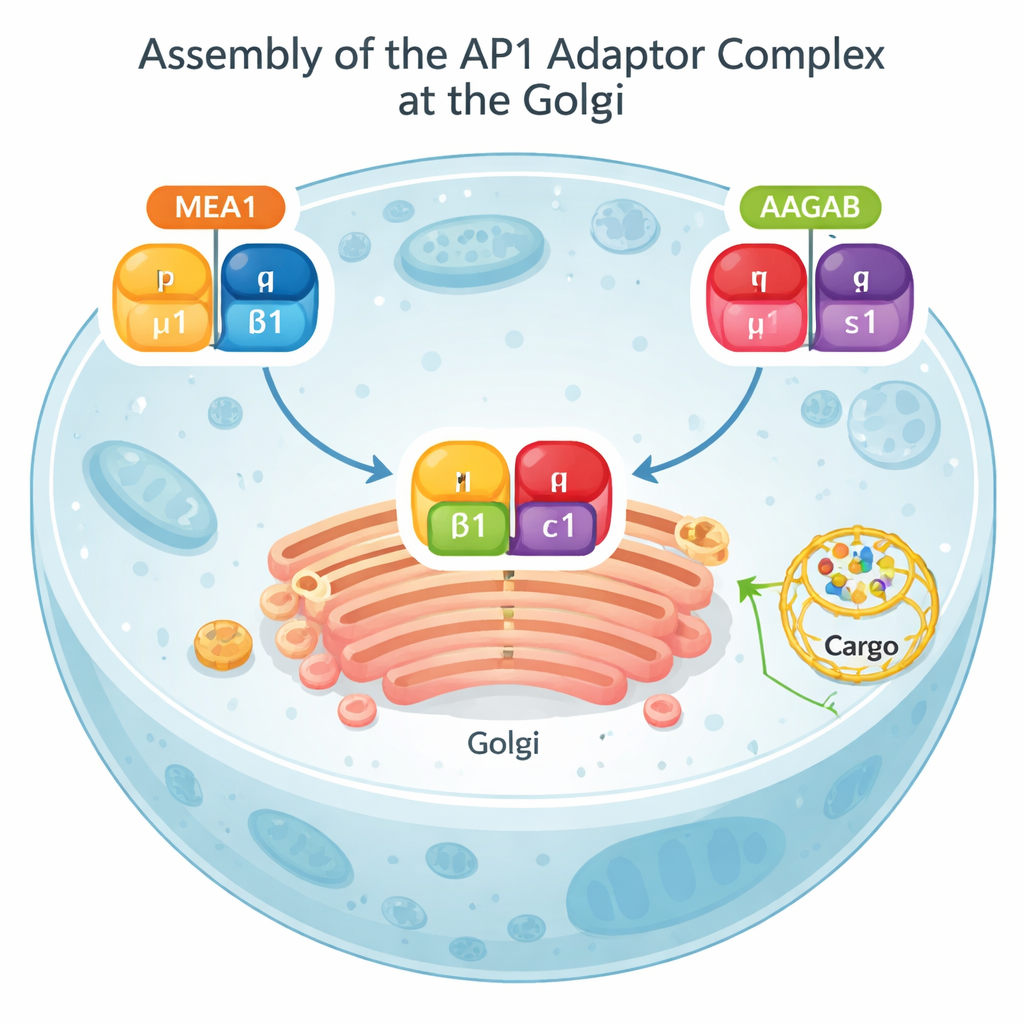
Odnalezienie brakującego pracownika montażu
Autorzy postanowili zidentyfikować białka fizycznie współdziałające z AP1, które mogłyby pomagać w jego składaniu. Przeszukali dużą bazę interakcji białkowych, odfiltrowali kandydatów mało prawdopodobnych do współpracy z AP1, a następnie użyli narzędzia sztucznej inteligencji AlphaFold, by przewidzieć, jak pozostałe białka mogłyby kontaktować się z poszczególnymi częściami AP1. W tym poszukiwaniu wyróżnił się MEA1 — niewielkie, wcześniej nieopisane białko obecne w wielu tkankach. Doświadczenia następcze w komórkach ludzkich potwierdziły, że MEA1 wiąże dwie konkretne podjednostki AP1, znane jako μ1 i β1, zarówno gdy były testowane osobno, jak i w ich naturalnych, niezmodyfikowanych formach.
MEA1 utrzymuje integralność AP1 i przepływ ładunków
Aby zbadać funkcję MEA1, badacze usunęli gen MEA1 w liniach komórkowych człowieka. W przypadku braku MEA1 wszystkie cztery składniki AP1 zostały drastycznie zredukowane, a charakterystyczne skupiska AP1 w pobliżu Golgiego niemal zniknęły. Utrata ta miała wyraźne konsekwencje funkcjonalne. Jeden z ładunków AP1, receptor folianu FOLR1, nagromadził się na powierzchni komórki zamiast być skierowany do wnętrza — objaw wadliwego sortowania przez AP1. Inny ładunek, białko sygnalizacyjne odporności STING, nie był już skutecznie pakowany do pęcherzyków kierowanych do lizosomów, czyli komórkowych centrów recyklingu. W rezultacie aktywne STING i jego partnerowa kinaza TBK1 utrzymywały się na wysokich poziomach, co wskazuje, że „wyłącznik” tej przeciwwirusowej ścieżki nie działał prawidłowo. Ponowne wprowadzenie MEA1 przywróciło poziomy AP1 i skorygowało te defekty w transporcie.
Dwurękowy chaperon i proces montażu oparty na zderzeniach
Testy biochemiczne i modele AlphaFold wykazały, że MEA1 działa jak „dwurękowy” chaperon montażowy: jego przednia część chwyta podjednostkę μ1, podczas gdy tylna część chwyta β1. Samodzielnie μ1 i β1 są niestabilne i mają tendencję do agregacji lub degradacji; w związaniu z MEA1 stają się rozpuszczalne i gotowe do montażu. Inny znany chaperon, AAGAB, pełni równoległą rolę dla pozostałych dwóch podjednostek AP1, γ i σ1. Kiedy kompleksy MEA1–μ1–β1 i AAGAB–γ–σ1 spotykają się, ich podjednostki łączą się w kompletny, czteroczęściowy adaptor AP1. W tym momencie oba chaperony odłączają się i wracają do cytosolu, podczas gdy nowo złożony AP1 przemieszcza się do błon, by wykonywać zadania sortujące. Ten mechanizm „zderzenia podwójnych chaperonów” pokazuje, że składanie AP1 jest starannie zorganizowane, a nie zostawione przypadkowi.
Szersze wnioski o kontroli jakości w komórce
Poza AP1, badanie sugeruje bardziej ogólną strategię, jaką komórki mogą wykorzystywać do budowy wielu dużych maszyn białkowych. MEA1 może też słabo wspierać inny kompleks adaptorowy, AP2, a wraz z AAGAB i trzecim chaperonem o nazwie CCDC32 ilustruje szerszą ścieżkę, którą autorzy określają jako „Chaperone-assisted Adaptor Protein Assembly”. W tym schemacie wyspecjalizowane chaperony stabilizują kruche podjednostki, łączą właściwe pary i tymczasowo blokują miejsca wiążące ładunki, aż kompleks zostanie w pełni uformowany i bezpieczny do użycia. 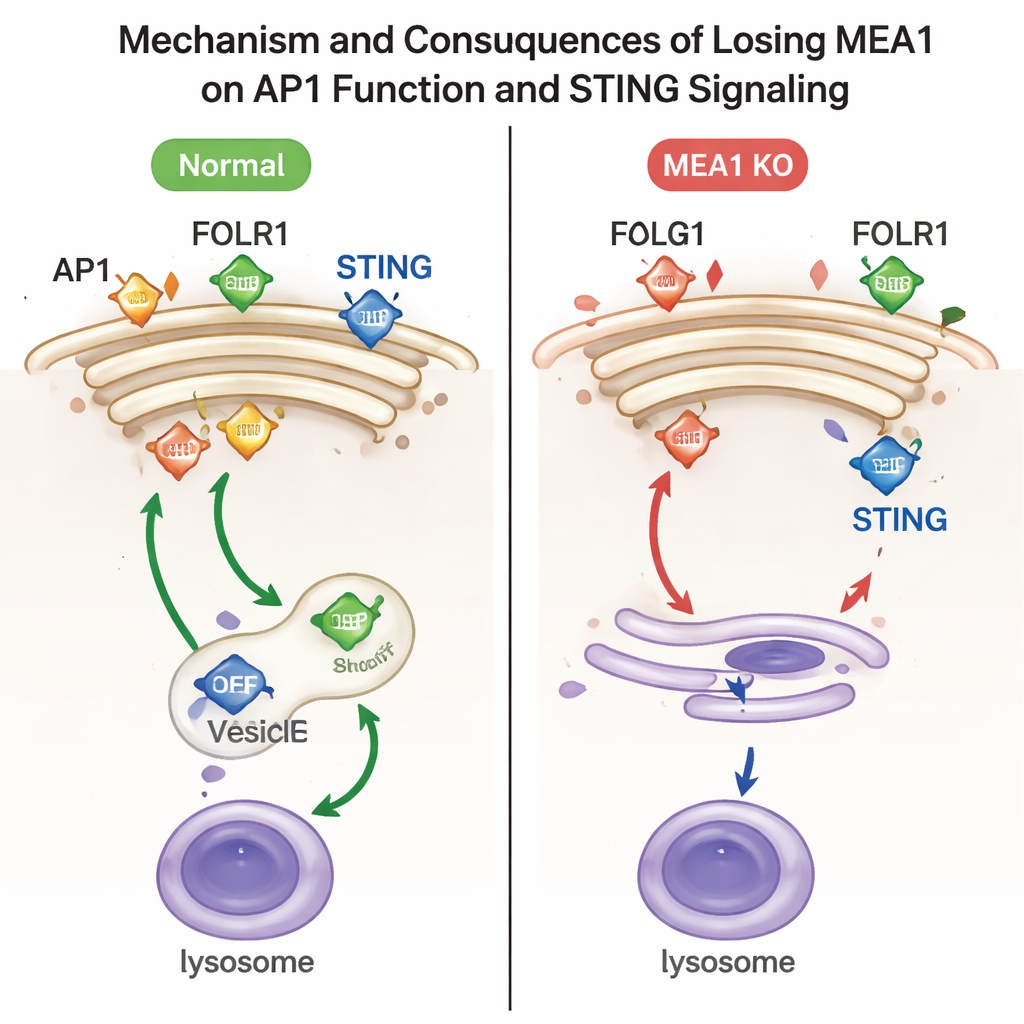
Co to oznacza dla zdrowia i chorób
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że MEA1 to istotny, działający za kulisami pracownik, który pomaga składać AP1 — podstawową maszynę sortującą w naszych komórkach. Gdy MEA1 jest nieobecny, AP1 się rozpada, powstają korki w ruchu wewnątrzkomórkowym, a ważne regulatory, takie jak STING, nie są prawidłowo wyłączane. Nowe poznanie może w przyszłości pomóc wyjaśnić niektóre zaburzenia odpornościowe lub inne choroby związane z wadliwym transportem białek i ujawnia ogólną zasadę, jak komórki bezpiecznie budują złożone maszyny molekularne z niestabilnych elementów.
Cytowanie: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Słowa kluczowe: transport białek, białko adaptora AP1, chaperony molekularne, sygnalizacja STING, biologia komórki