Clear Sky Science · pl
Rozpoznawanie cząsteczki tyreoglobuliny przez sortylinę
Jak komórki tarczycy decydują, kiedy uwolnić hormon
Hormony tarczycy ustawiają nasz metaboliczny „termometr”, wpływając na wszystko, od częstości akcji serca po temperaturę ciała. Hormony te są syntetyzowane i przechowywane wewnątrz olbrzymiego białka zwanego tyreoglobuliną. W badaniu tym wykazano, w jaki sposób inne białko, sortylina, pomaga komórkom tarczycy wybierać formę tyreoglobuliny, którą należy pobrać z powrotem do wnętrza komórki, aby hormon mógł zostać uwolniony do krwi – decyzję, która ostatecznie wpływa na ilość hormonów tarczycy dostępnych dla organizmu.
Białko magazynujące oczekujące na przetworzenie
Tyreoglobulina to ogromne, Y-kształtne białko produkowane i wydzielane przez komórki tarczycy do żelopodobnej przestrzeni zwanej koloidem. Działa tam zarówno jako surowiec, jak i magazyn dla hormonów tarczycy: określone reszty aminokwasowe w tyreoglobulinie są chemicznie modyfikowane przez jodowanie, tworząc hormony tarczycy, które pozostają osadzone w większym białku. Aby uwolnić te hormony, tyreoglobulina musi zostać zpowrotem pobrana do komórki, pocięta wewnątrz kompartmentów recyklingowych zwanych lizosomami, a fragmenty hormonalne przetransportowane do krwi.
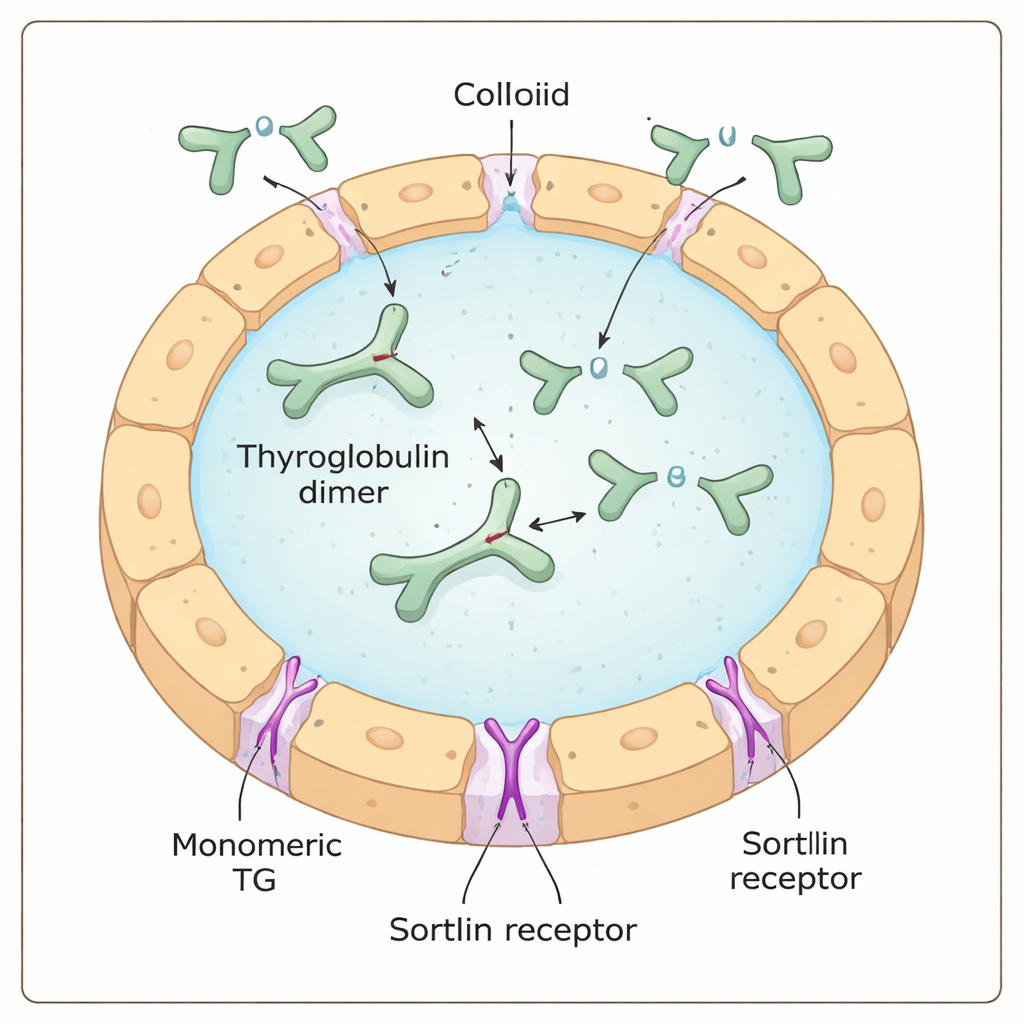
Komórkowy strażnik z ukrytą preferencją
Receptor sortylina został zaproponowany jako jeden ze „strażników”, które wiążą tyreoglobulinę na powierzchni komórki i kierują jej internalizację. Wcześniejsze prace sugerowały, że sortylina preferuje silnie iodowaną tyreoglobulinę, co dawało nadzieję, że receptor może bezpośrednio rozpoznawać zawartość jodu. Stosując kombinację testów biochemicznych, pomiarów masy pojedynczych cząsteczek i eksperymentów pobierania przez komórki, autorzy wykazali natomiast, że sortylina zdecydowanie faworyzuje jednoukładową, czyli monomeryczną, formę tyreoglobuliny w porównaniu z jej częstszą formą dwuczłonową, dimerem. Im więcej monomerów w próbce, tym wydajniej tworzyły one kompleksy ze sortyliną i były internalizowane przez komórki tarczycy, niezależnie od zawartości jodu.
Zbliżenie na punkt kontaktowy
Aby zrozumieć tę preferencję na poziomie atomowym, zespół zastosował wysokorozdzielczą kryo‑mikroskopię elektronową oraz spektrometrię mas po reakcji utwardzającej (cross-linking). Metody te pokazały, że sortylina rozpoznaje krótki, wiotki ogonek przy końcu C-terminus monomerycznej tyreoglobuliny. Ten ogonek wsuwa się do centralnej jamy sortyliny, przypominającej dziesięcioramienny wirnik, zakotwiczając się w dwóch małych „gorących punktach” wewnątrz. Co istotne, w formie dimeru fragment otaczający ten ogonek jest częściowo ukryty i niedostępny dla sortyliny, co wyjaśnia słabą współpracę dimera. Dane sugerują, że przycinanie lub rozluźnianie tyreoglobuliny na zewnątrz komórki — przez naturalne procesy degradacji białka — pomaga przekształcać dimery w monomery, które sortylina może wychwycić.
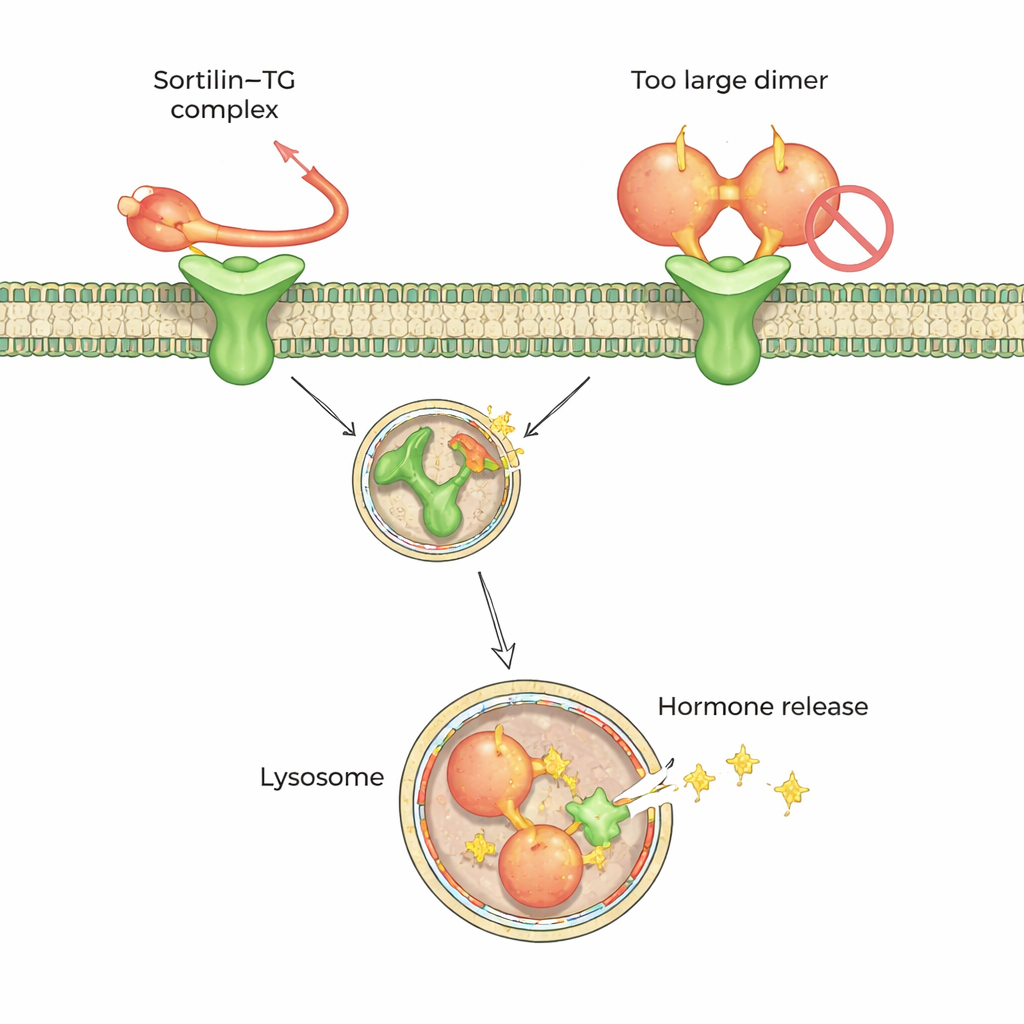
Wspólny kod dokowania dla wielu ładunków
Sortylina nie jest białkiem specyficznym tylko dla tarczycy; uczestniczy w transporcie wielu różnych cząsteczek w całym organizmie, w tym czynników związanych z chorobami serca i zaburzeniami mózgu. Łącząc ustalenia strukturalne z zaawansowanymi narzędziami do przewidywania struktur, takimi jak AlphaFold i AlphaPulldown, badacze porównali, w jaki sposób dziesiątki znanych partnerów sortyliny mogą wiązać jej jamę w kształcie wirnika. Odkryli powtarzalny wzorzec: wiele ładunków prezentuje nieuporządkowany odcinek peptydowy o długości około dwudziestu aminokwasów, który pasuje do tej samej kieszeni, co ogonek tyreoglobuliny, czasem biegnąc w tym samym kierunku co znany peptyd mózgowy neurotensyna, a czasem w kierunku przeciwnym. Pomimo odwrotnej orientacji, te peptydy mają podobne cechy — grupę kwaśną lub ujemnie naładowaną na jednym końcu, masywny aromatyczny resztę na drugim oraz elastyczny, często bogaty w prolinę odcinek pośrodku.
Dlaczego jod ma mniejsze znaczenie niż kształt
Ponieważ kluczowy kontakt między sortyliną a tyreoglobuliną stanowi ten elastyczny ogonek, autorzy sprawdzili, czy iodowanie tyrozyny tworzącej hormon w ogonku zmieni wiązanie. Nie zmieniło: syntetyczny peptyd niosący w pełni uformowany hormon tarczycy zachowywał się niemal identycznie jak wersja niemodyfikowana. Modelowanie wykazało, że pierścień z jodem wystaje do roztworu bez tworzenia nowych ciasnych kontaktów. Wraz z eksperymentami pobierania dowodzi to zrewidowanego spojrzenia: sortylina nie „liczy” atomów jodu na tyreoglobulinie. Raczej rozpoznaje, czy białko uległo rozluźnieniu lub częściowej degradacji na tyle, by odsłonić monomeryczną formę i ogonek w odpowiedni sposób.
Co to oznacza dla zdrowia tarczycy
Dla osoby niebędącej specjalistą główny wniosek jest taki, że uwalnianie hormonów tarczycy zależy mniej od wrodzonego czujnika jodu, a bardziej od mechanicznej kontroli kształtu i elastyczności białka. Sortylina działa jak skaner na powierzchni komórki, wyszukując molekuły tyreoglobuliny rozluźnione lub przycięte do postaci monomerów, po czym wciąga je do środka w celu ostatecznego uwolnienia hormonów i recyklingu jodu. Praca ta wyjaśnia kluczowy etap w biologii hormonów tarczycy i sugeruje, że leki blokujące sortylinę — dziś badane w kontekście innych chorób — mogą niezamierzenie zmieniać gospodarkę hormonów tarczycy przez zaburzenie tego etapu rozpoznawania.
Cytowanie: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Słowa kluczowe: hormon tarczycy, tyreoglobulina, sortylina, transport białek, endocytoza