Clear Sky Science · pl
Helisa mostka Cas12a jako allosteryczny regulator formowania R-pętli i aktywacji RuvC
Dlaczego ma to znaczenie dla edycji genów
Wiele potężnych narzędzi do edycji genów, w tym tych wykorzystywanych w nowych terapiach i szybkich testach diagnostycznych, opiera się na białkach CRISPR, które przecinają DNA w wybranych miejscach. Jeśli jednak te molekularne nożyce tną niewłaściwe miejsce, mogą wywołać szkodliwe skutki uboczne. W niniejszym badaniu rozłożono na czynniki pierwszy mały ruchomy element wewnątrz edytora Cas12a, zwany helisą mostka, i pokazano, jak zmiany jego kształtu działają jak wewnętrzny bezpiecznik łączący prawidłowe rozpoznanie celu z cięciem DNA. Zrozumienie tego przełącznika dostarcza wskazówek do inżynierii narzędzi CRISPR, które będą zarówno precyzyjne, jak i bezpieczniejsze w zastosowaniach medycznych i biotechnologicznych.
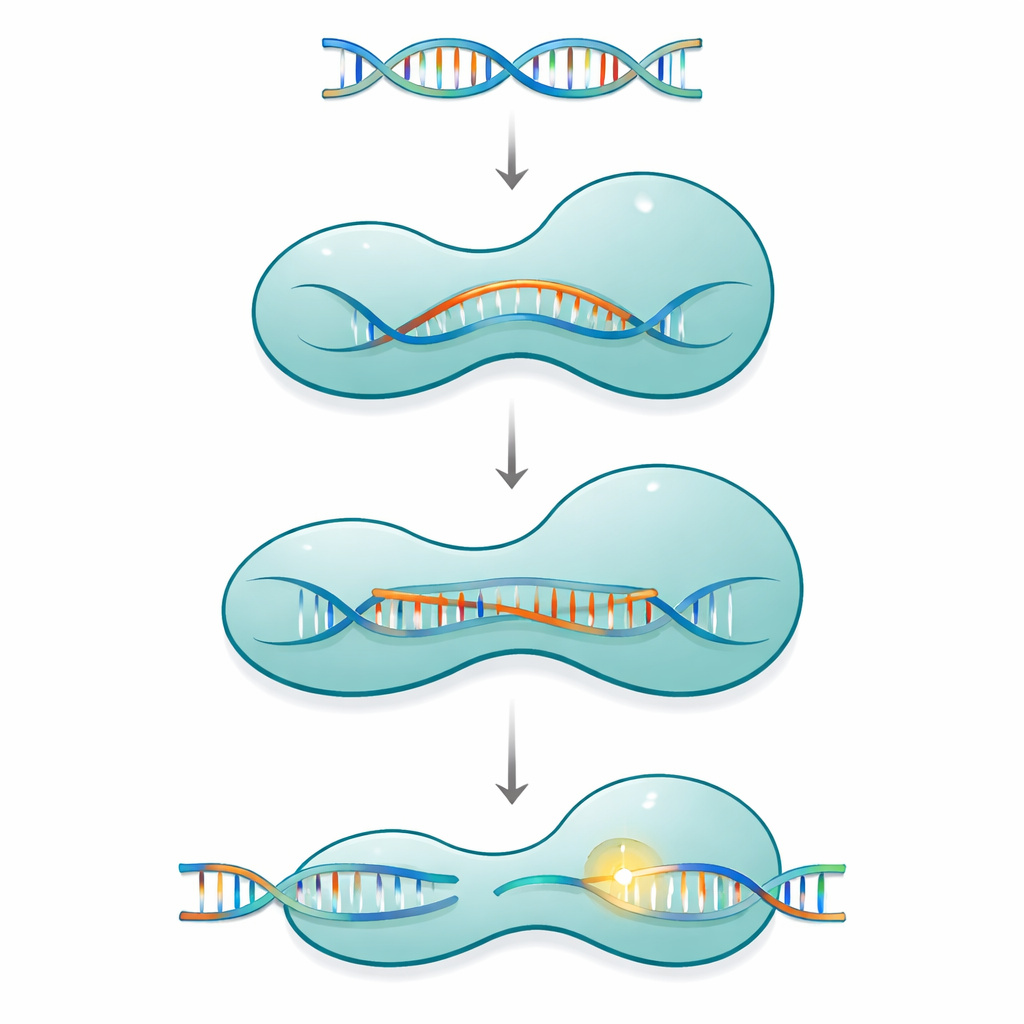
Molekularny zacisk z ruchomymi częściami
Cas12a należy do rodziny jednopodjednostkowych systemów CRISPR, które używają krótkiego RNA-przewodnika do odnajdywania i przecinania dopasowanego DNA w wirusach lub w genomie komórki. Białko ma kształt zacisku z dwiema ramionami: stronę rozpoznawczą sprawdzającą sekwencję oraz stronę tnącą, gdzie mieści się maszyna chemiczna. Te dwie połówki łączy smukły, dodatnio naładowany segment zwany helisą mostka. W miarę wiązania przez Cas12a RNA-przewodnika, a następnie docelowego DNA, białko nie zachowuje się jak sztywne narzędzie. Zamiast tego przechodzi przez serię dużych i małych zmian kształtu, które stopniowo zamykają się wokół rosnącej hybrydy RNA–DNA znanej jako R-pętla, aktywując miejsce cięcia dopiero wtedy, gdy utworzy się wystarczająco długi odcinek poprawnego parowania zasad.
Badanie wbudowanego bezpiecznika
Naukowcy skupili się na Cas12a pochodzącym od bakterii Francisella novicida oraz na wcześniej zaprojektowanej wersji, w której dwa aminokwasy w helisie mostka zostały zastąpione prolinami — zmianą znaną z usztywniania lub łamania helis. Ten wariant, nazwany FnoCas12aKD2P, tnie DNA bardziej selektywnie, ale wolniej niż białko naturalne. Dzięki krioelektronowej mikroskopii uchwycono pięć odrębnych strukturalnych migawkowych stanów tego wariantu związanych z RNA-przewodnikiem i fragmentem docelowego DNA. Migawki te pokazują białko na różnych etapach ścieżki aktywacji — od wczesnego rozpoznania DNA po późniejsze stany, w których część hybrydy RNA–DNA jest już uformowana, lecz pełna gotowość do cięcia jeszcze nie nastąpiła.
Jak zmiany kształtu napędzają dokładne cięcie
Porównanie wariantu ze wcześniej określonymi strukturami normalnego Cas12a ujawniło wyraźny wzorzec. W białku naturalnym fragment helisy mostka przechodzi od luźnej pętli do dłuższej, prostej helisy i wygina się w kierunku rosnącej hybrydy RNA–DNA, wchodząc z nią w bliski kontakt. Równocześnie sąsiednia helisa w domenie tnącej rozluźnia się, a mały obszar zwany „klapką”, który normalnie blokuje miejsce aktywne, zmienia się z pętli w helisę i odchyla się, otwierając drogę. Te skoordynowane ruchy tworzą kieszeń, która pozwala na wejście pojedynczej nici DNA i jej przecięcie. W wariancie zawierającym proliny helisa mostka nie może w pełni przeprowadzić przejścia pętla→helisa ani właściwie się wygiąć. W rezultacie hybryda RNA–DNA pozostaje zdeformowana i odsunięta, klapka utrzymuje zamkniętą, pętlową konformację, a kompleks rzadko osiąga w pełni prekatalityczny stan. To mechaniczne zwężenie spowalnia cięcie na docelowych sekwencjach i utrudnia DNA z niedopasowaniami prześlizgnięcie się przez wewnętrzne kontrole.
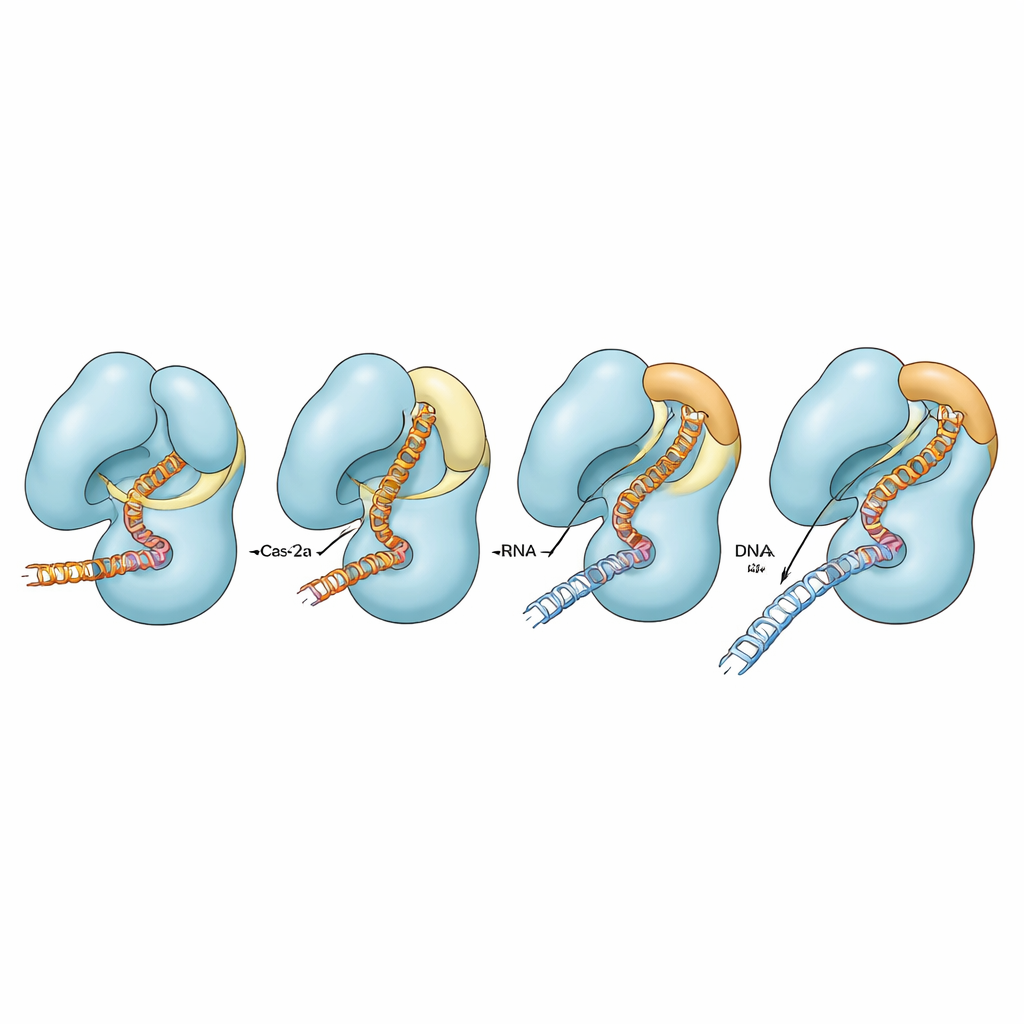
Dostrajanie dokładności przez modyfikację kontaktów
Aby sprawdzić, jak różne oddziaływania wokół klapki i helisy mostka wpływają na aktywność, autorzy zmienili konkretne naładowane reszty wiążące te regiony. W normalnym Cas12a zerwanie tych kontaktów miało tylko umiarkowany wpływ na przecinanie idealnie dopasowanego DNA, chociaż w niektórych warunkach wpłynęło na efektywność przecinania drugiej nici DNA przy obecności niedopasowań. W uszkodzonym tle helisy mostka te same substytucje znacznie osłabiły lub prawie znosiły przecinanie obu nici, szczególnie gdy przewodnik i DNA nie były idealnie dopasowane. Symulacje komputerowe potwierdziły te obserwacje, pokazując, że tylko gdy helisa mostka może w pełni przyjąć helicalną konformację, mostek, sąsiednia helisa, klapka i kwasy nukleinowe poruszają się silnie skoordynowanie. Gdy helisa jest uszkodzona, te ruchy stają się częściowo lub całkowicie odsprzężone, a enzym ma trudności z dokończeniem cyklu katalitycznego.
Przewodnik projektowy dla narzędzi CRISPR następnej generacji
Podsumowując, praca ujawnia helisę mostka jako wewnętrzną dźwignię kontrolną, która łączy długość i jakość hybrydy RNA–DNA z otwarciem kieszeni tnącej w Cas12a. Zmuszając białko do ukończenia określonej sekwencji zmian kształtu zanim nastąpi przecięcie DNA, mechanizm ten naturalnie wymusza rozróżnianie niedopasowań. Wyniki wyjaśniają, dlaczego celowane zmiany w tym niewielkim regionie mogą dawać warianty Cas12a o zmniejszonym cięciu poza miejscem docelowym i osłabionej aktywności „kolateralnej” wobec DNA — cechach pożądanych w bezpieczniejszej edycji genomu i diagnostyce. Szerzej, badanie podkreśla, jak subtelne przesunięcia krótkich helis mogą koordynować komunikację na duże odległości w dużych maszynach molekularnych, dostarczając ogólnych zasad do projektowania enzymów przetwarzających kwasy nukleinowe o wysokiej wierności.
Cytowanie: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Słowa kluczowe: CRISPR-Cas12a, dokładność edycji genów, helisa mostka, formowanie R-pętli, regulacja allosteryczna