Clear Sky Science · pl
RoboA wzmacnia los komórek macierzystych planarii poprzez FoxA i Anosmin1a
Jak robaki odrastają swoje narządy
Niektóre płazińce potrafią odtworzyć niemal każdą brakującą część ciała, od rurki pokarmowej po mózg. Ta niezwykła zdolność zależy od dorosłych komórek macierzystych, które na żądanie mogą przekształcać się w wiele różnych typów komórek. Ale przy takiej swobodzie, jak te komórki unikają budowania niewłaściwych tkanek w złym miejscu — na przykład tworzenia komórek żołądka w głowie zamiast neuronów? Badanie wykorzystuje płazińca planarię, by wyjaśnić, jak niewielki zestaw sygnałów utrzymuje wysoce plastyczne komórki macierzyste na właściwej ścieżce podczas regeneracji.
Regenerujący się robak i jego ukryty potencjał
Planaria Schmidtea mediterranea jest ulubionym modelem do badania regeneracji, ponieważ duża populacja komórek macierzystych jest rozproszona po całym ciele. Jednym z kluczowych narządów jest gardziel (pharynx), mięśniowa rurka pokarmowa położona w środku robaka, łącząca się z zewnętrzem podczas jedzenia. Wcześniejsze prace wykazały, że gen o nazwie foxA jest niezbędny do odbudowy tej gardzieli po urazie, i że tylko określone komórki macierzyste w pobliżu gardzieli normalnie włączają foxA. Nowe badanie stawia pozornie proste pytanie: co powstrzymuje komórki macierzyste w innych regionach — szczególnie w głowie i mózgu — przed wyborem tożsamości gardzieli?
Kiedy prowadzenie zawodzi
Naukowcy skupili się na białku receptorowym o nazwie RoboA, obecnym na niskim poziomie w wielu typach komórek, w tym w komórkach macierzystych. Gdy zmniejszyli aktywność RoboA za pomocą interferencji RNA, zwierzęta często wyrastały dodatkowe, nietypowo umieszczone gardziele po przecięciu. Dokładniejsza obserwacja ujawniła coś subtelniejszego: nawet u nieuszkodzonych robaków obniżenie RoboA powodowało pojawienie się neuronów i mięśni przypominających gardziel wewnątrz regionu mózgowego. Te „ektopijne neurony gardzieli” zachowywały się jak normalne komórki gardzieli pod względem ekspresji genów, ale znajdowały się w niewłaściwym miejscu. Co ważne, ogólny plan ciała i architektura mózgu pozostały w dużej mierze nienaruszone, co sugeruje, że RoboA nie przekształcało całego zwierzęcia, lecz precyzowało, w co przekształcają się pobliskie komórki macierzyste.
Trójczynnikowy przełącznik losu komórkowego
Aby zrozumieć, jak działa RoboA, zespół szukał partnerów poza komórką. Chociaż białka Robo są najbardziej znane z wiązania liganda zwanego Slit, wyłączenie Slit nie odtworzyło fenotypu z błędnie umieszczonymi komórkami gardzieli. Duże badanie RNAi białek sekrecyjnych i błonowych wskazało zamiast tego na Anosmin1a (Anos1a), białko wydzielane spokrewnione z czynnikiem u ludzi zaangażowanym w zespół Kallmanna. Redukcja Anos1a powodowała podobne dodatkowe neurony gardzieli, a wspólne wyciszenie RoboA i Anos1a zachowywało się, jakby działały w tej samej ścieżce. Jednocześnie profilowanie molekularne wykazało, że czynnik transkrypcyjny FoxA znajduje się w centrum tej decyzji: gdy RoboA jest obecne, utrzymuje FoxA wyłączone w komórkach macierzystych głowy; gdy sygnalizacja RoboA jest usunięta, FoxA się włącza i te same komórki macierzyste mogą obrać los neuronu gardzieli nawet siedząc w mózgu.
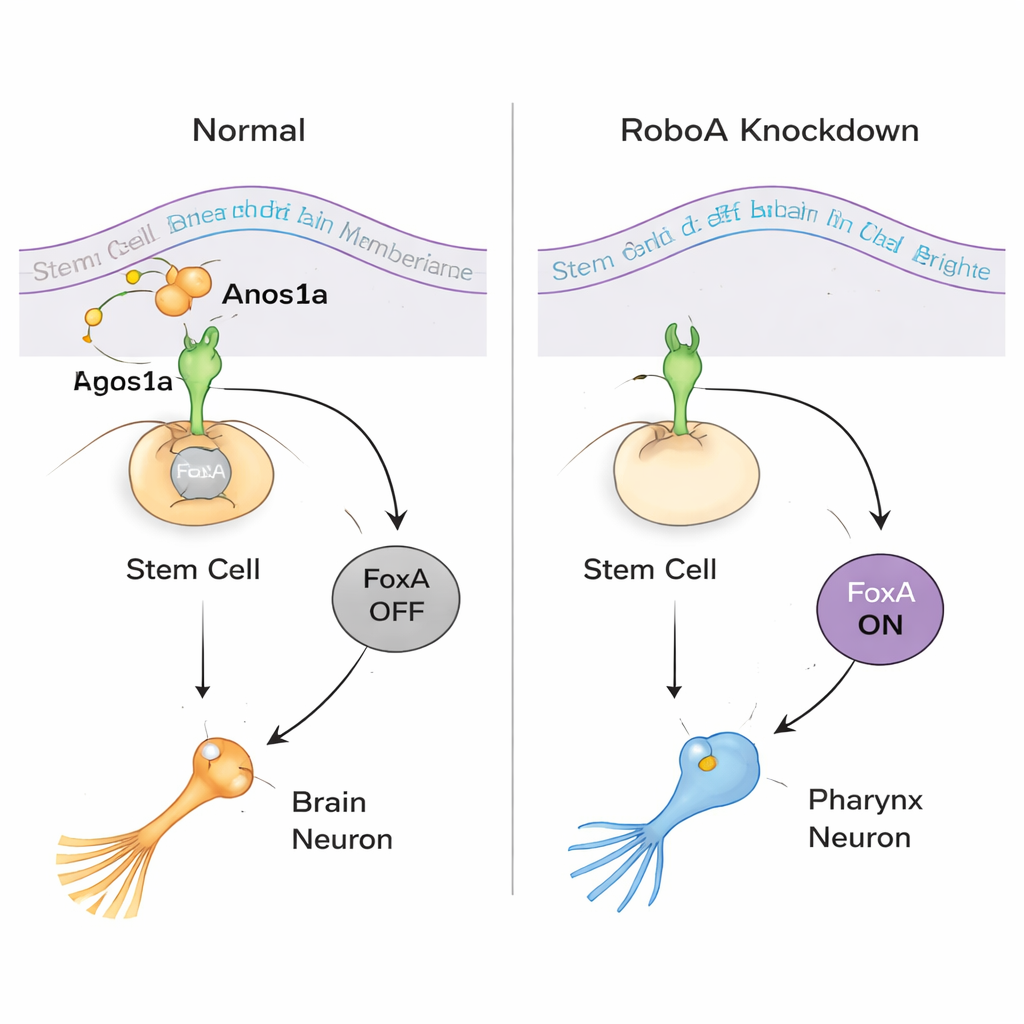
Ujawnienie dwukierunkowego wyboru w komórkach macierzystych
Zespół zapytał następnie, czy ta elastyczność działa w obu kierunkach. U normalnych zwierząt komórki macierzyste wokół gardzieli polegają na FoxA, aby stać się neuronami gardzieli i komórkami nabłonkowymi, podczas gdy mięśnie gardzieli podążają inną drogą. Gdy FoxA był dłużej wyciszany, robaki całkowicie traciły gardziele i rosły nietypowe wyrośla w środku ciała. Sekwencjonowanie RNA pojedynczych komórek i analiza markerów ujawniły, że te wyrośla zawierały wiele typów komórek normalnie ograniczonych do głowy, w tym komórki oka i neurony specyficzne dla mózgu. Innymi słowy, gdy FoxA brakowało tam, gdzie powinna tworzyć się gardziel, lokalne komórki macierzyste domyślnie skłaniały się ku losowi przypominającemu mózg. To odkrycie pokazuje, że te same komórki macierzyste mogą zostać popchnięte ku identyfikacjom „gardziel” lub „mózg” w zależności od odbieranych sygnałów.
Dostrajanie regeneracji, a nie przerysowywanie mapy
Składając wszystkie dowody, autorzy proponują, że regeneracja planarii jest kierowana na dwóch warstwach. Szerokie sygnały „kontroli pozycji”, takie jak Wnt i inne molekuły wzorcujące, ustawiają zgrubną mapę głowy, tułowia i ogona. Na to nakładają się lokalne geny „wzmacniające los”, takie jak RoboA i Anos1a, które działają jako zabezpieczenia, blokując nieodpowiednie opcje. W głowie sygnalizacja RoboA–Anos1a utrzymuje FoxA wyłączone, więc komórki macierzyste wytwarzają neurony mózgowe zamiast komórek gardzieli; w pobliżu gardzieli FoxA może się włączyć i napędzać losy specyficzne dla gardzieli. Ta wielowarstwowa kontrola pozwala komórkom macierzystym planarii pozostać wyjątkowo plastycznymi, jednocześnie odbudowując narządy we właściwym miejscu, co daje schemat pokazujący, jak odporna regeneracja może współistnieć z surowym porządkiem anatomicznym.
Cytowanie: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Słowa kluczowe: regeneracja planarii, plastyczność komórek macierzystych, wzorzec narządów, sygnalizacja RoboA, czynnik transkrypcyjny FoxA