Clear Sky Science · pl
Atypowe pericapilarne makrofagi Ly6G⁺Nur77⁺ inicjują odpowiedzi immunologiczne typu 2 na alergeny w płucach myszy
Dlaczego roztocza kurzu mają znaczenie dla twoich płuc
Dla milionów osób z astmą lub katarem siennym zwykły kurz może wywołać kaszel, świszczący oddech i swędzące oczy — jednak to, jak organizm po raz pierwszy wyczuwa te na pierwszy rzut oka niegroźne cząstki, pozostawało zagadką. To badanie wykorzystuje myszy, by odsłonić wcześniej nieznaną grupę komórek „zwiadowczych” w płucu, które wykrywają alergeny roztoczy kurzu domowego i uruchamiają rodzaj reakcji immunologicznej napędzającej alergie. Zrozumienie tego wczesnego systemu alarmowego może wskazać nowe sposoby zapobiegania lub łagodzenia zapalenia alergicznego, zanim przerodzi się w pełnoobjawową chorobę. 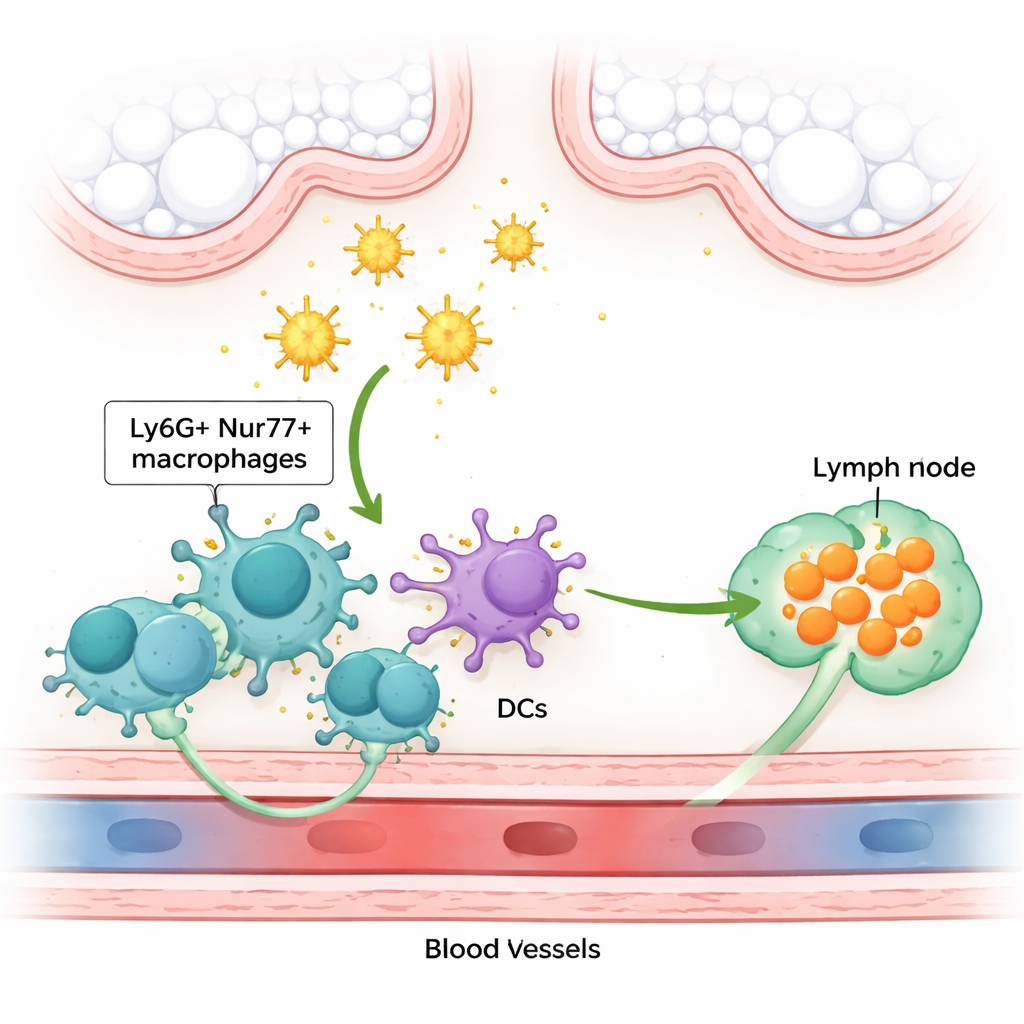
Ukryty system alarmowy w naczyniach krwionośnych płuc
Naukowcy skupili się na ekstrakcie z roztoczy kurzu domowego, jednym z najczęstszych wewnętrznych czynników alergicznych na świecie. Zamiast traktować alergen jako prosty obcy czynnik, zespół zadał inne pytanie: czy układ immunologiczny reaguje na to, co alergen robi tkankom? Wiele białek roztoczy działa jak nożyce, tnąc inne białka. Badacze wykazali, że specyficzna aktywność tnąca — zwana aktywnością cysteinowej proteazy — pochodząca od roztoczy i pokrewnych modelowych alergenów jest absolutnie niezbędna do wywołania klasycznej odpowiedzi typu 2, szlaku związanego z astmą i innymi chorobami alergicznymi. Gdy tę aktywność tnącą zablokowano, myszy nie rozwijały komórek Th2 napędzających alergię ani eozynofilów w płucach, mimo że sam alergen nadal był obecny.
Poznaj perivaskularne „zwiadowcze” makrofagi
W dalszych badaniach zespół odkrył niezwykły zestaw komórek odpornościowych usytuowanych tuż przy drobnych naczyniach krwionośnych płuc. Komórki te przypominają makrofagi — profesjonalnych „pożeraczy” fagocytujących cząstki — ale wykazują niespodziewany marker powierzchniowy (Ly6G) częściej kojarzony z neutrofilami oraz białko jądrowe Nur77 (znane też jako Nr4a1), które pomaga kontrolować aktywność genów. Ze względu na pozycję owiniętą wokół naczyń włosowatych autorzy nazywają je pericapillary Ly6G⁺Nur77⁺ makrofagami. Te „zwiadowcy” szczególnie dobrze wychwytują wdychane alergeny: choć stanowią zaledwie około 1% komórek płuca, odpowiadają za dużą część komórek, które faktycznie internalizują alergeny roztoczy lub papainy. Tworzą też stabilną, samoodnawialną populację zasiedloną we wczesnym okresie życia, odrębną od lepiej znanych makrofagów pęcherzykowych i śródmiąższowych.
Jak wykrywanie alergenu przekłada się na reakcję alergiczną
Pericapillary Ly6G⁺Nur77⁺ makrofagi wykrywają aktywność alergenu za pomocą receptora powierzchniowego PAR2, który zostaje uruchomiony, gdy proteazy go tną. Po aktywacji przez alergeny bogate w proteazy te makrofagi namnażają się w płucu i wysyłają sygnał chemiczny, który kształtuje kolejne etapy odpowiedzi immunologicznej. Same nie przemieszczają się do węzłów chłonnych; zamiast tego kontrolują ruch konwencjonalnych komórek dendrytycznych, które przenoszą fragmenty alergenu do pobliskich węzłów śródpiersiowych, gdzie następuje aktywacja komórek T. Makrofagi osiągają to przez produkcję leukotrienów cysteinowych — lipidowych mediatorów znanych z leczenia astmy — zwłaszcza LTC₄. Molekuły te zwiększają zdolność komórek dendrytycznych, poprzez ich receptor CCR7, do migracji w kierunku sygnału kierunkowego zwanego CCL21 i efektywnego dotarcia do węzła chłonnego. 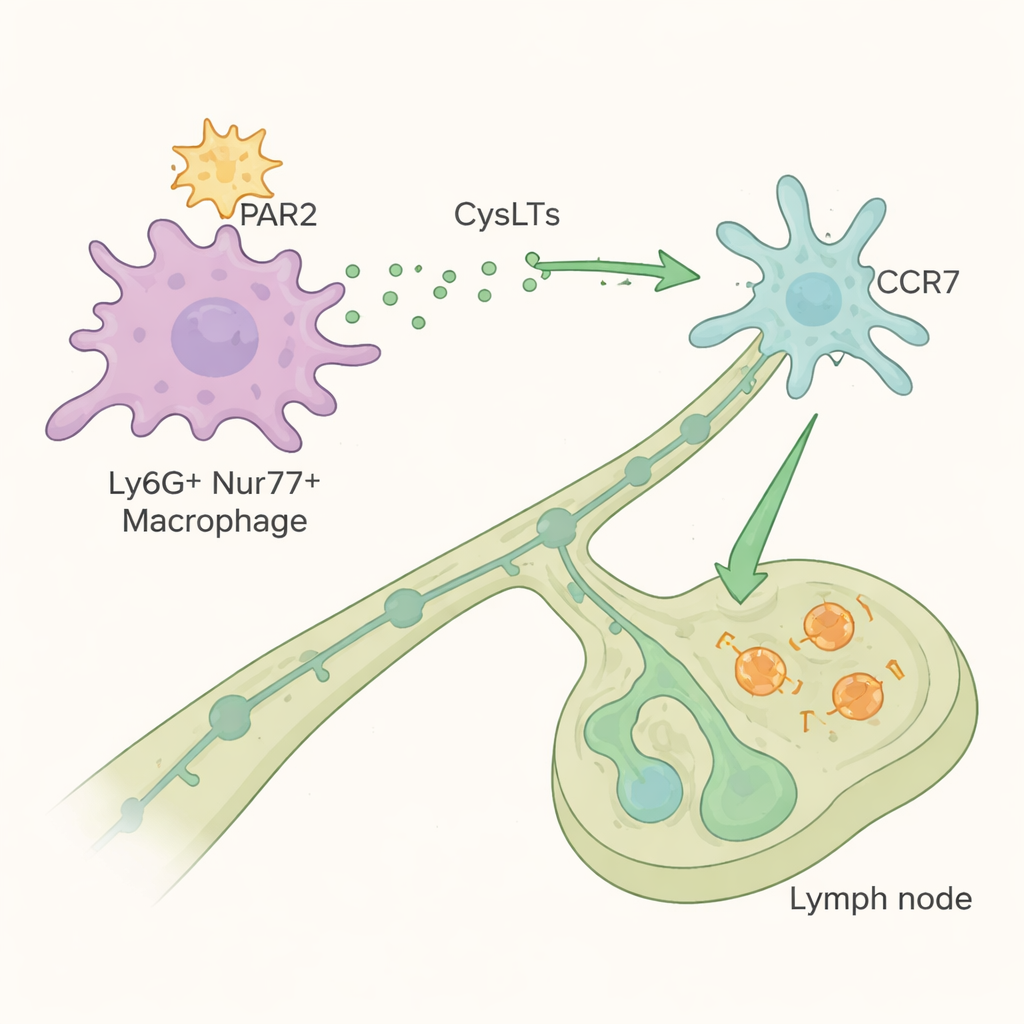
Wyłączanie sygnału bez wyłączania całej odporności
Używając modeli genetycznych i chimeryk szpikowych, autorzy pokazali, że zarówno PAR2, jak i Nur77 są wewnętrznie wymagane w tych atypowych makrofagach, aby mogły się rozszerzać, syntetyzować leukotrieny i napędzać migrację komórek dendrytycznych. Myszy pozbawione funkcjonalnych Ly6G⁺Nur77⁺ makrofagów lub ich enzymów syntezujących leukotrieny wykazywały słaby napływ komórek dendrytycznych do węzłów chłonnych, słabe namnażanie komórek T specyficznych dla alergenu i osłabione zapalenie Th2 w płucu. Co kluczowe, ten szlak wydawał się selektywny dla alergenów bogatych w proteazy: odpowiedzi na infekcję wirusową lub sygnał bakteryjny (LPS) były zachowane, co sugeruje, że jego zablokowanie nie osłabiłoby ogólnej odporności. Gdy badacze farmakologicznie zablokowali enzym syntazy LTC₄ — etap generujący leukotrieny cysteinowe — mogli wyraźnie zmniejszyć migrację komórek dendrytycznych, aktywację komórek T i alergiczne zapalenie płuc, nawet gdy lek podawano tylko podczas uczulenia lub tylko podczas późniejszego kontaktu z alergenem.
Co to oznacza dla osób z alergiami
Mówiąc prościej, praca identyfikuje wyspecjalizowaną grupę makrofagów płucnych usytuowanych przy naczyniach włosowatych, które rozpoznają „nożycową” aktywność alergenów roztoczy przez PAR2, a następnie przywołują inne komórki odpornościowe za pomocą leukotrienów, aby uruchomić odpowiedź alergiczną typu 2. Nakierowując produkcję leukotrienów u źródła, zamiast jedynie blokować pojedynczy receptor leukotrienowy jak robią obecne leki na astmę, możliwe może być precyzyjniejsze stłumienie zapalenia specyficznego dla alergii przy zachowaniu prawidłowych mechanizmów obronnych. Ta perivaskularna oś makrofag–leukotrieny daje nowe pojęciowe wyjaśnienie, dlaczego niektóre białka środowiskowe stają się alergenami, i wskazuje obiecującą ścieżkę dla przyszłych terapii mających na celu zapobieganie lub łagodzenie alergicznej choroby dróg oddechowych.
Cytowanie: Meloun, A., Bachus, H., Lewis, C. et al. Atypical pericapillary Ly6G⁺Nur77⁺ macrophages initiate type-2 immune responses to allergens in the mouse lung. Nat Commun 17, 1946 (2026). https://doi.org/10.1038/s41467-026-68652-5
Słowa kluczowe: astma alergiczna, roztocze kurzu domowego, makrofagi płucne, leukotrieny, odporność typu 2