Clear Sky Science · pl
NeoPrecis: poprawa przewidywania odpowiedzi na immunoterapię poprzez integrację kwalifikowanej immunogenności i uwzględniającego klonalność krajobrazu neoantygenów
Dlaczego niektóre nowotwory odpowiadają na immunoterapię, a inne nie
Immunoterapia zrewolucjonizowała opiekę onkologiczną, jednak wielu pacjentów nadal nie odnosi z niej korzyści, a niektórzy doświadczają poważnych działań niepożądanych. Kluczowym pytaniem jest, dlaczego niektóre guzy zostają dostrzeżone i zniszczone przez układ odpornościowy, podczas gdy inne umykają jego uwadze. W tym badaniu przedstawiono NeoPrecis — metodę obliczeniową, która dokładniej analizuje „znaki” wystawiane przez guzy układowi odpornościowemu — tzw. neoantygeny — i wykorzystuje te informacje do lepszego przewidywania, którzy pacjenci prawdopodobnie odpowiedzą na nowoczesne immunoterapie.
Nowe znaki na komórkach nowotworowych
Komórki nowotworowe gromadzą mutacje DNA, które mogą zmieniać białka, jakie produkują. Małe fragmenty tych zmienionych białek, nazywane neoantygenami, mogą być prezentowane na powierzchni komórki i rozpoznawane jako obce przez komórki T — zabójców układu odpornościowego. Przez lata lekarze i naukowcy opierali się na przybliżonych miarach, takich jak obciążenie mutacyjne guza — całkowita liczba mutacji — aby oszacować prawdopodobieństwo odpowiedzi na inhibitory punktów kontrolnych. To jednak narzędzie tępe: nie każda mutacja tworzy widoczny lub atrakcyjny cel dla komórek T, a guzy mogą stanowić mozaikę wielu różnych podtypów komórek. NeoPrecis został zaprojektowany, by wyjść poza proste liczenie mutacji i zamiast tego oceniać, które z nich są rzeczywiście obiecującymi celami w obrębie całego guza.
Analiza trzech kluczowych składników naraz
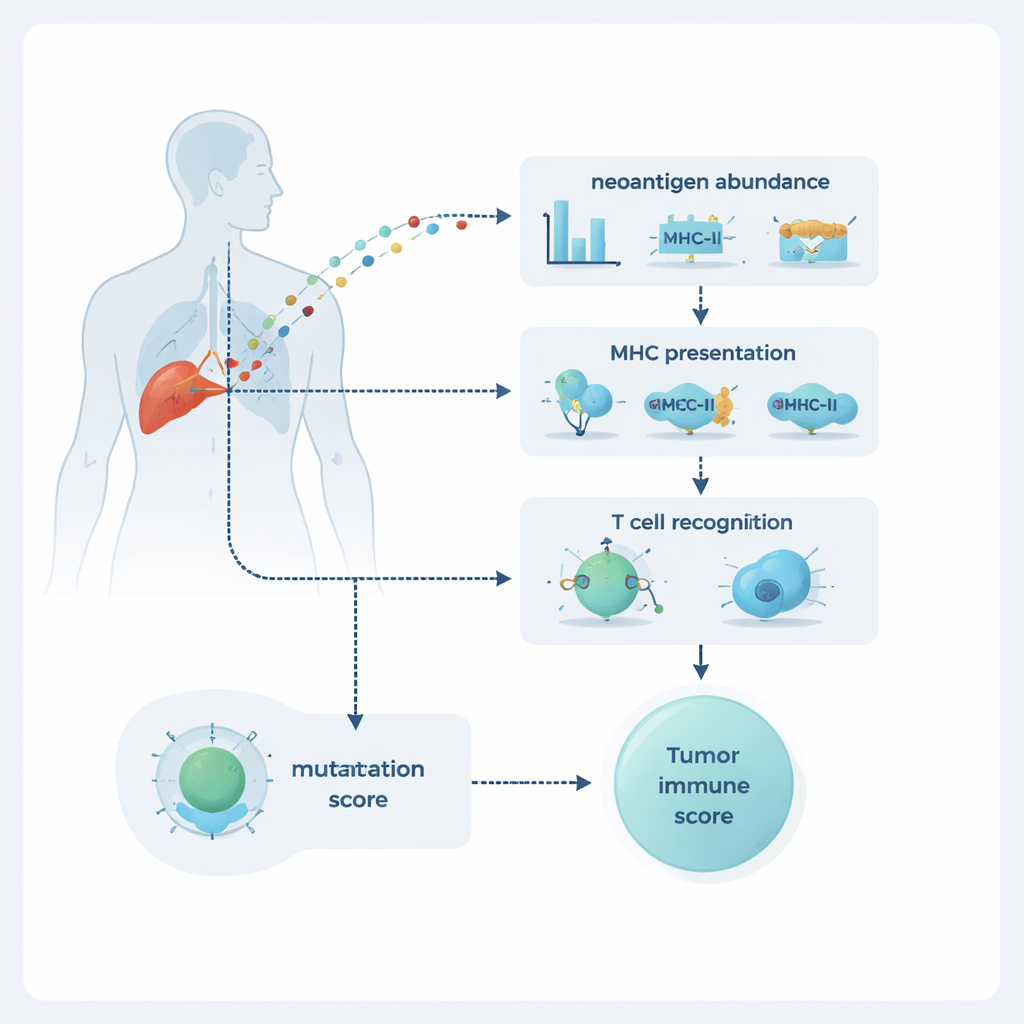
NeoPrecis ocenia każdą mutację w trzech wymiarach: jej obfitość w guzie, prawdopodobieństwo prezentacji na powierzchni komórki oraz szansę na zauważenie przez komórki T. Obfitość szacuje się na podstawie sekwencjonowania DNA i RNA, które ujawnia, jak często występuje mutacja i jak silnie jest ekspresjonowana. Prezentację modeluje się poprzez wiązanie z cząsteczkami MHC klasy I i klasy II, które działają jak tablice reklamowe pokazujące fragmenty białek komórkom T. Najbardziej nowatorskim elementem jest komponent rozpoznawania przez komórki T, NeoPrecis-Immuno. Model ten uczy się na dużych bazach danych znanych interakcji pomiędzy komórkami T a peptydami, aby ocenić, na ile zmieniony fragment różni się od swojej normalnej wersji w sposób istotny dla rozpoznawania przez komórki T, przy jednoczesnym uwzględnieniu konkretnych wariantów MHC, które nosi dana osoba.
Nauka komputera, co „widzą” komórki T
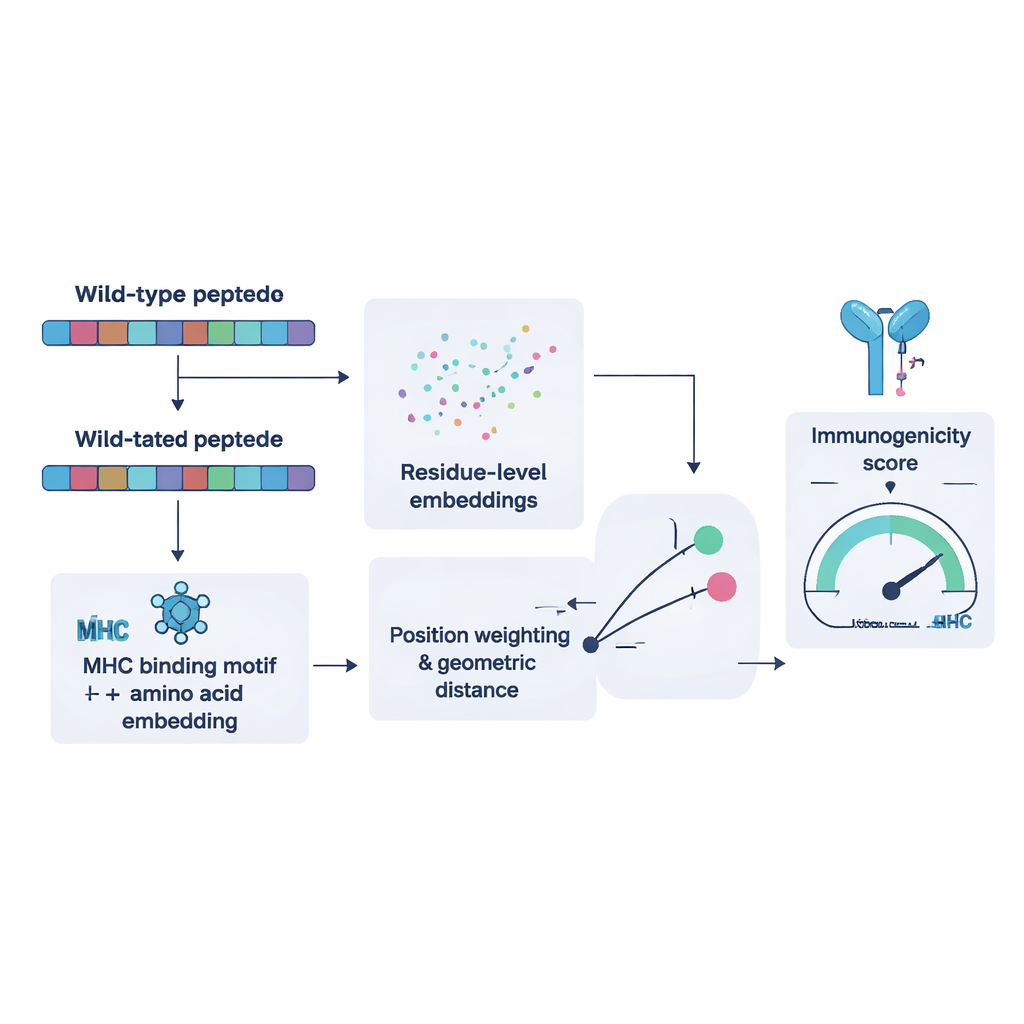
Aby wytrenować NeoPrecis-Immuno, badacze najpierw zgromadzili tysiące przykładów, w których te same komórki T rozpoznają wiele podobnych peptydów oraz przypadków, gdy tego nie czynią. Wykorzystali je, aby nauczyć model, że mutacyjne fragmenty bardzo podobne do normalnych są mniej skłonne wywołać atak immunologiczny, ponieważ takie podobne do self celów zwykle eliminowane są w trakcie dojrzewania komórek T. Model reprezentuje każdy peptyd jako punkt w przestrzeni matematycznej kształtowanej zarówno przez sekwencję aminokwasową, jak i preferencje wiązania specyficzne dla cząsteczek MHC danej osoby. Następnie mierzy, jak daleko mutowany peptyd leży od oryginalnego. Większe odległości informowane motywami odpowiadają wyższemu prawdopodobieństwu immunogenności. W testach na niezależnych zestawach danych z nowotworów NeoPrecis-Immuno dorównywał lub przewyższał istniejące narzędzia, szczególnie w odniesieniu do MHC klasy II, które prezentuje peptydy komórkom T pomocniczym wspierającym i podtrzymującym odpowiedzi przeciwnowotworowe.
Od pojedynczych mutacji do całego guza
Pojedyncze mutacje to tylko część obrazu; istotne jest także, jak są rozłożone w obrębie guza. Niektóre mutacje są klonalne — występują w niemal każdej komórce nowotworowej — podczas gdy inne są subklonalne, obecne tylko w określonych ogniskach. NeoPrecis buduje „krajobraz neoantygenowy”, sumując swoje oceny immunogenności w odniesieniu do mutacji i nakładając informacje o tym, do których podklonów należą oraz jak powszechne są te podklony. Powstają w ten sposób wskaźniki na poziomie guza, które uwypuklają nowotwory bogate w silne, szeroko współdzielone neoantygeny — zwłaszcza te mogące być prezentowane zarówno przez MHC klasy I, jak i klasy II, i potencjalnie wywołujące skoordynowane odpowiedzi komórek T pomocniczych i zabójczych. W grupach pacjentów z czerniakiem i niedrobnokomórkowym rakiem płuca leczonych inhibitorami punktów kontrolnych, wskaźniki oparte na NeoPrecis dokładniej odróżniały responderów od non‑responderów niż standardowe liczniki mutacji i okazały się szczególnie pomocne w skomplikowanych, heterogenicznych guzach płuc.
Co to oznacza dla pacjentów
Dla pacjentów obietnica NeoPrecis to bardziej precyzyjne dopasowanie immunoterapii do tych, którzy mają największe szanse na korzyść, oraz jaśniejsze zrozumienie, dlaczego niektóre guzy opierają się leczeniu. Koncentrując się na jakości i rozmieszczeniu neoantygenów — nie tylko na ich liczbie — ramy te pomagają wyjaśnić, dlaczego guzy o podobnym obciążeniu mutacyjnym mogą zachowywać się bardzo różnie. W przyszłości tak szczegółowe mapy immuno‑widzialnego krajobrazu guza mogą kierować nie tylko stosowaniem inhibitorów punktów kontrolnych, lecz także tworzeniem spersonalizowanych szczepionek przeciwnowotworowych, które priorytetyzują najsilniejsze i najszerzej współdzielone cele w obrębie raka każdej osoby.
Cytowanie: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Słowa kluczowe: immunoterapia nowotworów, neoantygeny, heterogeniczność guza, inhibitory punktów kontrolnych, onkologia obliczeniowa