Clear Sky Science · pl
Stenotrophomonas sprzyja progresji nowotworów przewodu pokarmowego poprzez degradację STING w komórkach nowotworowych i osłabienie odpowiedzi immunologicznej
Ukryte drobnoustroje wewnątrz guzów
Większość ludzi wie, że mikroby w naszych jelitach wpływają na trawienie, a nawet nastrój, ale niewielu zdaje sobie sprawę, że żywe bakterie mogą osiedlać się wewnątrz samych komórek nowotworowych. Badanie to ujawnia, jak powszechna w środowisku bakteria Stenotrophomonas ukrywa się w nowotworach przewodu pokarmowego i potajemnie wspiera ich wzrost, jednocześnie osłabiając obronę immunologiczną organizmu i zmniejszając skuteczność współczesnych immunoterapii przeciwnowotworowych.
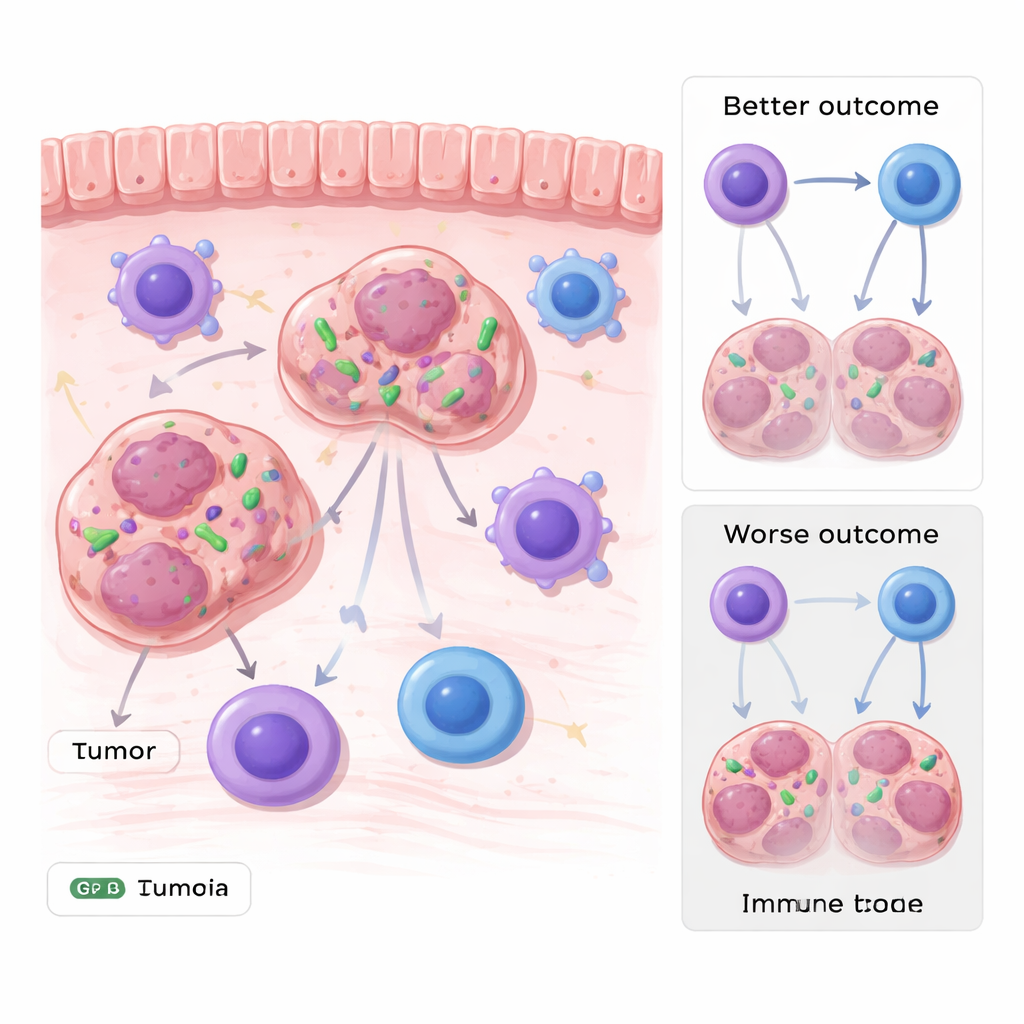
Bakterie żyjące w komórkach nowotworowych
Nowotwory przewodu pokarmowego, takie jak nowotwory żołądka i jelita grubego, rozwijają się w ciągłym kontakcie z bogatymi społecznościami bakteryjnymi przewodu pokarmowego. Analizując wielorakie zbiory danych genetycznych od pacjentów i następnie weryfikując wyniki w próbkach guza, badacze odkryli, że DNA Stenotrophomonas występowało w nadmiernej ilości w kilku typach nowotworów przewodu pokarmowego. Co ważne, jego obecność nie była jedynie zanieczyszczeniem powierzchniowym: metody obrazowania, w tym sondy fluorescencyjne i mikroskopia elektronowa, ukazały całe bakterie znajdujące się w cytoplazmie komórek nowotworowych. Pacjenci, których guzy zawierały więcej tej bakterii, mieli zwykle gorsze rokowania, co łączy mikroba z niekorzystnym przebiegiem choroby.
Jak mikroorganizm przechyla równowagę immunologiczną
Zespół następnie zapytał, czy te ukryte bakterie jedynie towarzyszą agresywnym guzom, czy aktywnie napędzają chorobę. W modelach mysich zakażono komórki nowotworowe fluorescencyjnie znakowaną Stenotrophomonas przed wszczepieniem ich do zwierząt. Guzy zawierające bakterię rosły szybciej i były większe niż te bez niej, w różnych typach komórek nowotworowych. Po zbadaniu otaczającego mikrośrodowiska immunologicznego okazało się, że całkowita liczba komórek odpornościowych, w tym limfocytów T i makrofagów, była podobna. Kluczowa różnica dotyczyła wyspecjalizowanej populacji makrofagów prezentujących cząsteczkę MHC-II, która pomaga im prezentować fragmenty guza komórkom T zabójczym. W guzach zawierających Stenotrophomonas liczba makrofagów MHC-II dodatnich była znacznie zmniejszona, a komórki T wykazywały słabszą aktywność niszczenia komórek nowotworowych.
Przerywanie komórkowego systemu alarmowego
Aby zrozumieć mechanizm, badacze skupili się na kluczowym wewnątrzkomórkowym szlaku alarmowym zwanym STING, który normalnie wykrywa obce DNA i uruchamia uwalnianie przeciwwirusowych sygnałów „niebezpieczeństwa” zwanych interferonami typu I. W eksperymentach laboratoryjnych komórki nowotworowe zakażone Stenotrophomonas produkowały znacznie mniej interferonu beta, a geny zwykle uruchamiane przez ten szlak były przytłumione. Badanie wykazało, że bakteria indukuje stres w fabryce fałdowania białek komórki — retikulum endoplazmatycznym — a następnie wykorzystuje szlak kontroli jakości zwany degradacją związaną z ER (ER-associated degradation). Poprzez pomocnicze białko SEL1L ten szlak oznacza białko STING do zniszczenia w proteasomie komórki. Przy obniżonym poziomie STING komórka nowotworowa wysyła słabszy alarm, co prowadzi do mniejszej produkcji interferonu, a w dalszej kolejności do obniżonej aktywacji makrofagów MHC-II dodatnich.
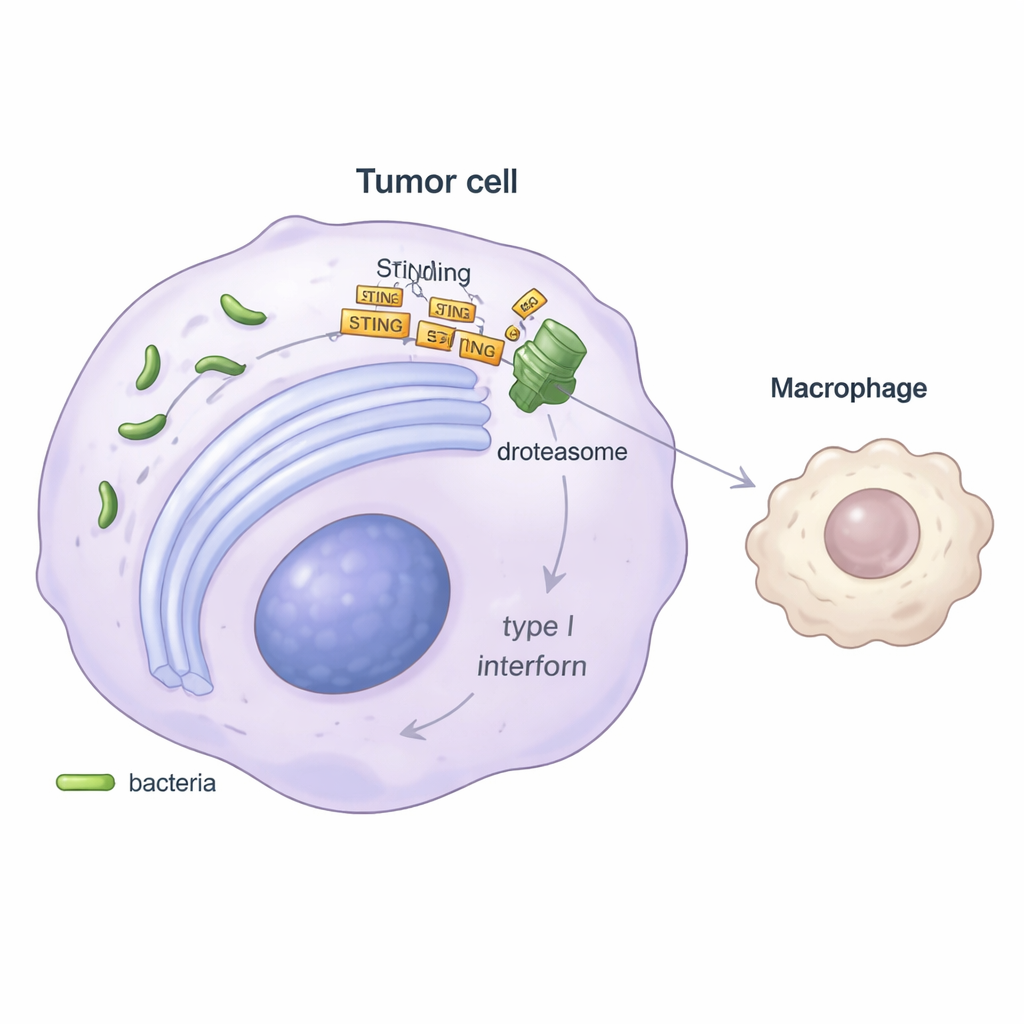
Podważanie immunoterapii — i możliwe rozwiązanie
Ponieważ nowoczesne immunoterapie, takie jak leki anty–PD-1, opierają się na silnej odpowiedzi limfocytów T, zespół przetestował, jak wewnątrzkomórkowa Stenotrophomonas wpływa na leczenie. U myszy guzy zawierające bakterię słabo odpowiadały na terapię anty–PD-1 w porównaniu z guzami wolnymi od bakterii, nawet w połączeniu z chemioterapią. Limfocyty T w tych guzach wykazywały obniżone markery aktywności i podziału, zgodne ze słabą stymulacją immunologiczną. Co istotne, gdy badacze leczyli zwierzęta antybiotykiem lewofloksacyną, która skutecznie zabija Stenotrophomonas, wzrost guza spowolnił, a odpowiedź na terapię anty–PD-1 poprawiła się. Przywrócenie sygnalizacji interferonowej za pomocą klinicznego leku interferonowego mogło także odtworzyć populację pomocnych makrofagów MHC-II dodatnich i przywrócić zabijanie przez komórki T w niektórych warunkach, podkreślając centralną rolę tego szlaku.
Co to oznacza dla pacjentów
Dla czytelnika popularnonaukowego kluczowy przekaz jest taki, że niektóre nowotwory przewodu pokarmowego mogą mieć „własny” wewnętrzny mikrobiom, który pomaga im unikać ataku immunologicznego. Stenotrophomonas, poprzez degradację systemu alarmowego STING w komórkach nowotworowych, osłabia sygnały immunologiczne, które normalnie mobilizowałyby makrofagi i komórki T zabójcze. To nie tylko przyspiesza wzrost guza, ale może także tłumaczyć, dlaczego niektórzy pacjenci nie odnoszą korzyści z silnych immunoterapii. Choć potrzeba więcej badań, zanim odkrycia te wpłyną na praktykę kliniczną, wyniki sugerują możliwość badania obecności takich bakterii w guzach — i selektywnego leczenia ich ukierunkowanymi antybiotykami lub lekami stabilizującymi STING — co mogłoby kiedyś poprawić wyniki u osób z rakiem żołądka i jelita grubego.
Cytowanie: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
Słowa kluczowe: mikrobiom nowotworu, rak przewodu pokarmowego, Stenotrophomonas, szlak STING, immunoterapia raka