Clear Sky Science · pl
NR6A1 jest niezbędny do specyfikacji, formowania i przeżycia komórek grzebienia nerwowego
Jak wczesne decyzje komórkowe kształtują twarz i ciało
Zanim się urodzimy, specjalna grupa komórek zwana komórkami grzebienia nerwowego wędruje przez zarodek, pomagając zbudować twarz, serce, układ nerwowy i inne struktury. Gdy te komórki ulegają zaburzeniom, noworodki mogą mieć poważne wady wrodzone. Badanie to odsłania wcześniej niedoceniany przełącznik molekularny — białko o nazwie NR6A1 — który pomaga zdecydować, kiedy i gdzie komórki grzebienia nerwowego powstają u ssaków, oraz co się dzieje, gdy ten przełącznik zawiedzie.
Błądzący budowniczowie zarodka
Komórki grzebienia nerwowego pojawiają się bardzo wcześnie w rozwoju wzdłuż granicy tworzącego się mózgu i rdzenia kręgowego. Po oddzieleniu się od tego tkanki migrują na duże odległości, tworząc wiele różnych struktur — od kości i chrząstek twarzy po elementy obwodowego układu nerwowego i komórki barwnikowe skóry. Ponieważ biorą udział w powstawaniu wielu narządów, nawet niewielkie zaburzenia ich formowania mogą powodować szeroki zakres zaburzeń znanych jako neurocristopatie, w tym zespoły czaszkowo-twarzowe takie jak zespół Treachera Collinsa. Zrozumienie, jak te komórki po raz pierwszy się pojawiają, jest więc kluczowe dla wyjaśnienia zarówno prawidłowego rozwoju, jak i wad wrodzonych.
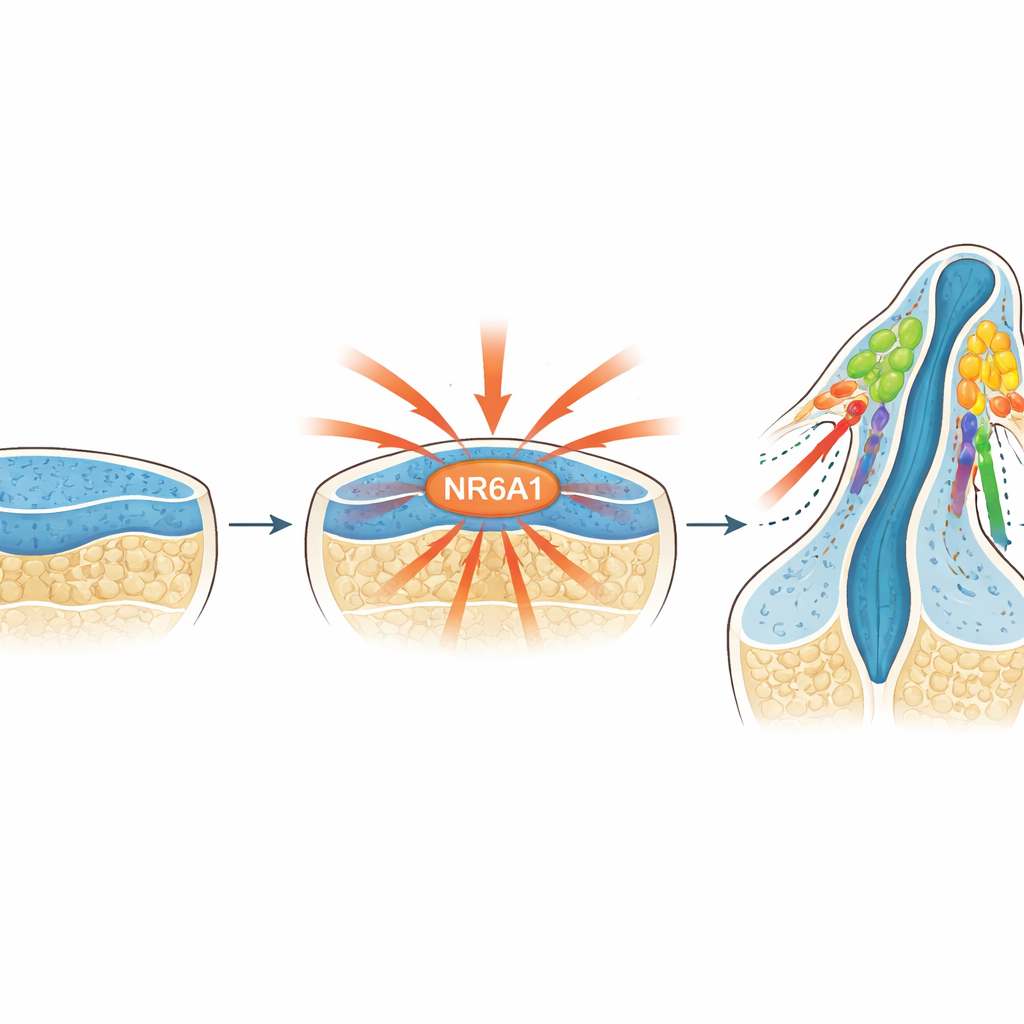
Nowo rozpoznany główny przełącznik
Naukowcy skupili się na NR6A1, członku rodziny receptorów jądrowych kontrolujących aktywność genów. Wcześniejsze badania sugerowały, że NR6A1 może uczestniczyć w wadach głowy i twarzy, lecz jego rola w komórkach grzebienia nerwowego była nieznana. Śledząc NR6A1 u mysich zarodków od momentu tuż po implantacji, zespół odkrył, że jego obecność ściśle odpowiada miejscu i czasowi, w którym zwykle powstają komórki grzebienia nerwowego: pojawia się w wczesnej tkance nerwowej, koncentruje się wzdłuż grzbietowej (tylnej) strony rozwijającego się mózgu i rdzenia kręgowego, a także występuje w komórkach właśnie oddzielających się od tej tkanki, by rozpocząć migrację.
Co się dzieje, gdy przełącznik jest nieobecny
Myszy całkowicie pozbawione NR6A1 ginęły we wczesnym stadium rozwoju, więc zespół przeanalizował zarodki tuż przed tym punktem. Zaobserwowano poważny niedobór komórek grzebienia nerwowego, zwłaszcza za pierwszym łukiem, który utworzy części szczęki i szyi — tam komórki migrujące były niemal całkowicie nieobecne. Kluczowe programy genowe, które normalnie oznaczają tożsamość komórek grzebienia nerwowego i umożliwiają im odłączenie się i poruszanie, były wyraźnie osłabione. Jednocześnie utrzymywała się aktywność genów podtrzymujących stan macierzysty i wysoką proliferację, a wiele komórek przypominających komórki grzebienia nerwowego, które się utworzyły, szybko obumierało. Wyniki te wskazują, że bez NR6A1 komórki nerwowe nie przechodzą prawidłowo w migracyjne komórki grzebienia nerwowego i nie potrafią przetrwać.
Wyłączanie cech macierzystych i włączanie ruchu
Aby zrozumieć, jak NR6A1 sprawuje tę kontrolę, autorzy połączyli kilka zaawansowanych technik molekularnych, w tym sekwencjonowanie RNA pojedynczych komórek, mapowanie dostępności chromatyny oraz ukierunkowane testy wiązania DNA–białko w mysich i ludzkich komórkach grzebienia nerwowego pochodzących z linii macierzystych. Stwierdzili, że NR6A1 fizycznie wiąże się ze specyficznymi motywami DNA w pobliżu genów kierujących dwoma przeciwstawnymi programami: jednym utrzymującym pluripotencję (zdolność do różnicowania się w wiele typów komórek), a drugim napędzającym tożsamość komórek grzebienia nerwowego oraz ich migrację. Gdy NR6A1 jest obecny, chromatyna wokół genów utrzymujących stan macierzysty, takich jak Oct4 i Nanog, staje się mniej dostępna i te geny są wyciszane, podczas gdy obszary przy genach związanych z grzebieniem nerwowym i przejściem epitelialno-mezenchymalnym stają się bardziej otwarte i aktywne. Nadekspresja Oct4 w krytycznym oknie formowania komórek grzebienia nerwowego naśladowała utratę NR6A1, co dodatkowo pokazuje, że cechy macierzyste muszą być wyciszone, aby komórki grzebienia nerwowego mogły się pojawić.
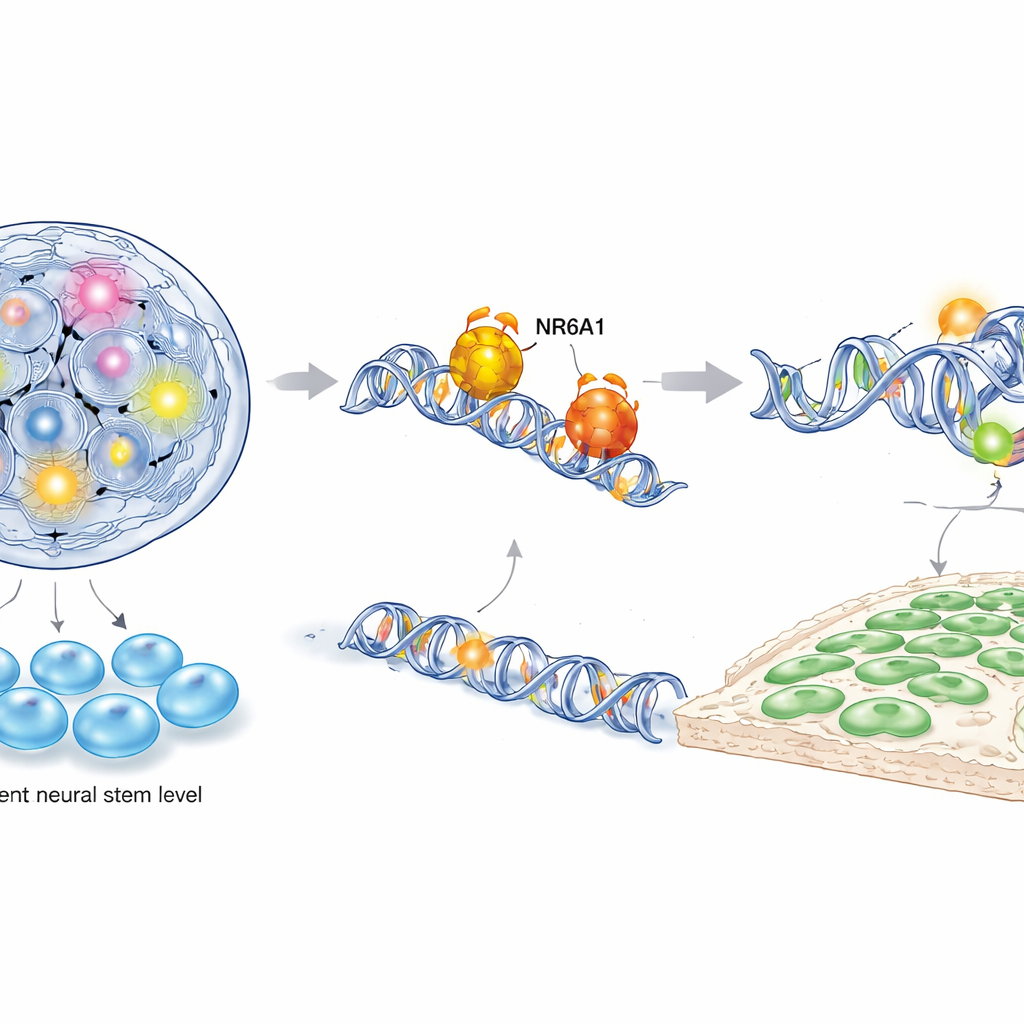
Przepisywanie osi czasowej wczesnego rozwoju
Badanie również koryguje harmonogram momentu, w którym u ssaków zaczyna się specyfikacja komórek grzebienia nerwowego. Używając indukowalnego systemu genetycznego do usuwania NR6A1 w różnych momentach, zespół wykazał, że jego usunięcie do połowy gastrulacji — etapu wcześniejszego niż tradycyjnie sądzono — wystarcza, by zablokować aktywację genów grzebienia nerwowego. Natomiast usunięcie NR6A1 później, włącznie z użyciem powszechnie stosowanej linii aktywującej specyficzne dla grzebienia nerwowego, nie powodowało wyraźnych wad. Oznacza to, że kluczowe decyzje dotyczące losu komórek grzebienia nerwowego zapadają zanim standardowe narzędzia zaczynają działać, co wyjaśnia, dlaczego niektóre wcześniejsze badania na myszach mogły przeoczyć wczesne wymagania.
Dlaczego to ma znaczenie dla wad wrodzonych i chorób
Podsumowując, praca ujawnia NR6A1 jako centralnego koordynatora, który pomaga komórkom nerwowym „dorosnąć” do komórek grzebienia nerwowego poprzez jednoczesne wyłączanie programów pluripotencji i uruchamianie programów migracji oraz przetrwania. To dwojakie działanie wydaje się rozpoczynać w połowie gastrulacji, wcześniej niż dotąd rozpoznawano u ssaków, i zbliża rozwój myszy do tego obserwowanego u innych kręgowców. Wyjaśniając, kiedy i jak działa ten przełącznik, badanie dostarcza ram do reinterpretacji wcześniejszych eksperymentów genetycznych, wskazuje lepsze narzędzia do badania biologii grzebienia nerwowego oraz ostatecznie pomaga zrozumieć i potencjalnie zapobiegać neurocristopatiom powstającym, gdy ta wczesna decyzja rozwojowa idzie nie tak.
Cytowanie: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Słowa kluczowe: komórki grzebienia nerwowego, NR6A1, rozwój embrionalny, przełącznik pluripotencji, neurocristopatia