Clear Sky Science · pl
Inżynieria systemu MmeFz2-ωRNA dla wydajnej edycji genomu poprzez zintegrowane ramy obliczeniowo-eksperymentalne
Mniejsze nożyce genowe na wielkie problemy medyczne
Edycja genów już zmieniła sposób, w jaki naukowcy badają choroby, ale przekształcenie jej w bezpieczną, praktyczną terapię wciąż stanowi poważne wyzwanie. Jedną z głównych przeszkód jest to, że najsilniejsze dzisiaj „nożyce” DNA, takie jak CRISPR-Cas9, są fizycznie duże i trudne do zapakowania w malutkie nośniki stosowane u pacjentów. W tym badaniu wprowadzono nowe, kompaktowe narzędzie do edycji genów zbudowane z mało znanej rodziny enzymów zwanych Fanzor2 i pokazano, jak sztuczna inteligencja może szybko przeprojektować je w silnego kandydata do przyszłych terapii genetycznych.
Nowa klasa kompaktowych edytorów genów
Większość obecnych edytorów genomu, takich jak Cas9 i Cas12a, to masywne białka złożone z ponad tysiąca aminokwasów. Ich rozmiar utrudnia zmieszczenie ich w wektorach opartych na wirusach adeno‑powiązanych (AAV), które są wiodącym systemem dostarczania w terapii genowej. W przeciwieństwie do nich białka Fanzor2 są znacznie mniejsze i naturalnie występują w eukariontach — gałęzi życia obejmującej zwierzęta i ludzi. Autorzy skupili się na jednym członku tej rodziny, MmeFz2, który wykorzystuje krótką cząsteczkę RNA nazwaną ωRNA do odnajdywania i przecinania określonych sekwencji DNA. Na papierze MmeFz2 wyglądał idealnie do terapii: kompaktowy i programowalny. W praktyce jednak jego aktywność w komórkach ludzkich była marna — edytował mniej niż jeden procent miejsc docelowych. Zespół postawił sobie za cel przekształcenie tego słabo działającego enzymu w narzędzie praktyczne.
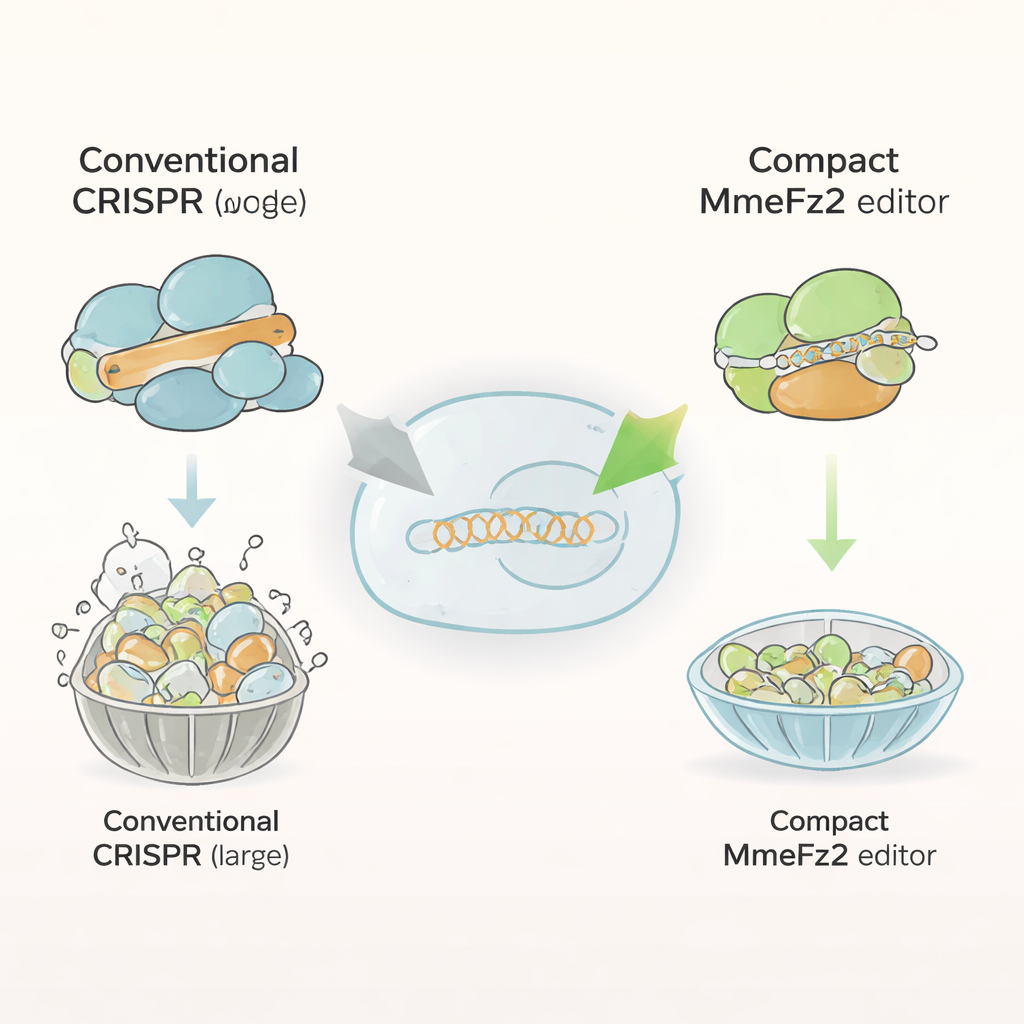
Wykorzystanie AI do przeprojektowania cząsteczki przewodniej
Pierwszym celem była ωRNA — przewodnik wskazujący MmeFz2, gdzie ciąć. Korzystając z AlphaFold3, zaawansowanego programu przewidującego struktury 3D kompleksów białko–RNA–DNA, badacze zbudowali model MmeFz2 związanej z jej ωRNA i celem DNA. Ta wirtualna struktura ujawniła, że fragmenty ωRNA były wiotkie, słabo sparowane i ledwie stykały się z białkiem. Kierując się tymi informacjami, zespół systematycznie zastępował niestabilne wiązania w RNA i usuwał ciągi urydyn, które mogą przeszkadzać w transkrypcji. Następnie przetestowali dziesiątki wariantów w komórkach ludzkich. Składając najlepsze modyfikacje i przycinając niepotrzebny region pętelki, stworzyli skróconą ωRNA mniejszą o 30%, która jednak dostarczyła blisko 20‑krotnego wzrostu efektywności edycji w wielu miejscach DNA.
Dopasowywanie białka za pomocą uczenia maszynowego
Następnie zespół dopracował samo białko. Ponownie użyli AlphaFold3, aby odwzorować miejsca kontaktu MmeFz2 z RNA i DNA oraz zaprojektowali ponad sto pojedynczych zmian aminokwasowych mających na celu wzmocnienie tych kontaktów lub poprawę elastyczności. Po przesiewowym przetestowaniu tych wariantów w komórkach, dane wydajnościowe trafiły do EVOLVEpro — systemu uczenia maszynowego opartego na modelach języka białkowego trenowanych na milionach naturalnych sekwencji. To narzędzie nauczyło się, które cechy zwykle zwiększają aktywność i zasugerowało nowe kombinacje mutacji przewidywane jako jeszcze skuteczniejsze. Poprzez kilka rund tej obliczeniowo‑eksperymentalnej pętli naukowcy otrzymali dwa zoptymalizowane warianty enzymu, które w połączeniu z ulepszoną ωRNA zwiększyły aktywność edycyjną ponad 60‑krotnie w porównaniu z systemem wyjściowym.
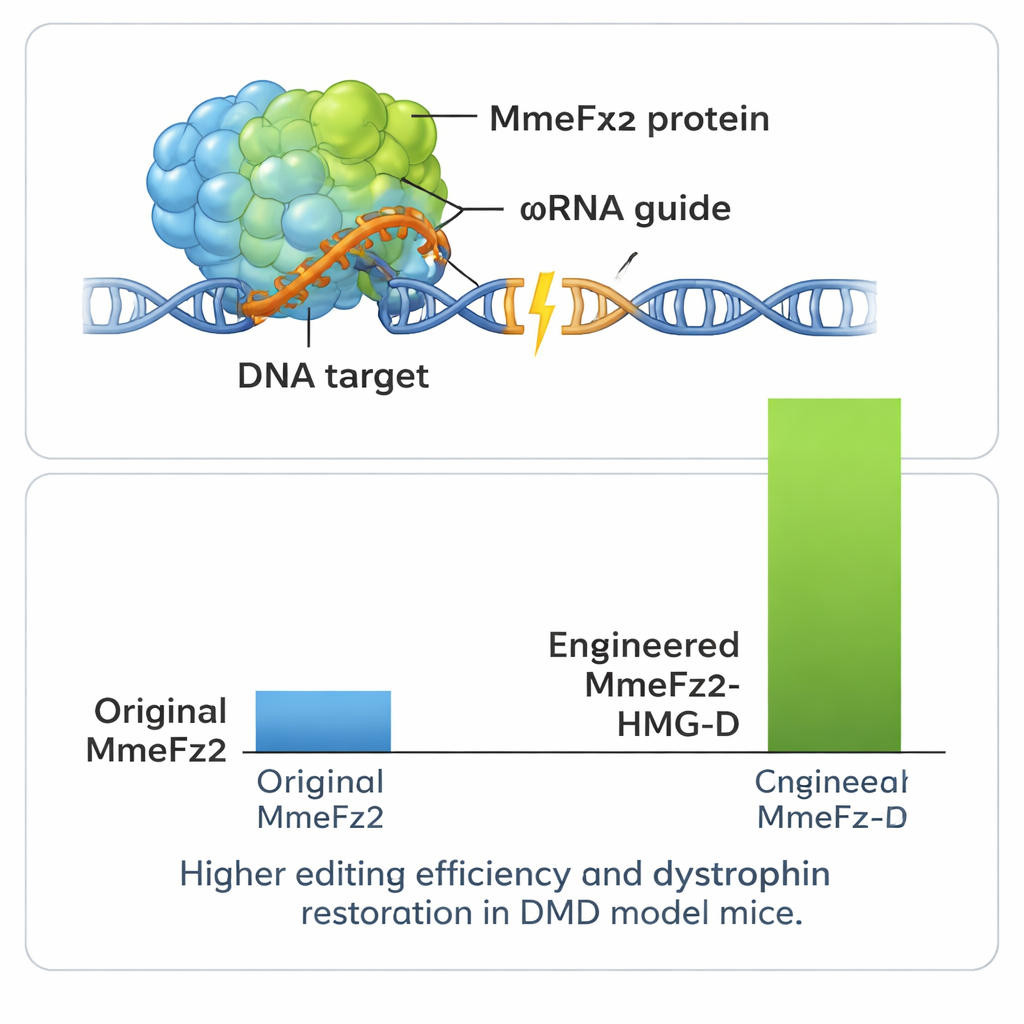
Zwiększanie mocy i testy w modelu choroby
Aby uzyskać jeszcze większą wydajność systemu, autorzy połączyli MmeFz2 z małymi domenami wiążącymi DNA, które pomagają białkom przyczepiać się do materiału genetycznego. Jedna z tych domen, nazwana HMG‑D, okazała się szczególnie skuteczna po przyłączeniu do końca zmodyfikowanego enzymu, dając poziomy edycji powyżej 80% w niektórych miejscach. Co ważne, testy w przewidywanych miejscach poza celem w genomie wykazały, że dodatkowa moc nie wiązała się z istotną utratą precyzji. Ponieważ cały edytor genów — zarówno białko, jak i przewodnik RNA — jest tak kompaktowy, mieści się wygodnie w pojedynczym wektorze AAV, co dla większości systemów CRISPR nie jest możliwe. Zespół wykorzystał tę przewagę w modelu myszy z dystrofią mięśniową Duchenne’a, śmiertelną chorobą prowadzącą do wyniszczenia mięśni spowodowaną błędami w genie dystrofiny. Jednorazowe wstrzyknięcie edytora dostarczonego przez AAV do mięśnia nogi doprowadziło do wykrywalnych korekt w RNA genu i przywrócenia białka dystrofiny w znacznej części włókien mięśniowych.
Co to oznacza dla przyszłych terapii genowych
Dla laików kluczowy przekaz jest taki, że autorzy przemienili słaby, mało znany enzym tnący geny w kompaktowy, wysokowydajny edytor, który można dostarczyć w pojedynczym wirusowym opakowaniu i który potrafi naprawić poważną chorobę genetyczną w realistycznym modelu zwierzęcym. Równie istotne jest to, jak to osiągnęli: poprzez ścisłe połączenie predykcji struktury opartej na AI i uczenia maszynowego z ukierunkowanymi testami laboratoryjnymi, poprawili zarówno białko, jak i jego przewodnik RNA znacznie wydajniej niż tradycyjne podejścia metodą prób i błędów. Ta zintegrowana strategia może przyspieszyć tworzenie wielu kolejnych generacji edytorów genomu, przybliżając precyzyjne i bezpieczniejsze terapie genowe dla pacjentów z dystrofią mięśniową i innymi chorobami dziedzicznymi.
Cytowanie: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Słowa kluczowe: edycja genów, alternatywy dla CRISPR, Dystrofia mięśniowa Duchenne’a, terapia genowa wirusowa, sztuczna inteligencja w biologii