Clear Sky Science · pl
Oszacowanie stabilności fałdowania białek z wyraźnym uwzględnieniem stanów niepofałdowanych
Dlaczego stabilność białek ma znaczenie
Każde białko w twoim organizmie to maleńka maszyneria molekularna, która musi złożyć się w precyzyjny, trójwymiarowy kształt, żeby działać poprawnie. Jeśli to pofałdowanie jest zbyt kruche, białko może działać nieprawidłowo, zlepiać się lub w ogóle nie być wytwarzane — problemy związane z chorobami oraz z niepowodzeniami przy produkcji leków i enzymów opartych na białkach. Pomiar stabilności białka w laboratorium jest powolny i trudny, dlatego naukowcy szukają metod komputerowych, które z samej sekwencji potrafią wiarygodnie przewidzieć, jak łatwo białko się rozwinie.
Nowe spojrzenie na stany złożone i niezłożone
Większość współczesnych algorytmów koncentruje się prawie wyłącznie na złożonym kształcie białka. Często zaczynają od struktury przewidzianej przez sztuczną inteligencję, na przykład z AlphaFold, i traktują tę pojedynczą strukturę jako główny wyznacznik stabilności. Tymczasem stabilność to właściwie różnica energetyczna między dwoma szerokimi zespołami: zwartym stanem pofałdowanym i wieloma luźnymi konformacjami, które tworzą stan niezłożony. Autorzy argumentują, że ignorowanie strony niezłożonej tej równowagi jest kluczową przyczyną, dla której istniejące narzędzia mają trudności z dopasowaniem do eksperymentalnych pomiarów energii fałdowania, znanej jako ΔG.
Nowy model uczący się obu stanów
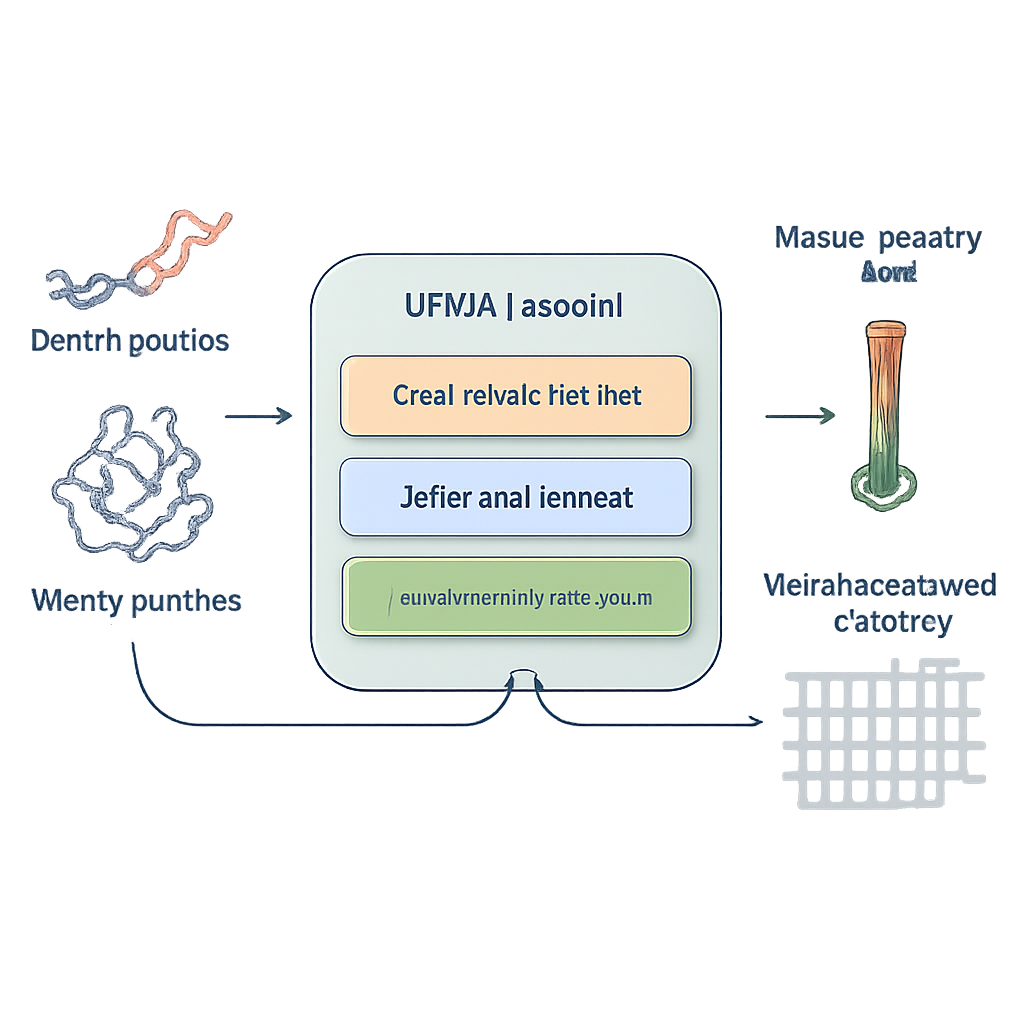
Naukowcy przedstawiają IFUM, system oparty na uczeniu głębokim, zaprojektowany do oszacowania ΔG przy jednoczesnym uczeniu się, jak wygląda równowaga między stanami złożonymi i niezłożonymi dla każdego białka. Zamiast traktować stan niezłożony jako niejasne tło, IFUM korzysta z pomysłów fizyki polimerów, przedstawiając go jako „losową pętlę” i koduje oba stany jako mapy odległości między parami aminokwasów. Model pobiera informacje z potężnych, wstępnie wytrenowanych sieci sekwencji i struktur, a następnie jednocześnie przewiduje całkowitą stabilność oraz mapę prawdopodobieństwa opisującą, jaka część populacji białek jest złożona versus niezłożona dla każdej pary reszt. Trenowanie na bardzo dużym zbiorze małych białek charakteryzowanych eksperymentalnie oraz znanych białek nieuporządkowanych pomaga IFUM rozpoznawać zarówno dobrze uporządkowane, jak i luźne sekwencje.
Lepsze wyniki i szersze pokrycie mutacji
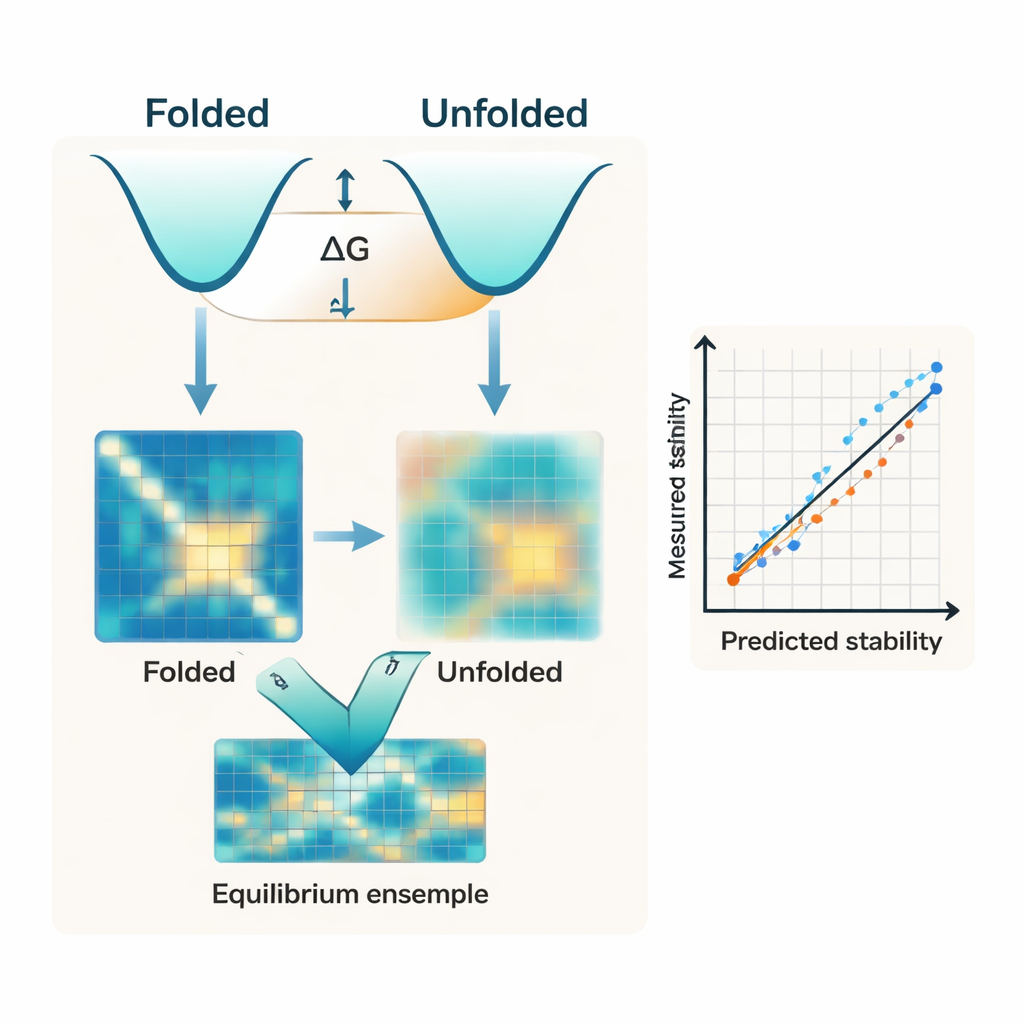
W testach na starannie kontrolowanym zbiorze małych białek IFUM przewiduje eksperymentalne wartości ΔG z mniejszym błędem i wyższą korelacją niż wcześniejsze metody oparte na sztucznej inteligencji, które polegają tylko na złożonej strukturze lub na modelach językowych trenowanych na sekwencjach. Co istotne, model radzi sobie też z szeroką gamą zmian sekwencji. Dokładnie odwzorowuje skutki pojedynczych i podwójnych mutacji punktowych, a także insercji i delecji zmieniających długość białka — sytuacje, w których wiele istniejących narzędzi albo zawodzą, albo nie zostały zaprojektowane do działania. Porównanie wewnętrzne pokazuje, że usunięcie celu dotyczącego stanu niezłożonego znacząco pogarsza wydajność, podkreślając, że jawne modelowanie zespołu stanów niezłożonych to nie tylko koncepcyjna ozdoba, lecz element kluczowy dla dokładności przewidywań.
Od warsztatu projektowego do testów w świecie rzeczywistym
Aby sprawdzić, czy IFUM może wspierać rzeczywiste inżynierię białek, autorzy zastosowali go do trzech wymagających problemów projektowych: stabilizacji białek interferonu‑lambda, przekształcenia białka sygnalizacji immunologicznej IL‑10 oraz ulepszenia enzymu modyfikującego cukry o nazwie UGT76G1. We wszystkich trzech przypadkach przewidywane przez IFUM stabilności dobrze korelowały z mierzoną temperaturą topnienia, która informuje, jak dużo ciepła białko wytrzymuje zanim się rozwinie. Model pomaga też przesiewać setki zupełnie nowych, komputerowo zaprojektowanych białek, wybierając te najprawdopodobniej składające się i pozostające rozpuszczalne w komórkach, przewyższając powszechnie używane wskaźniki zaufania z sieci przewidujących strukturę. Wyniki sugerują, że IFUM może służyć jako praktyczny „filtr stabilności” obok kontroli opartych na strukturze w nowoczesnych przepływach pracy projektowania białek.
Ograniczenia i kierunki rozwoju
Jak każdy model, IFUM ma granice. Jest trenowany głównie na krótkich, jednoniciowych, rozpuszczalnych białkach, a jego bezwzględne wartości stabilności stają się mniej wiarygodne dla znacznie większych białek lub tych z rozległymi, elastycznymi pętlami czy regionami błonowymi. Opis stanu niezłożonego pozostaje uproszczonym modelem statystycznym, a nie w pełni realistycznym obrazem wszystkich możliwych kształtów. Niemniej podejście pokazuje, że uczenie AI uwzględniania zarówno zespołów złożonych, jak i niezłożonych daje bardziej wiarygodne szacunki stabilności. Dla osób niebędących ekspertami kluczowy wniosek jest taki, że IFUM przybliża nas do możliwości zapytania komputera z ilościową pewnością: "Czy ten projekt białka faktycznie się utrzyma?", co może przyspieszyć rozwój bezpieczniejszych leków biologicznych i bardziej wytrzymałych enzymów przemysłowych.
Cytowanie: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
Słowa kluczowe: stabilność białek, fałdowanie białek, uczenie głębokie, projektowanie białek, mutacje