Clear Sky Science · pl
Kamuflowane nanoroboty celują i regulują wzorce komunikacji między organellami makrofagów, by wspierać regenerację nerwów
Dlaczego małe „ukryte” pomocniki są ważne przy urazach rdzenia kręgowego
Uraz rdzenia kręgowego często oznacza dożywotnie porażenie, ponieważ uszkodzona tkanka nerwowa jest niezwykle trudna do naprawy. Główną przyczyną jest to, że miejsce urazu staje się wrogą strefą wypełnioną stanem zapalnym i stresem komórkowym, które blokują gojenie. W pracy opisano nowy rodzaj kamuflowanego nanorobota, który podróżuje krwią, omija obronne mechanizmy organizmu i przeprogramowuje komórki odpornościowe w miejscu urazu — przełączając je z trybu ataku w tryb naprawczy — co sprzyja odrastaniu nerwów u zwierząt z uszkodzeniem rdzenia.
Problem: zapalenie, które nie chce zgasnąć
Po urazie rdzenia kręgowego pierwsza fala uszkodzeń wynika z samej traumy fizycznej. Jednak druga, wolniejsza fala jest napędzana przez stan zapalny, toksyczne cząsteczki zwane reaktywnymi formami tlenu oraz rozległą śmierć komórek. Komórki odpornościowe zwane makrofagami napływają, by posprzątać szczątki. Na początku przyjmują agresywny stan „M1”, który zabija patogeny i uszkodzone komórki, ale też uwalnia silne sygnały zapalne. Aby rozpoczęło się prawdziwe gojenie, te same komórki muszą później przejść w uspokajający stan „M2”, wspierający naprawę tkanek, wzrost naczyń krwionośnych i regenerację nerwów. Niestety intensywny stres w uszkodzonej tkance może uwięzić makrofagi w szkodliwym stanie M1, zamykając cykl przewlekłego zapalenia i uniemożliwiając odzyskanie funkcji.
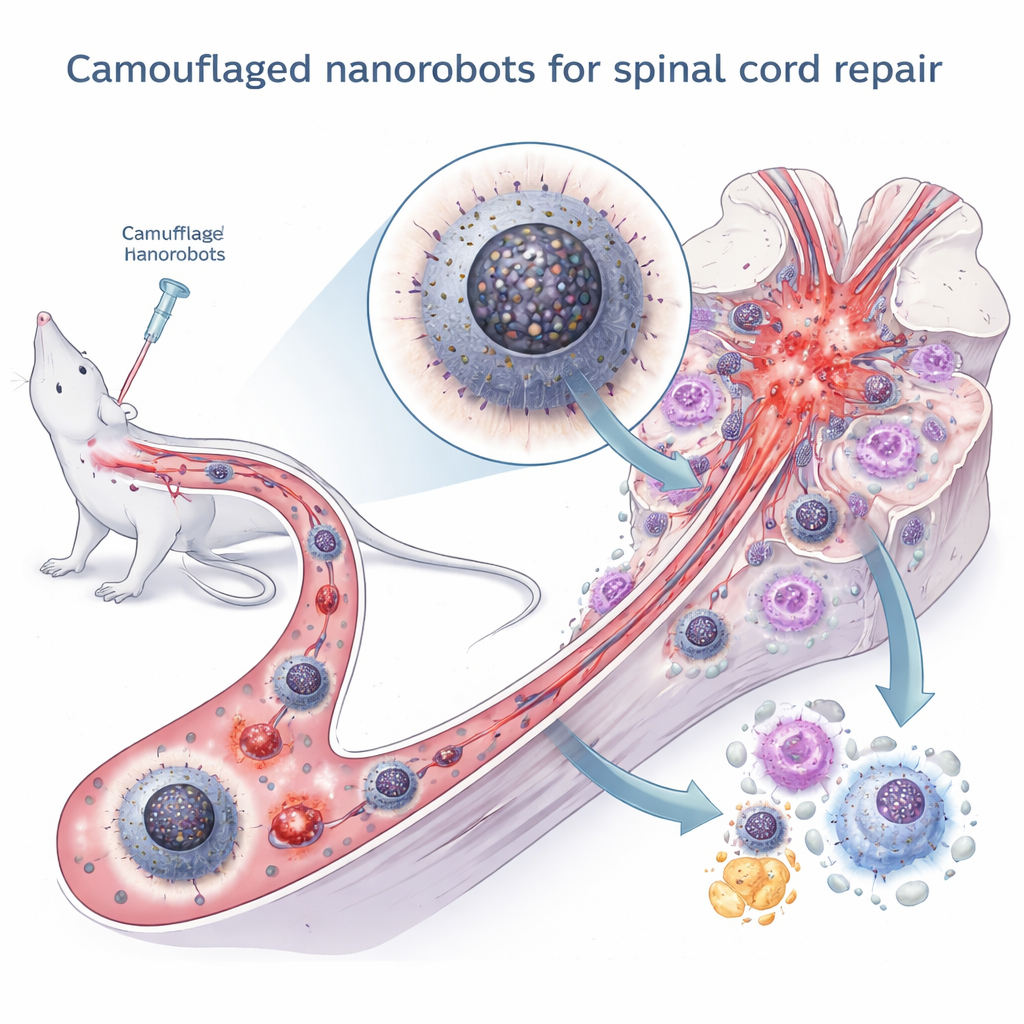
Ukryta rozmowa między częściami komórkowymi
Autorzy skupili się na subtelnej, ale kluczowej „rozmowie” wewnątrz makrofagów: interakcji między dwoma istotnymi przedziałami — retikulum endoplazmatycznym (które pomaga fałdować białka i magazynuje wapń) a mitochondriami (elektrowniami komórki). W normalnych warunkach struktury te wymieniają niewielkie ilości jonów wapnia przez wyspecjalizowane strefy kontaktu, co pomaga dopasować produkcję energii do potrzeb komórki. Po urazie jednak nadmiar reaktywnych form tlenu powoduje nieprawidłowe fałdowanie białek i stres w retikulum endoplazmatycznym. Ten stres napędza nadmierny transfer wapnia do mitochondriów, prowadząc do załamania energetycznego, powstawania kolejnych toksycznych cząsteczek oraz wydostawania się mitochondrialnego DNA do cytoplazmy. Uwolnione DNA uruchamia silną ścieżkę alarmową zwaną cGAS–STING–NFκB, która dodatkowo utrwala makrofagi w zapalnym stanie M1.
Projektowanie kamuflowanego nanorobota
Aby przerwać ten błędne koło, zespół zbudował wielowarstwowego nanorobota nazwanego BP@D/N. W jego rdzeniu znajdują się kropki kwantowe z czarnego fosforu — maleńkie cząstki o silnym działaniu antyoksydacyjnym i przeciwzapalnym, ale słabej stabilności w organizmie. Kropki te umieszczono w pustej skorupie z polidopaminy, biokompatybilnego materiału, który chroni je przed przedwczesnym rozpadem i dodaje własnych właściwości antyoksydacyjnych. Na koniec całą cząstkę owinięto błoną pobraną z aktywowanych neutrofili, typu białych krwinek naturalnie przyciąganych do miejsc zapalenia. Ten „płaszcz” pozwala nanorobotowi unikać usuwania przez układ odpornościowy, podążać za sygnałami zapalnymi do uszkodzonego rdzenia i przylegać do makrofagów, co ułatwia jego pobranie przez te komórki.
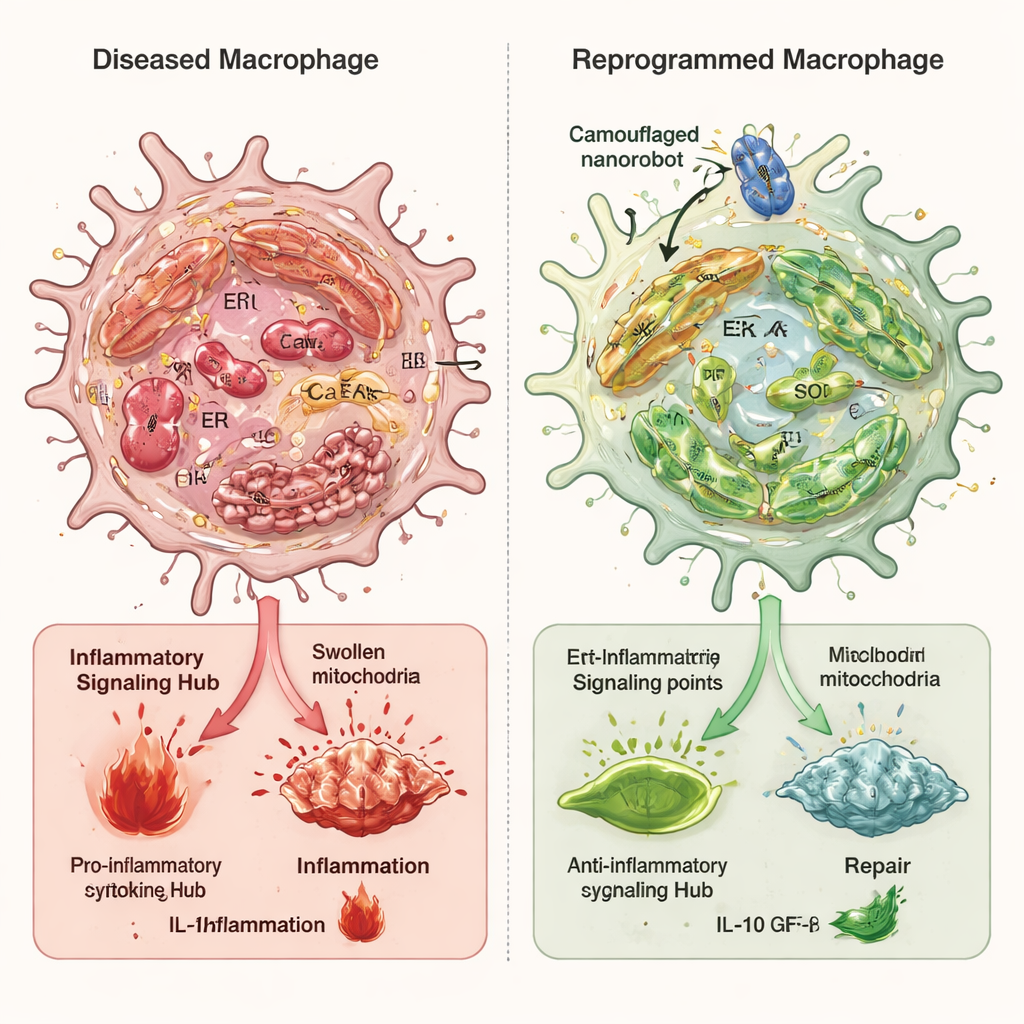
Przeprogramowywanie zestresowanych komórek odpornościowych
W badaniach na komórkach makrofagi wystawione na czynniki zapalne wykazywały wysoki poziom stresu retikulum endoplazmatycznego, obrzęknięte i uszkodzone mitochondria, przeciążenie wapniem oraz silną aktywację ścieżki alarmowej cGAS–STING–NFκB. Po leczeniu kamuflowanymi nanorobotami ogólny stres oksydacyjny spadł gwałtownie, wewnętrzne połączenia między retikulum a mitochondriami stały się mniej nadmierne, a poziom wapnia w mitochondriach wrócił w kierunku normy. To zapobiegło wyciekom mitochondrialnego DNA do cytoplazmy i osłabiło kaskadę sygnałów zapalnych. Kluczową rolę w tym procesie odgrywał enzym Ero1α, który pomaga kontrolować środowisko oksydacyjne i uwalnianie wapnia z retikulum endoplazmatycznego. Nanoroboty zmniejszyły aktywność Ero1α, a gdy badacze sztucznie zwiększyli poziom Ero1α, korzyści wynikające z działania nanorobotów zostały w dużej mierze zniwelowane, co potwierdza jego centralną rolę.
Od łagodzenia zapalenia do odrastania nerwów
Te wewnętrzne zmiany przełączyły makrofagi ze szkodliwego stanu M1 w leczniczy stan M2. W hodowlach komórkowych komórki przesunięte w stronę M2 wydzielały mniej prozapalnych cząsteczek, takich jak TNF-α i IL-6, oraz więcej czynników wzrostu, które zachęcają neurony i komórki wspierające do wzrostu i wydłużania aksonów. W modelach szczurzych urazu rdzenia wielokrotne podawanie nanorobotów prowadziło do mniejszej liczby szkodliwych sygnałów odpornościowych w obrębie rany, mniejszego bliznowacenia, mniejszego tworzenia się jam oraz większej liczby regenerujących się włókien nerwowych. Zwierzęta otrzymujące kamuflowane nanoroboty odzyskiwały lepszą ruchomość tylnych kończyn, silniejsze odpowiedzi mięśniowe i poprawioną strukturę pęcherza w porównaniu z nieleczonymi lub mniej celowanymi terapiami nanopartykuł.
Co to może znaczyć dla przyszłych pacjentów
Praca ta pokazuje, że precyzyjne dostrojenie wewnętrznego stresu i komunikacji między przedziałami komórkowymi może przełączyć komórki odpornościowe z wyrządzających szkody na wspierające odbudowę nerwów. Poprzez zapakowanie silnych, lecz kruchych cząstek antyoksydacyjnych w kamuflowanego, celowanego nanorobota, badacze przywrócili zdrowszą równowagę między zapaleniem a naprawą w uszkodzonym rdzeniu kręgowym szczurów. Chociaż przed zastosowaniem u ludzi potrzeba jeszcze wielu badań, podejście to daje obiecujący plan działania: zamiast szeroko tłumić zapalenie, przyszłe terapie mogłyby sterować specyficznymi mechanizmami wewnątrz makrofagów, tworząc bardziej sprzyjające środowisko dla regeneracji nerwów po urazie rdzenia kręgowego.
Cytowanie: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Słowa kluczowe: uraz rdzenia kręgowego, nanoroboty, makrofagi, regeneracja nerwów, nanomedycyna