Clear Sky Science · pl
Charakterystyka metaboliczna interakcji nowotwór–układ odpornościowy za pomocą multipleksowej immunofluorescencji ujawnia przestrzenne mechanizmy odpowiedzi na immunoterapię w niedrobnokomórkowym raku płuca (NSCLC)
Dlaczego to badanie ma znaczenie
Immunoterapia zrewolucjonizowała leczenie u niektórych osób z zaawansowanym rakiem płuca, jednak większość pacjentów nadal doświadcza progresji choroby pomimo tych silnych leków. To badanie stawia proste, ale kluczowe pytanie: czy przyjrzenie się bliżej samym tkankom nowotworowym — temu, gdzie znajdują się różne komórki i ile energii zużywają — pozwoli przewidzieć, kto rzeczywiście skorzysta na immunoterapii? Przekształcając niewielkie próbki biopsji w szczegółowe mapy komórkowe, badacze dążą do przybliżenia opieki nad rakiem płuca do prawdziwie spersonalizowanego podejścia.
Patrzenie wewnątrz guzów płuca jak na mapę miasta
Zespół przeanalizował tkanki od 55 osób z zaawansowanym niedrobnokomórkowym rakiem płuca (NSCLC), które były leczone inhibitorami punktów kontrolnych układu odpornościowego, ważną klasą leków immunoterapeutycznych. Przed leczeniem próbki guza zabarwiono panelem 44 markerów za pomocą multipleksowej immunofluorescencji, co pozwoliło jednocześnie zobaczyć wiele białek. System oparty na głębokim uczeniu rozpoznał następnie kluczowe typy komórek — takie jak komórki nowotworowe, limfocyty T, limfocyty B, makrofagi i fibroblasty — i zaklasyfikował ich stan funkcjonalny (np. aktywowane, dzielące się, wyczerpane) oraz profil metaboliczny, czyli sposób pozyskiwania i wykorzystywania energii. Zamiast jedynie liczyć komórki, badacze zmapowali także wzajemne pozycje komórek, tworząc w obrębie każdej biopsji regiony przypominające sąsiedztwa.
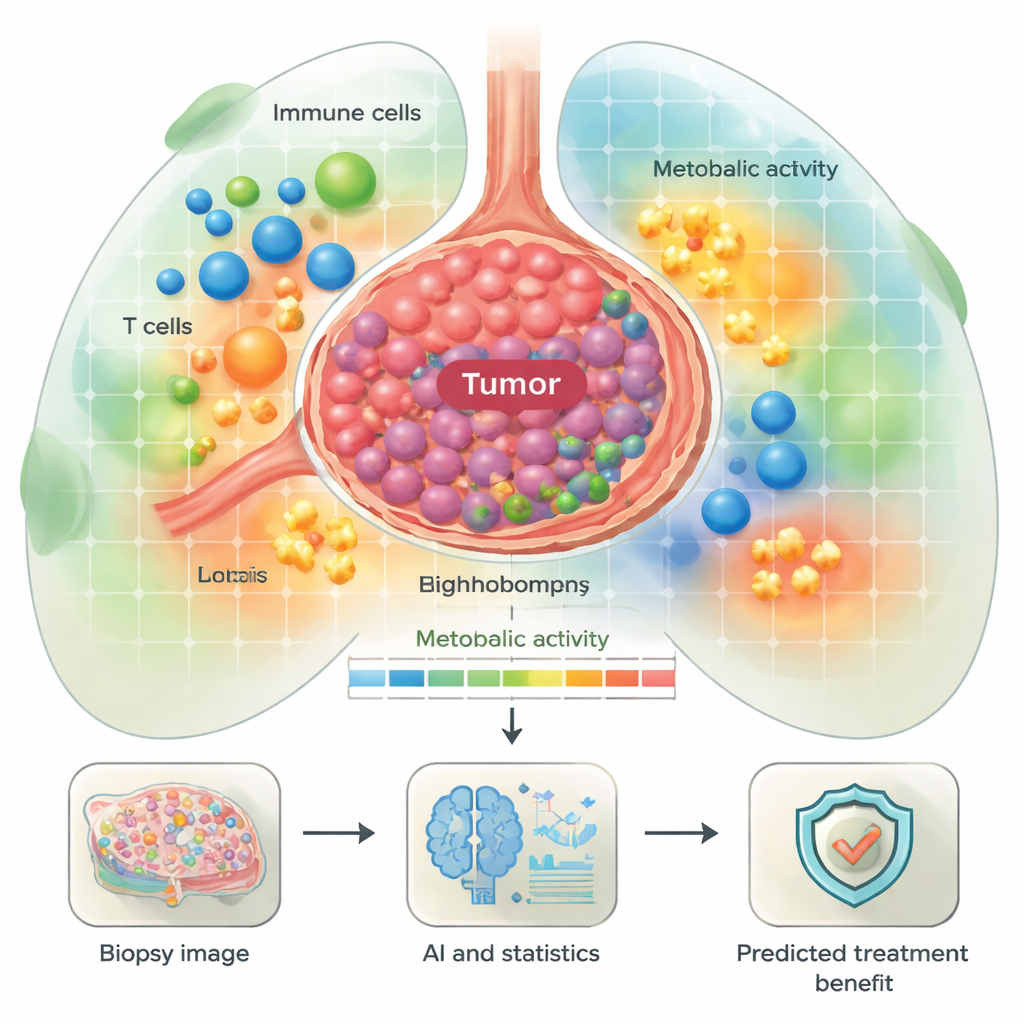
Energożerne guzy i ich immunologiczne otoczenie
Jednym z głównych obszarów zainteresowania był metabolizm — sposoby, w jakie komórki wytwarzają paliwo do wzrostu lub walki z chorobą. Badacze zdefiniowali „metaboliczne sąsiedztwa” o różnym natężeniu i typie aktywności energetycznej, od stref o niskiej aktywności po wysoce aktywne rejony bogate w fosforylację oksydacyjną i glikolizę. Stwierdzili, że zarówno komórki nowotworowe, jak i pewne komórki odpornościowe, np. makrofagi, często wykazywały silne szlaki wytwarzania energii. Niektóre z tych wzorców korelowały z wynikami u pacjentów. Na przykład guzy z wysoką aktywnością szlaków umożliwiających wykorzystanie aminokwasów i funkcjonowanie cyklu TCA częściej występowały u pacjentów, którzy szybko doświadczyli nawrotu po immunoterapii. Natomiast pewne komórki plazmatyczne (produkujące przeciwciała) o aktywnych ścieżkach energetycznych wewnątrz guza były częstsze u pacjentów, którzy mieli lepsze wyniki, co sugeruje, że nie wszystkie energetyczne komórki są szkodliwe — niektóre mogą wspierać efektywną odpowiedź przeciwnowotworową.
Dobrzy i źli gracze odpornościowi w krajobrazie guza
Ponad samą obfitością, istotny był także typ i zachowanie komórek odpornościowych. Makrofagi niosące cytotoksyczną cząsteczkę granzyme B były silnie powiązane z gorszym przeżyciem bez progresji, szczególnie gdy występowały w metabolicznie słabych lub nieaktywnych sąsiedztwach. Te obszary mogą odpowiadać rejonom ubogim w składniki odżywcze lub uśpionym, gdzie atak immunologiczny jest osłabiony. W przeciwieństwie do tego, pewne konfiguracje komórek regulatorowych T (Treg) i fibroblastów na granicy między guzem a tkanką otaczającą wydawały się wiązać z lepszymi wynikami, co może odzwierciedlać sytuację, w której komórki supresyjne pozostają u krawędzi, zamiast przenikać głęboko do guza. Stosunki różnych komórek odpornościowych, takie jak stosunek granulocytów do limfocytów CD8, również korelowały z odpowiedzią, podkreślając, że ważna jest równowaga i rozmieszczenie odporności, a nie tylko całkowite liczby.
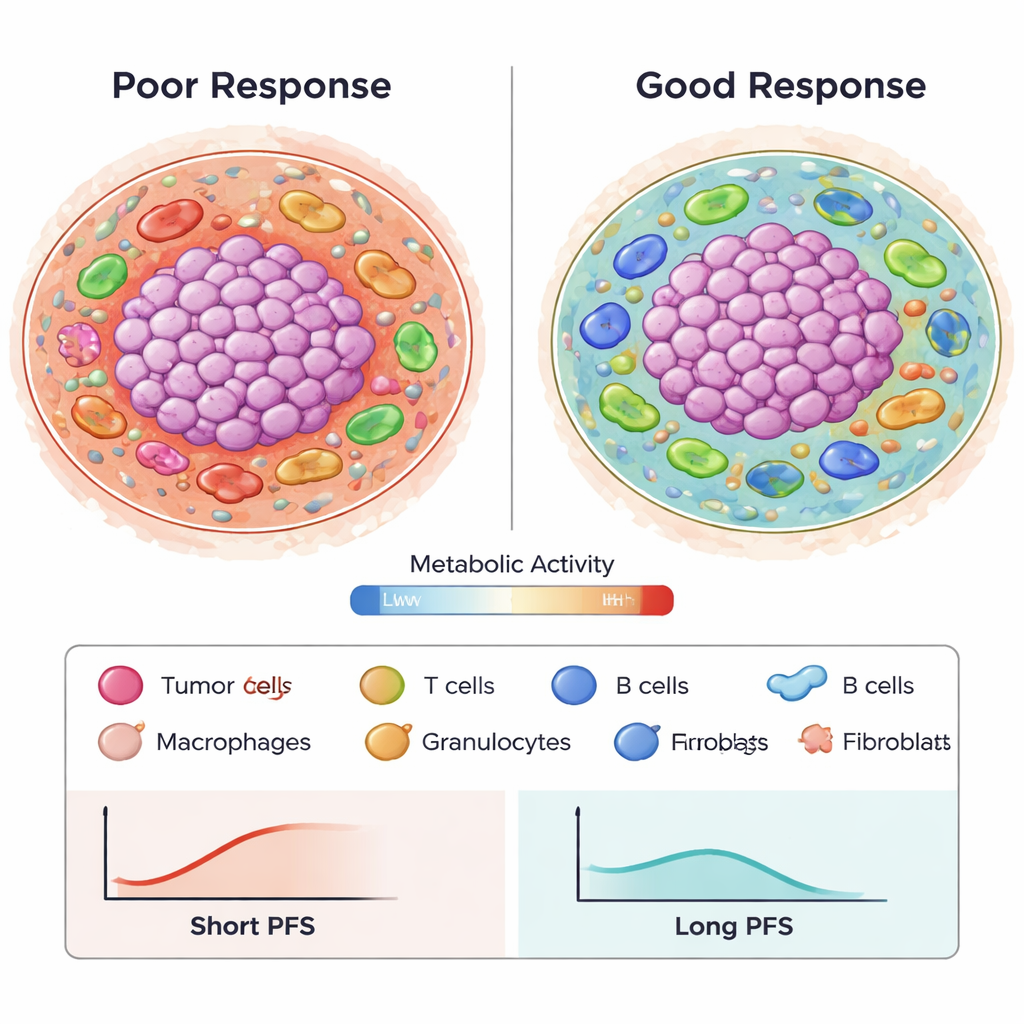
Od złożonych obrazów do wzorców predykcyjnych
Aby zrozumieć ponad milion wyodrębnionych cech przestrzennych opisujących typy komórek, odległości i stany metaboliczne, autorzy zastosowali zaawansowaną metodę selekcji cech (Stabl) oraz narzędzia do modelowania przeżycia. Zidentyfikowali 87 kluczowych cech, z których wiele odzwierciedlało interakcje metabolcznie aktywnych komórek nowotworowych z makrofagami i limfocytami T, albo skupianie się konkretnych typów komórek odpornościowych w sąsiedztwie naczyń krwionośnych i fibroblastów. Wykorzystując te cechy w modelach regresji Coxa, zbudowali predyktor szacujący przeżycie bez progresji z dokładnością (AUC) około 0,8 w ciągu 24 miesięcy, przewyższając tradycyjne pojedyncze markery, takie jak barwienie PD-L1 czy obciążenie mutacyjne guza, opisane w uprzednio opublikowanych pracach. Co ważne, kilka cech okazało się powtarzalnych w dwóch niezależnych kohortach pacjentów, co sugeruje, że wzorce te nie są jedynie przypadkowym szumem.
Co to oznacza dla pacjentów
Dla osoby niebędącej specjalistą główny wniosek jest taki, że położenie komórek w guzie płuca i sposób, w jaki się odżywiają, może pomóc wyjaśnić, dlaczego niektórzy pacjenci dobrze odpowiadają na immunoterapię, a inni nie. Badanie pokazuje, że bogate informacje przestrzenne i metaboliczne uzyskane z rutynowej biopsji, w połączeniu ze sztuczną inteligencją i modelowaniem statystycznym, mogą ujawnić sygnatury wskazujące na prawdopodobne korzyści lub oporność. Choć wyniki wymagają walidacji w większych grupach i na przekrojach całej tkanki, wytyczają drogę ku przyszłym testom, które mogłyby od początku leczenia informować lekarzy, którzy pacjenci mają większe szanse na długotrwałą kontrolę dzięki immunoterapii, a którzy mogą wymagać alternatywnych lub terapii łączonych.
Cytowanie: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Słowa kluczowe: oporność na immunoterapię, niedrobnokomórkowy rak płuca, mikrośrodowisko guza, biologia przestrzenna, metabolizm nowotworu