Clear Sky Science · pl
Hydrożel z sygnałami adhezji międzykomórkowej wzmacnia regenerację nerwową
Pomoc dla zranionego mózgu w samoleczeniu
Urazowe uszkodzenia mózgu mogą pozostawić długotrwałe problemy z ruchem, pamięcią i myśleniem, ponieważ uszkodzone neurony rzadko odrastają lub ponownie łączą się prawidłowo. Lekarze mogą usunąć skrzepy krwi lub ustabilizować czaszkę, ale mają niewiele narzędzi do odbudowy delikatnych połączeń mózgowych. W badaniu opisano miękki, wodnisty materiał zwany hydrożelem, zaprojektowany tak, by naśladować naturalne sposoby, w jakie komórki mózgu przylegają do siebie. Odtwarzając te drobne „uściski dłoni” między komórkami, materiał pomaga uszkodzonym włóknom nerwowym odrastać, ponownie tworzyć połączenia i przywracać funkcję w uszkodzonych mózgach szczurów.
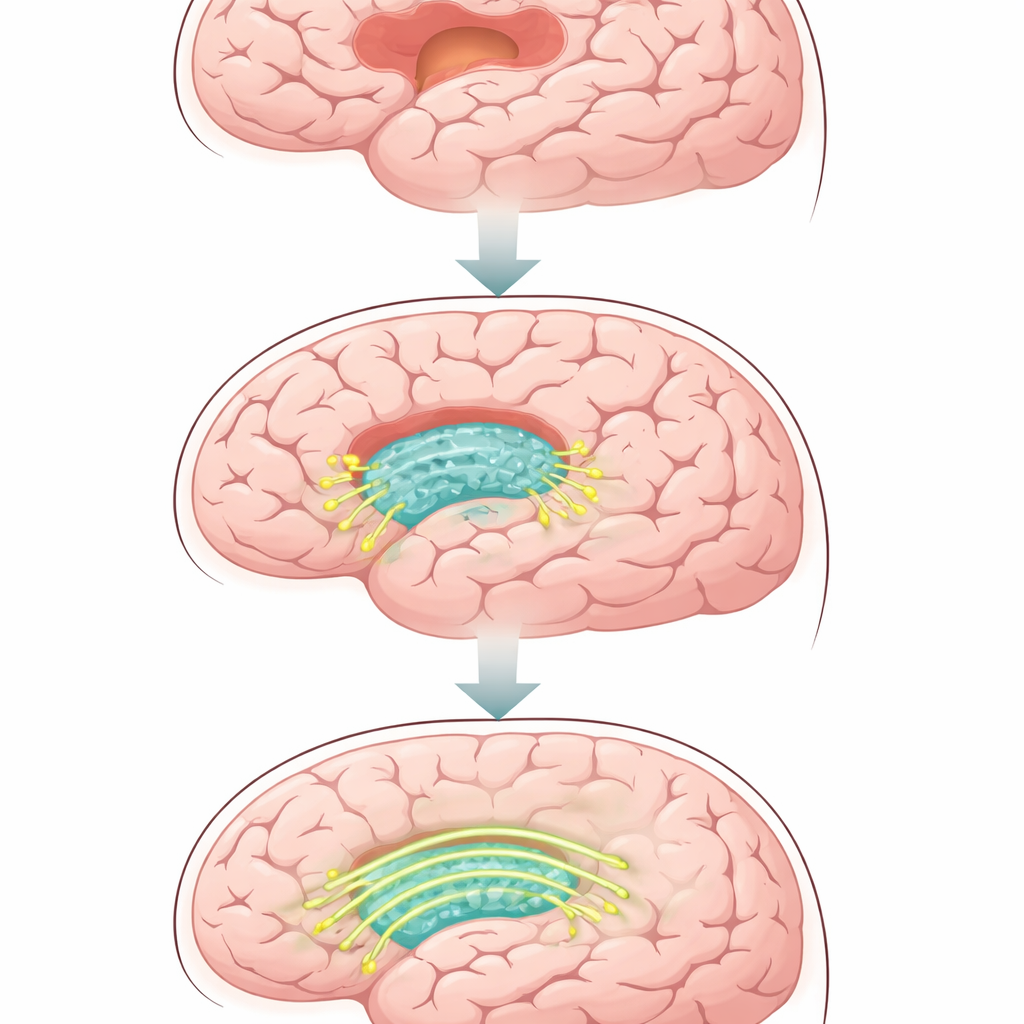
Miękkie rusztowanie dla uszkodzonej tkanki mózgowej
Naukowcy zaczęli od hydrożelu na bazie jedwabiu, który ma konsystencję zbliżoną do tkanki mózgowej — bardzo miękki i elastyczny, z wieloma drobnymi porami, w których komórki mogą się poruszać i wydłużać wypustki. Następnie powlekli ten żel cienką, płynną warstwą cząsteczek tłuszczu, która zachowuje się jak błona komórkowa. Ta warstwa może utrzymywać specjalne białka, jednocześnie pozwalając im przesuwać się wzdłuż powierzchni, tak jak na prawdziwych komórkach. W efekcie powstał trójwymiarowy, wstrzykiwalny materiał, który może wypełniać nieregularne ubytki mózgu i przedstawiać ruchome sygnały okolicznym neuronom, zamiast być biernym wypełnieniem.
Wypożyczając międzykomórkowy „uścisk dłoni” natury
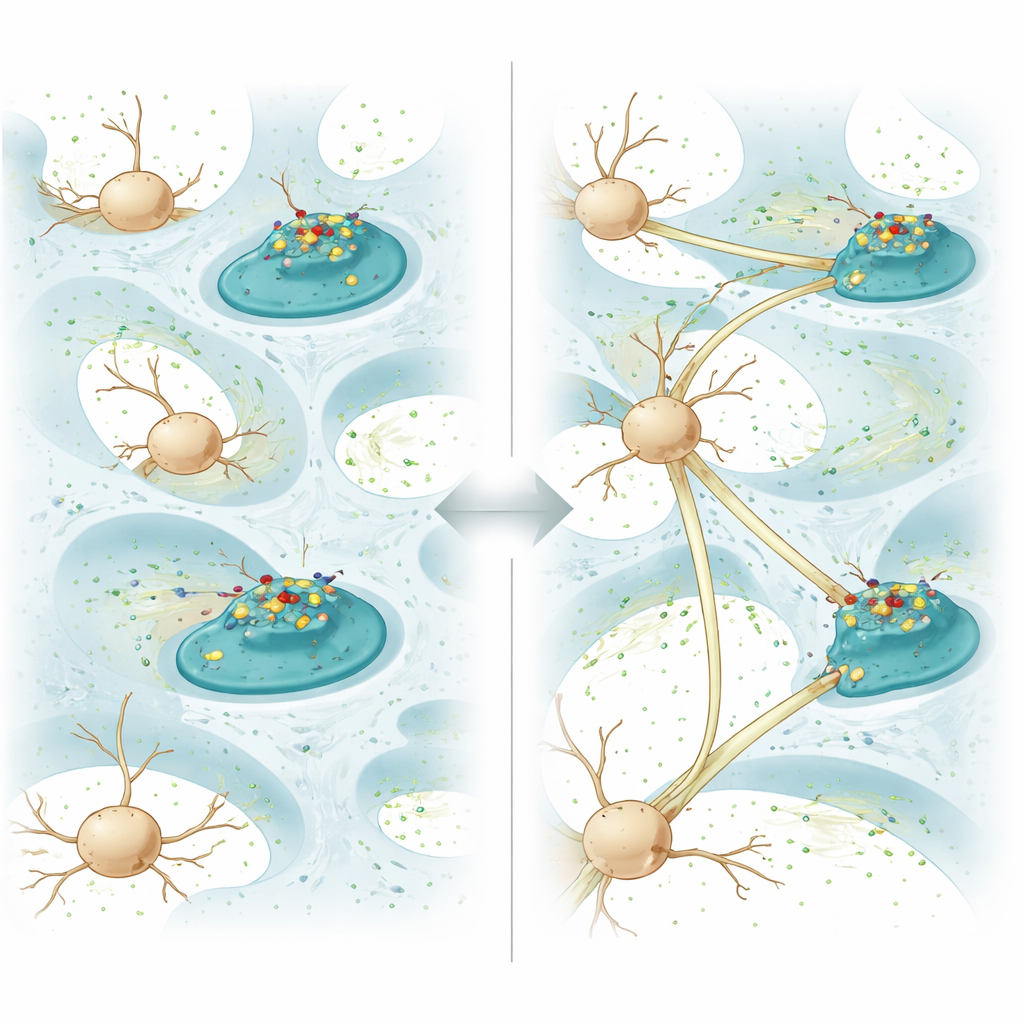
Aby przekształcić hydrożel w aktywnego partnera w gojeniu, zespół przyłączył białko zwane N-kadheryną do tłuszczowej powłoki. W mózgu N-kadheryna znajduje się na powierzchni neuronów i pomaga sąsiednim komórkom rozpoznawać się i chwytać nawzajem, tworząc stabilne kontakty, a ostatecznie synapsy, gdzie sygnały przechodzą z komórki do komórki. W tym żelu N-kadheryna nie jest unieruchomiona; może swobodnie dyfundować po powłoce. Kiedy neurony rosną w kontakcie z żelem, białko grupuje się w punktach styku ich błon z materiałem, przebudowując drobne wypustki komórek i uruchamiając tworzenie połączeń międzykomórkowych. W hodowlach neurony rosnące na żelu z „dyfuzyjną N-kadheryną” wydłużały dłuższe włókna, tworzyły więcej połączeń i wykazywały silniejszą komunikację elektryczną niż na podobnych żelach, gdzie białko było unieruchomione i niemobilne.
Aktywacja wewnętrznych programów naprawczych mózgu
Ponad zwykłym kontaktem, hydrożel także skłania neurony do włączenia wewnętrznych szlaków naprawczych. Analizy genów i białek wykazały, że komórki na żelu z dyfuzyjną N-kadheryną zmniejszały sygnały prowadzące do zaprogramowanej śmierci komórkowej i wzmacniały szlaki znane z wspierania wzrostu i przeżycia. W szczególności materiał zwiększał poziomy białka zwanego trombospondyną-1, które jest wydzielane przez komórki wspierające w mózgu i może zarówno promować tworzenie synaps, jak i aktywować sygnały sprzyjające wzrostowi. Dwa z tych szlaków, często określane jako TGF-β/Smad oraz AKT/mTOR, zostały silnie włączone, prowadząc do zdrowszych mitochondriów, większej produkcji energii i zwiększonego odrastania przeciętych włókien nerwowych w modelu mikrofluidycznym imitującym przecięte aksony.
Od szalki Petriego do żywego mózgu
Aby sprawdzić, czy te efekty mają znaczenie w żywym mózgu, zespół wstrzyknął hydrożel do szczurów z kontrolowaną formą urazowego uszkodzenia mózgu. W ciągu kilku tygodni zwierzęta leczone żelem z dyfuzyjną N-kadheryną wypadały lepiej w testach ruchowych oraz w zadaniu labiryntu wodnego mierzącym uczenie się i pamięć, w porównaniu ze zwierzętami otrzymującymi zwykły żel, żel z samymi lipidami lub tylko sól fizjologiczną. Obrazowanie mózgu i preparaty tkankowe ujawniły mniejsze jamy w miejscu urazu oraz więcej nowo utworzonych włókien nerwowych i synaps w obrębie naprawianego obszaru. Jednocześnie leczone mózgi wykazywały mniej nadaktywnych komórek odpornościowych i mniej gęste bliznowacenie, tworząc bardziej przyjazne środowisko dla odrostu. Markery śmierci komórek były zredukowane, podczas gdy białka związane ze zdrową komunikacją między neuronami były podwyższone.
Dlaczego to ma znaczenie dla przyszłej naprawy mózgu
Mówiąc prościej, praca ta pokazuje, że dostarczenie uszkodzonej tkance mózgowej odpowiedniego rodzaju „sygnałów społecznych” może istotnie wpłynąć na to, jak dobrze się goi. Zamiast jedynie mechanicznie podpierać komórki, hydrożel odtwarza ruchome sygnały kontaktowe, których prawdziwe komórki mózgu używają do odnajdywania się i trzymania razem. U szczurów ta strategia nie tylko wypełniała ubytki w mózgu, ale także pomagała odbudować funkcjonalne obwody nerwowe i poprawiała zachowanie po urazie. Chociaż przed zastosowaniem u ludzi potrzebne są dalsze badania, podejście — osadzanie swobodnie poruszających się białek adhezyjnych w miękkich, wstrzykiwalnych żelach — może wykraczać poza N-kadherynę i poza mózg, oferując uniwersalną receptę na materiały, które aktywnie kierują regeneracją tkanek.
Cytowanie: Tang, X., Zhang, S., Liu, M. et al. Hydrogel with cell-cell adhesion cues enhances neural regeneration. Nat Commun 17, 2178 (2026). https://doi.org/10.1038/s41467-026-68632-9
Słowa kluczowe: regeneracja nerwowa, urazowe uszkodzenie mózgu, rusztowanie hydrożelowe, adhezja komórkowa, N-kadheryna