Clear Sky Science · pl
H3K9me2 zależne od G9a kieruje regeneracją nabłonka jelitowego poprzez epigenetyczne wyciszanie genów związanych z cyklem komórkowym
Dlaczego samonaprawa jelita ma znaczenie
Każdego dnia wyściółka jelita wystawiona jest na surowe warunki: kwas żołądkowy, cząstki pokarmu i biliony mikroorganizmów. Mimo to tkanka ta nie tylko przetrwa, lecz nieustannie się naprawia. Gdy ten system naprawczy zawodzi — po radioterapii, w chorobach zapalnych jelit czy przy ciężkich infekcjach — ludzie mogą cierpieć z powodu bólu, krwawień i zagrożenia życia. Badanie to odkrywa ukryty „włącznik” w komórkach jelitowych, który pomaga im zdecydować, kiedy przestać odpoczywać, a kiedy zacząć odbudowę, co daje wskazówki do nowych terapii mogących wzmocnić naturalne mechanizmy naprawcze jelita.
Delikatna architektura nieustannie pod obciążeniem
Wnętrze jelita pod mikroskopem przypomina puszysty dywan, z palczastymi kosmkami absorbującymi składniki odżywcze oraz kieszeniami zwanymi kryptami, gdzie mieszkają komórki macierzyste. Te komórki oraz ich szybko dzielące się potomki muszą utrzymać równowagę między stałą odnową a naprawą awaryjną. Autorzy skupili się na tym, jak chemiczne znaczniki na białkach upakowujących DNA, zwanych histonami, wpływają na tę równowagę. Znaczniki te nie zmieniają samych genów, lecz działają bardziej jak regulatory natężenia — przyciski ściemniające, które włączają lub wyciszają grupy genów, gdy jelito przechodzi ze stanu normalnego do uszkodzenia i z powrotem do zdrowia.
Marka epigenetyczna śledząca uszkodzenia i gojenie
Na modelu myszy narażonych na promieniowanie — częstą przyczynę uszkodzeń jelita podczas leczenia nowotworów — badacze przeanalizowali wiele różnych znaków histonowych w kryptach bogatych w komórki macierzyste. Jeden znacznik, znany jako H3K9me2, gwałtownie wzrastał, gdy jelito przechodziło ze stanu uszkodzenia do naprawy. Jego enzym „piszący”, białko nazwane G9a, wykazywało podobny wzorzec. Zespół przeanalizował także próbki ludzkie od pacjentów po radioterapii miednicy oraz od osób z chorobą Crohna. W obu przypadkach wyższe poziomy H3K9me2 i G9a w komórkach jelitowych szły w parze z lepszymi oznakami naprawy tkanki, co sugeruje zachowanie tego mechanizmu u myszy i u ludzi.
Gdy włącznik naprawy zawodzi
Aby sprawdzić, czy ten znacznik jest tylko obserwatorem, czy rzeczywiście napędza gojenie, naukowcy usunęli G9a specyficznie z wyściółki jelita myszy albo zablokowali jego aktywność lekiem. W obu przypadkach poziomy H3K9me2 spadły. Po napromieniowaniu lub uszkodzeniu chemicznym takie myszy traciły więcej masy ciała, miały krótsze, bardziej uszkodzone jelita i wykazywały mniej regenerujących krypt oraz komórek macierzystych niż zwierzęta kontrolne. Nawet bez celowego urazu wyściółka jelita myszy pozbawionych G9a wyglądała ubożej: krypty były płytsze, kosmki krótsze, a liczba komórek macierzystych i ich wyspecjalizowanych potomków spadła. Malutkie „mini‑jelita” hodowane z tych komórek in vitro również słabo rosły, co podkreśla, że ten układ molekularny jest kluczowy dla codziennej odnowy jelita.
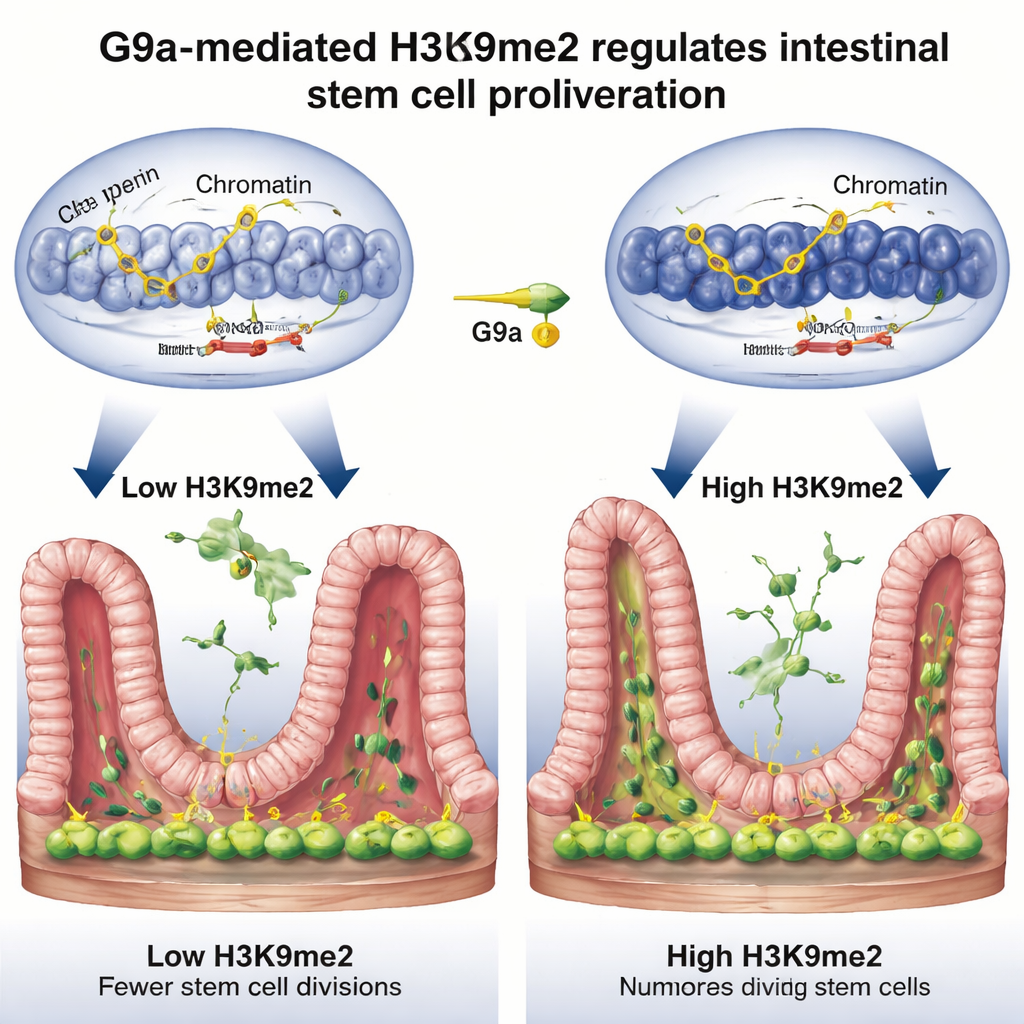
Zmniejszanie hamulców podziału komórkowego
Idąc dalej, zespół zapytał, które geny są kontrolowane przez ten włącznik naprawczy. Łącząc trzy silne metody genomowe, odkryli, że H3K9me2, umieszczany przez G9a, ma tendencję do lokalizowania się na odcinkach DNA, które zwykle działają jak hamulce cyklu komórkowego — genach takich jak Rb1cc1, Rb1, Cdkn1a i Pten, które spowalniają lub zatrzymują podziały. Gdy G9a zabrakło, chemiczny znak znikał z tych regionów, otwierała się okoliczna struktura chromatinowa, a geny‑hamulce były silniej aktywowane, prowadząc do osłabionej proliferacji komórek macierzystych. Podczas normalnej naprawy po urazie poziomy H3K9me2 przy tych genach rosły, ich aktywność malała, a komórki macierzyste mogły swobodniej dzielić się i odbudowywać wyściółkę. W istocie G9a i H3K9me2 tymczasowo uciszają sygnały „stop”, aby tkanka mogła się odnowić.
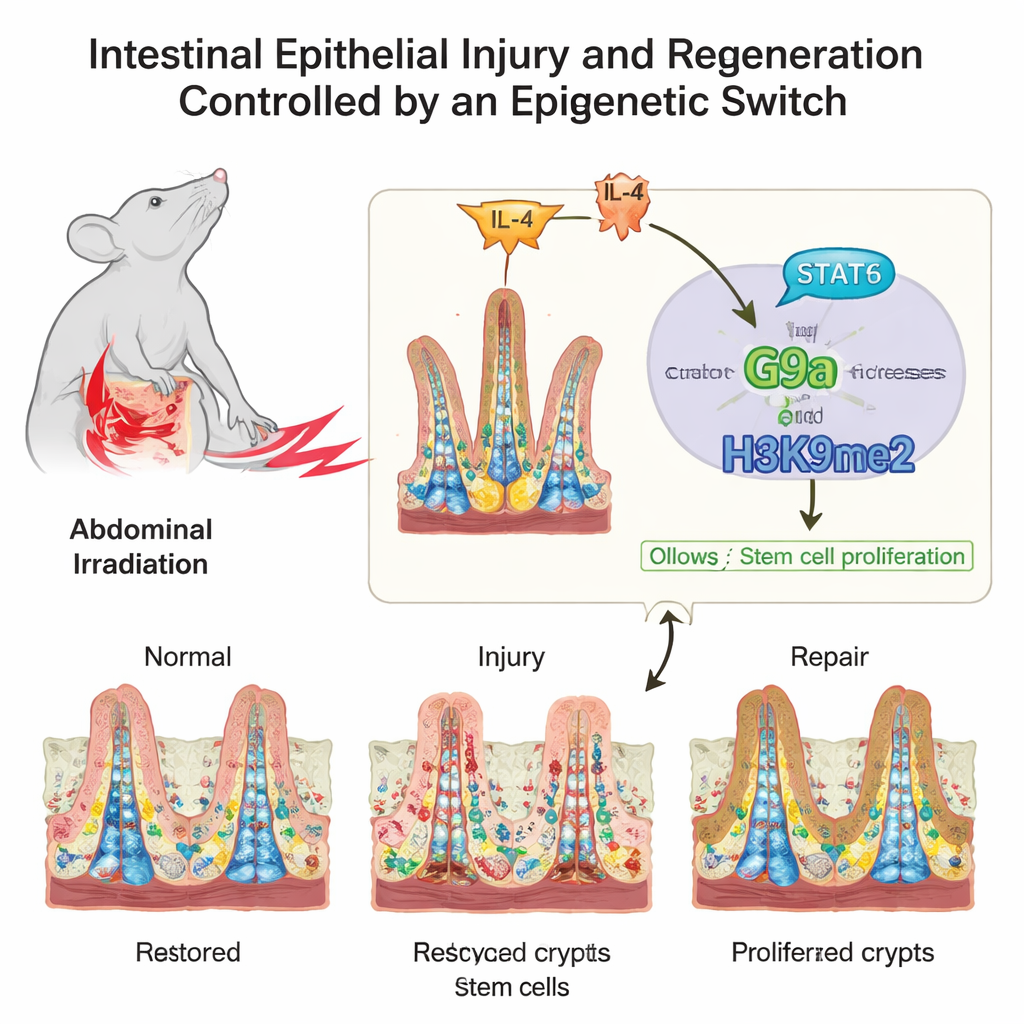
Łańcuch sygnałowy od wskazówek immunologicznych do naprawy
Jelito nie działa w izolacji; nieustannie nasłuchuje sygnałów od układu immunologicznego. Badacze wyśledzili jeden taki sygnał będący powyżej G9a. Po urazie wzrosły poziomy posłańca immunologicznego IL‑4, co uruchomiło aktywację białka STAT6 wewnątrz komórek jelitowych. Aktywowany STAT6 wiązał się bezpośrednio z regionem kontrolnym genu G9a, zwiększając jego ekspresję. Powstał w ten sposób łańcuch dowodzenia: IL‑4 aktywuje STAT6, STAT6 podnosi poziomy G9a, a G9a dodaje H3K9me2, aby wyciszyć geny‑hamulce cyklu komórkowego, co umożliwia ekspansję komórek macierzystych i odtworzenie uszkodzonej wyściółki.
Co to oznacza dla przyszłych terapii
Dla czytelnika nienależącego do specjalistów te odkrycia pokazują, że naprawa jelita jest sterowana nie tylko przez geny, lecz przez odwracalne zmiany chemiczne, które precyzyjnie regulują, kiedy te geny są używane. Szlak IL‑4–STAT6–G9a–H3K9me2 działa jak wewnętrzny panel sterowania, który chwilowo luzuje hamulce podziału komórek macierzystych na tyle, by umożliwić gojenie, a następnie można go zresetować. W przyszłości terapie delikatnie wzmacniające ten szlak — na przykład leki czy narzędzia genowe podnoszące poziom G9a we właściwym czasie i miejscu — mogą pomóc pacjentom szybciej dochodzić do zdrowia po uszkodzeniach radiacyjnych, zaostrzeniach chorób zapalnych jelit czy innych stanach uszkadzających wyściółkę jelita, przy jednoczesnym minimalizowaniu ryzyka niekontrolowanego wzrostu komórek.
Cytowanie: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Słowa kluczowe: regeneracja jelit, epigenetyka, komórki macierzyste, metylacja histonów, choroba zapalna jelit