Clear Sky Science · pl
WDR5 przebudowuje kondensaty NANOG, aby napędzać programy transkrypcyjne i podtrzymywać tożsamość komórek macierzystych
Dlaczego to ma znaczenie dla komórek macierzystych i raka
Komórki macierzyste mają niezwykłą zdolność przekształcania się w wiele różnych typów komórek — cecha ta napędza wczesny rozwój, naprawę tkanek, a niestety także niektóre nowotwory. Badanie to odkrywa, w jaki sposób dwa kluczowe białka, NANOG i WDR5, współdziałają, by utrzymać komórki macierzyste w tym elastycznym stanie. Pokazując, że WDR5 może fizycznie przekształcać sposób, w jaki NANOG tworzy skupiska na DNA, praca łączy fizykę kropelek białkowych wewnątrz jądra z kontrolą genów zarówno w zdrowych komórkach macierzystych, jak i w białaczce.
Białka, które decydują o przyszłości komórki
Komórki macierzyste embrionalne pozostają pluripotentne — czyli zdolne do przekształcenia się w prawie każdy typ komórki — dzięki regulatorom głównym takim jak NANOG, OCT4 i SOX2. Te białka włączają i wyłączają całe sieci genów. NANOG jest szczególnie centralny: nie tylko wiąże DNA, lecz także rekrutuje duże kompleksy enzymatyczne, które dodają aktywujące modyfikacje do histonów, białek pakujących DNA. WDR5 to kolejny kluczowy gracz — pomaga maszynom modyfikującym histony umieszczać znaki wskazujące aktywne geny. Choć wiadomo, że zarówno NANOG, jak i WDR5 wspierają tożsamość komórek macierzystych, nie było jasne, jak komunikują się na poziomie molekularnym i czy to wpływa na sposób, w jaki tworzą drobne kropelki, czyli „kondensaty”, w jądrze.
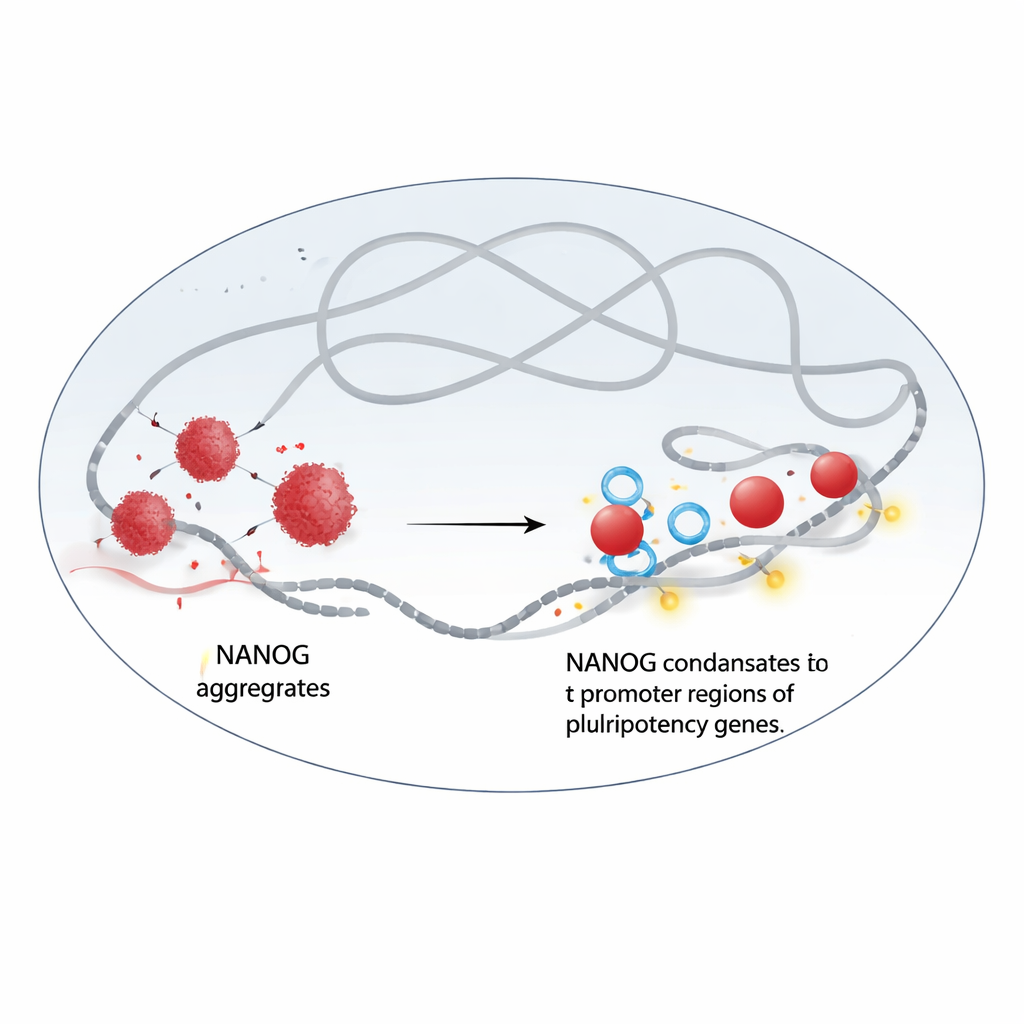
Od grudek do płynnych kropelek
Autorzy odkryli, że NANOG i WDR5 wchodzą w bezpośrednią interakcję. Gdy NANOG jest oczyszczony samodzielnie, ma tendencję do zlepiania się w nieregularne, przypominające ciało stałe agregaty. Za pomocą mikroskopii elektronowej i eksperymentów fluorescencyjnych zespół wykazał, że dodanie WDR5 reorganizuje te grudki w okrągłe, płynopodobne krople, które zachowują się jak dynamiczne kondensaty. W żywych komórkach NANOG i WDR5 gromadzą się razem w jasnych jądrowych punktach, które szybko się rozpuszczają po zastosowaniu związku chemicznego znanego z zakłócania separacji faz typu ciecz–ciecz. Gdy to następuje, oba białka tracą dużą część przyczepności do chromatyny — kompleksu DNA i białek przechowującego informację genetyczną — a ich obecność przy kluczowych genach pluripotencji spada gwałtownie.
Specjalne molekularne uściśnięcie dłoni
Aby zrozumieć partnerstwo w skali atomowej, badacze wyznaczyli strukturę krystaliczną regionu NANOG wiążącego DNA w kompleksie z WDR5. W przeciwieństwie do wielu innych partnerów WDR5, które wykorzystują krótkie elastyczne pętle, NANOG angażuje WDR5 poprzez rozległą powierzchnię obejmującą zarówno nieustrukturyzowane ramię, jak i pobliskie helisy. Pojedynczy aminokwas arginina w NANOG, na pozycji 153, wsuwa się głęboko w centralny kanał WDR5, tworząc kluczowy element interakcji „zamek-i-klucz”. Zmiana tego resztu na alaninę (mutacja R153A) w dużym stopniu eliminuje wiązanie. Co ważne, zmutowany NANOG nadal może wiązać DNA, ale WDR5 nie jest już w stanie efektywnie przekształcać jego agregatów w płynne krople, co wskazuje, że ten konkretny kontakt jest niezbędny do tworzenia funkcjonalnych kondensatów.
Utrzymywanie młodości komórek macierzystych — i co się dzieje, gdy to zawiedzie
Gdy autorzy zmodyfikowali mysie komórki macierzyste embrionalne tak, by wyrażały wyłącznie zmutowany NANOG R153A, konsekwencje były dramatyczne. Komórki mutantów straciły zwarte, kopułowate kolonie typowe dla komórek pluripotentnych i spłaszczyły się — widoczny znak różnicowania. Tworzyły mniej kolonii pozytywnych w teście fosfatazy zasadowej, kolejny wyznacznik „stemness”, i obniżyły ekspresję wielu podstawowych genów pluripotencji, takich jak Nanog, Sox2, Esrrb i Klf4. Jednocześnie włączone zostały geny związane ze specyficznymi liniami rozwojowymi, w tym regulatory kości i rozwoju. Profilowanie całego genomu wykazało, że NANOG i WDR5 przestały współzajmować tysiące promotorów, a dwie kluczowe aktywujące modyfikacje histonów, H3K4me3 i H4K16ac, zostały specyficznie utracone na tych wspólnych miejscach. Wczesne podczas różnicowania te chemiczne znaki i nowo powstałe transkrypty RNA malały zanim spadły całkowite poziomy mRNA, co wskazuje na pierwotną porażkę w utrzymaniu aktywnej chromatyny.
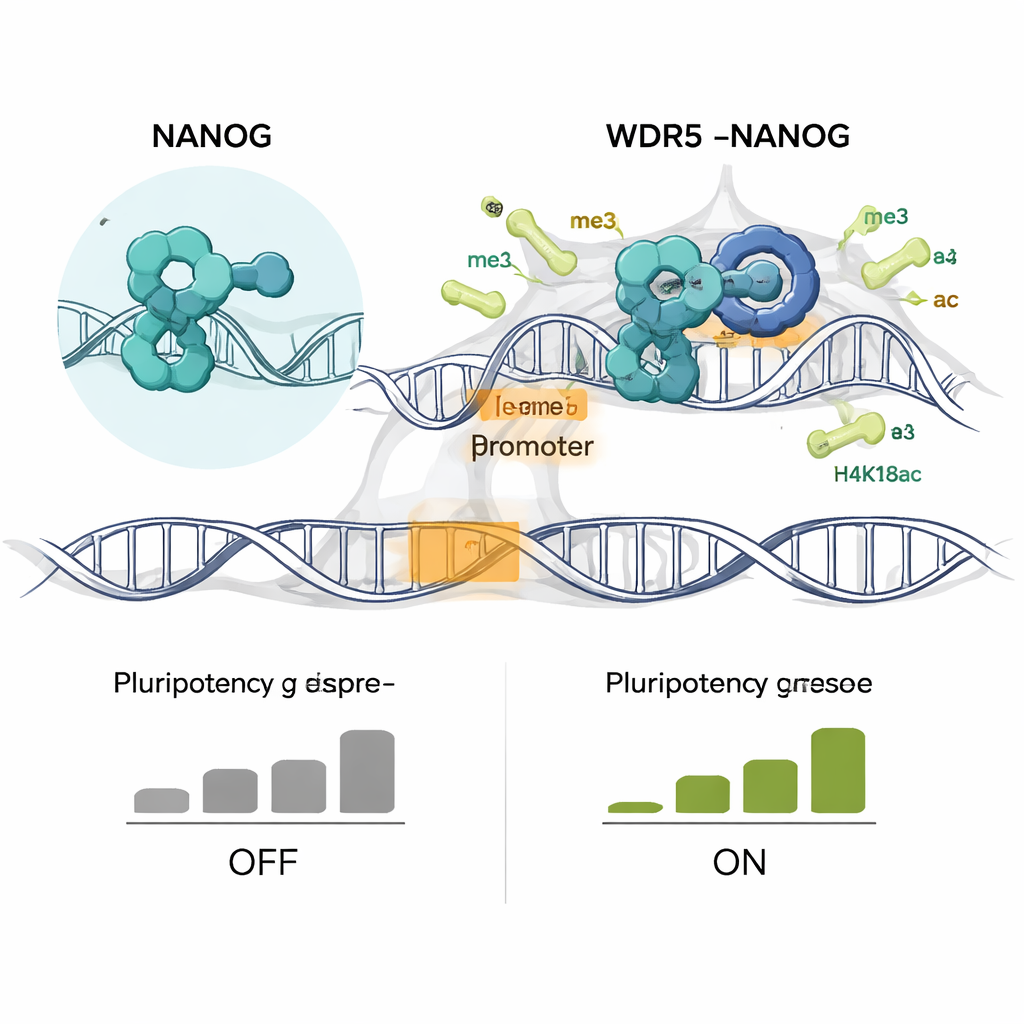
Przekształcanie podstawowego mechanizmu w strategię przeciwnowotworową
Ponieważ podobne sieci genowe kontrolują niektóre komórki macierzyste nowotworów, zespół sprawdził, czy zakłócenie osi NANOG–WDR5 może osłabić komórki macierzyste białaczki w modelu mysiej ostrej białaczki mieloblastycznej. Małocząsteczkowy lek C16, który wiąże to samo wnękowe miejsce WDR5 używane przez NANOG, selektywnie osłabił interakcję WDR5–NANOG. W komórkach białaczkowych C16 zdecydowanie zmniejszył tworzenie kolonii, wyczerpał populację przypominającą komórki macierzyste i przesunął komórki w kierunku dojrzałych losów mieloidalnych, jednocześnie znacznie bardziej oszczędzając normalne krwiotwórcze komórki macierzyste niż istniejący lek przeciw białaczce, który celuje w innego partnera WDR5. Sekwencjonowanie RNA pokazało, że C16 wyłącza programy genowe związane ze stemness i samoodnową oraz zwiększa ścieżki różnicowania. U myszy leczenie C16 zmniejszyło populacje komórek macierzystych i prekursorowych białaczki, podkreślając terapeutyczny potencjał ukierunkowania tego partnerstwa białkowego.
Szeroki obraz: jak krople pomagają zdecydować o tożsamości komórki
Ta praca ujawnia, że WDR5 robi więcej niż tylko osiadać na chromatynie i rekrutować enzymy: może fizycznie przebudowywać NANOG z inertnych agregatów w elastyczne płynne kondensaty, które osiadają na promotorach genów pluripotencji i przyciągają aktywujące modyfikacje histonów. Gdy ta przebudowa zostaje zablokowana — albo przez precyzyjną mutację w NANOG, albo przez małą cząsteczkę zakłócającą ich kontakt — komórki macierzyste tracą swoją tożsamość, a komórki macierzyste nowotworu tracą zdolność samoodnowy. Dla czytelnika niebędącego specjalistą kluczowe przesłanie jest takie, że drobne zmiany w tym, jak białka składają się w krople na DNA, mogą mieć ogromne konsekwencje dla tego, czy komórka pozostaje młoda i plastyczna, dojrzewa w określony los czy napędza chorobę.
Cytowanie: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
Słowa kluczowe: pluripotencja komórek macierzystych, NANOG, WDR5, separacja faz, komórki macierzyste białaczki