Clear Sky Science · pl
Dwufunkcyjne syntazy sygnału quorum DspII i DspI koordynują przełącznik wirulencji w Pseudomonas aeruginosa
Jak szpitalny „superbakterium” zmienia strategię ataku
Pseudomonas aeruginosa to znany drobnoustrój szpitalny, który może wywoływać uporczywe zakażenia płuc i ran, zwłaszcza u pacjentów o osłabionej odporności. Przeżywa, przełączając się między dwoma stylami życia: chronioną, wolno rosnącą społecznością zwaną biofilmem a szybko poruszającą się, agresywną formą atakującą tkanki. Badanie ujawnia, jak bakteria sama decyduje, kiedy uciec z długotrwałego biofilmu i rozpocząć nagły ostry atak, co odsłania potencjalne nowe słabe punkty dla przyszłych terapii.
Życie mikroba między ukrywaniem się a atakiem
Wiele zakażeń bakteryjnych przebiega etapami. Na początku komórki pływające swobodnie rozprzestrzeniają się po organizmie i uruchamiają silne mechanizmy uszkadzające tkanki gospodarza. Później często osiadają w biofilmach — grubych, śluzowatych warstwach przylegających do powierzchni, takich jak cewniki, tkanka płucna czy rany. W tych społecznościach komórki są otoczone ochronną macierzą, która utrudnia ich eliminację antybiotykami lub przez układ odpornościowy. Biofilmy nie są jednak ślepą uliczką. Komórki mogą je opuszczać, odzyskiwać zdolność ruchu i inicjować nowe ogniska ostrego zakażenia gdzie indziej. Do tej pory nie było jasne, jak Pseudomonas aeruginosa aktywnie koordynuje ten przełącznik z przewlekłego przetrwania z powrotem na agresywną chorobę.
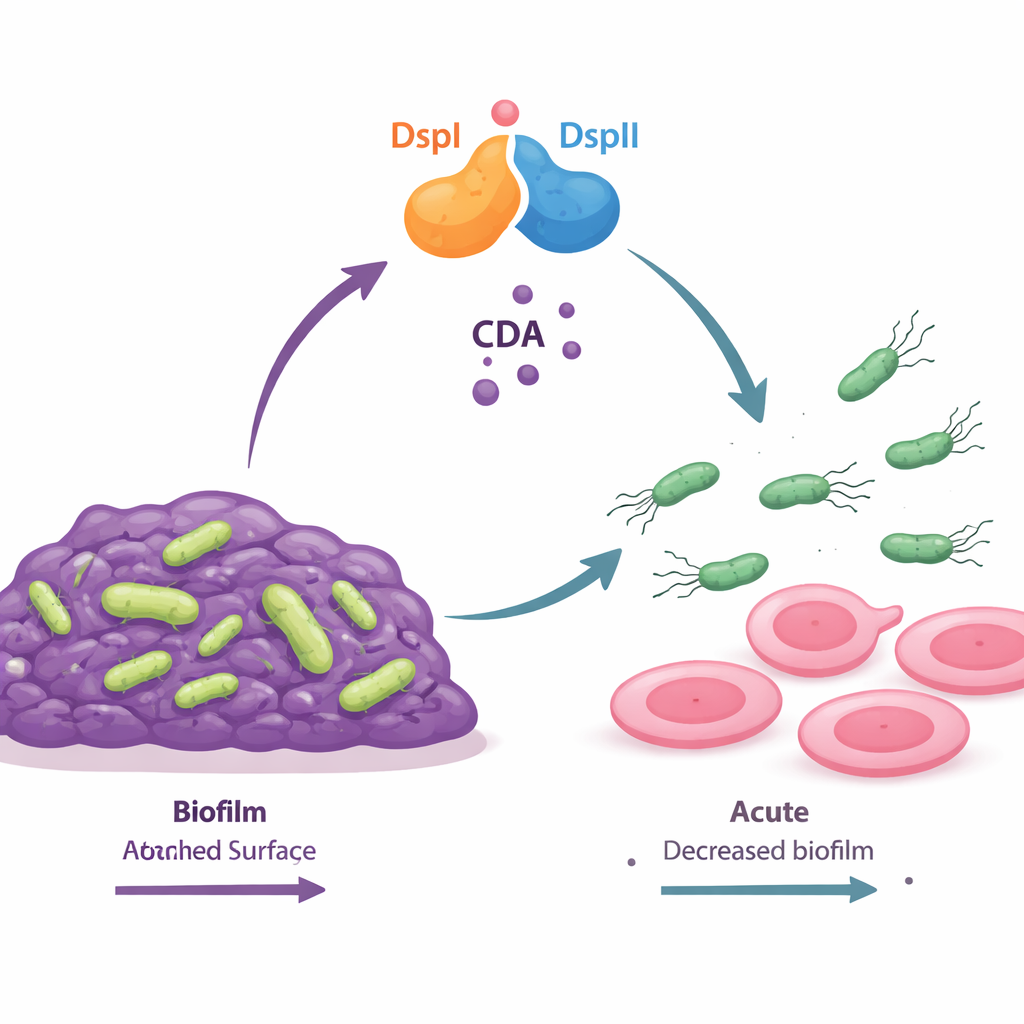
Dwubiałkowy przełącznik, który wytwarza chemiczny sygnał „start”
Autorzy odkryli, że dwa białka bakteryjne, nazwane DspI i DspII, współpracują jako rodzaj molekularnego przełącznika. Oba są enzymami tego samego ogólnego typu i znajdują się obok siebie w genomie bakterii, włączając się razem wraz ze wzrostem gęstości populacji. Gdy łączą się w parę, wytwarzają mały kwas tłuszczowy zwany cis-2-dekenoicznym kwasem (CDA), będący częścią szerszej grupy cząsteczek komunikacyjnych znanych jako sygnały DSF. Mutanty pozbawione DspI lub DspII nie potrafiły już produkować CDA, tworzyły nadzwyczaj grube biofilmy i traciły zdolność do rozprzestrzeniania się po powierzchniach. Dopiero przywrócenie obu białek razem przywracało normalną produkcję sygnału, rozpad biofilmu i ruchliwość, co pokazuje, że oba enzymy funkcjonują jako współzależny zespół.
Z chemicznego sygnału do ruchu i ucieczki
CDA nie działa samotnie; wnika w wewnętrzne okablowanie bakterii. Zespół wykazał, że CDA obniża poziomy innego przekaźnika, cyklicznego di-GMP, poprzez zwiększenie aktywności specyficznego enzymu RbdA, który rozkłada ten przekaźnik. Wysoki poziom cyklicznego di-GMP zwykle sprzyja budowie biofilmu, stymulując produkcję lepkawej macierzy cukrowej i tłumiąc wici — maleńkie śmigła napędzające pływanie. Gdy obecne jest CDA, poziomy cyklicznego di-GMP spadają, regulator FleQ zmienia sposób działania, produkcja lepkich cukrów maleje, a wici są wydłużane i wzmacniane. W efekcie biofilmy rozluźniają się, a komórki odzyskują zdolność do oddalania się, zasiedlając nowe terytoria.
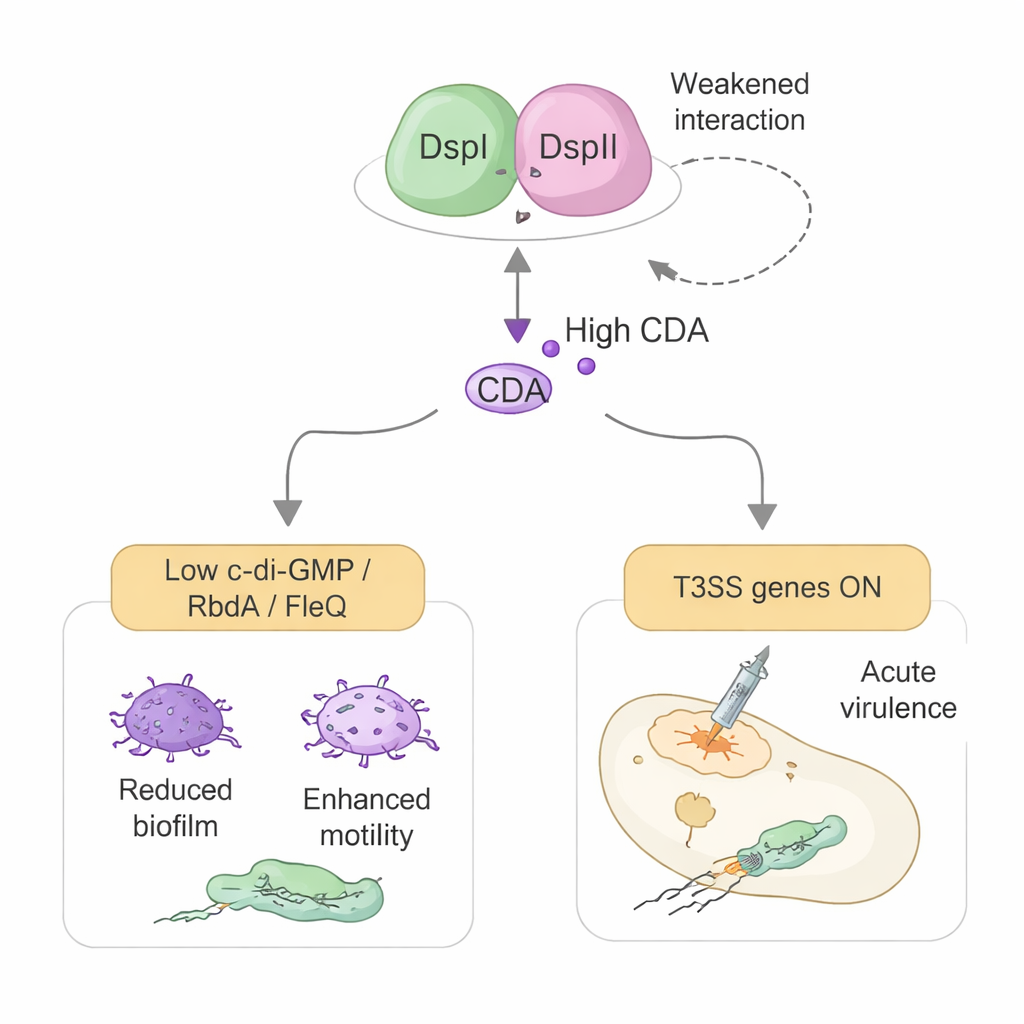
Przeprogramowanie bakteryjnego systemu broni
Badanie ujawnia także druga, nieoczekiwaną rolę DspI i DspII wykraczającą poza chemię. Ta sama para białek pomaga włączyć system sekrecji typu III (T3SS) bakterii — strzykawkowaty aparat służący do wstrzykiwania toksyn bezpośrednio do komórek gospodarza. Zamiast działać przez CDA, efekt ten zachodzi poprzez bezpośrednią kontrolę przełączników genetycznych. DspI i DspII tłumią produkcję dwóch małych regulatorowych RNA, RsmY i RsmZ, które normalnie hamują syntezę białek T3SS. Dokonują tego, wiążąc się z regionem kontroli DNA jednego z tych RNA i fizycznie wchodząc w interakcję z głównym regulatorem zwanym GacA. Gdy RsmY i RsmZ są utrzymywane w ryzach, uwalnia się aktywator pośredni RsmA, a geny kodujące T3SS i jego głównego kontrolera ExsA zostają włączone, co zwiększa cytotoksyczność w hodowli komórkowej i śmiertelność w modelu infekcji owadów.
System samoregulujący z celami leków
Sprytnie, siła partnerstwa DspI–DspII i jego kontrola nad wirulencją są same regulowane przez poziomy CDA. Przy niskich stężeniach — takich, jakie można oczekiwać w komórkach właśnie opuszczających biofilm — CDA wzmacnia interakcję między dwoma białkami i promuje dalszą produkcję sygnału oraz aktywację T3SS. Przy wysokich stężeniach wewnątrz gęstych biofilmów CDA osłabia ich interakcję i zmniejsza ich związanie z DNA, ograniczając dalszą syntezę sygnału i kosztowną produkcję broni u komórek, które pozostają na miejscu. Ta podwójna rola sprawia, że kompleks DspI–DspII jest centralnym węzłem łączącym wielkość populacji, ucieczkę z biofilmu i ostrą wirulencję. Ponieważ zakłócenie kompleksu może zablokować zarówno produkcję sygnału, jak i aktywację systemu toksyn, stanowi on atrakcyjny cel dla przyszłych leków, które mogłyby utrzymać Pseudomonas w mniej szkodliwym, przewlekłym stanie i zapobiec niebezpiecznym zaostrzeniom.
Cytowanie: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Słowa kluczowe: Pseudomonas aeruginosa, dyspersja biofilmu, quorum sensing, przełącznik wirulencji, cis-2-dekenoiczny kwas