Clear Sky Science · pl
Atlas przestrzenny raka żołądka charakteryzuje obszar zagęszczenia limfocytów
Dlaczego otoczenie guza ma znaczenie
Nowotwór to nie tylko skupisko zbuntowanych komórek; funkcjonuje w zatłoczonym sąsiedztwie komórek odpornościowych i strukturalnych, które mogą albo wspierać walkę z guzem, albo pozwalać mu się niekontrolowanie rozwijać. To badanie mapuje to otoczenie w raku żołądka z niespotykaną dotąd szczegółowością, pokazując, jak drobne ogniska aktywności immunologicznej i strefy „zimne” w obrębie tego samego guza mogą wpływać na to, czy pacjent odpowie na nowoczesne immunoterapie.
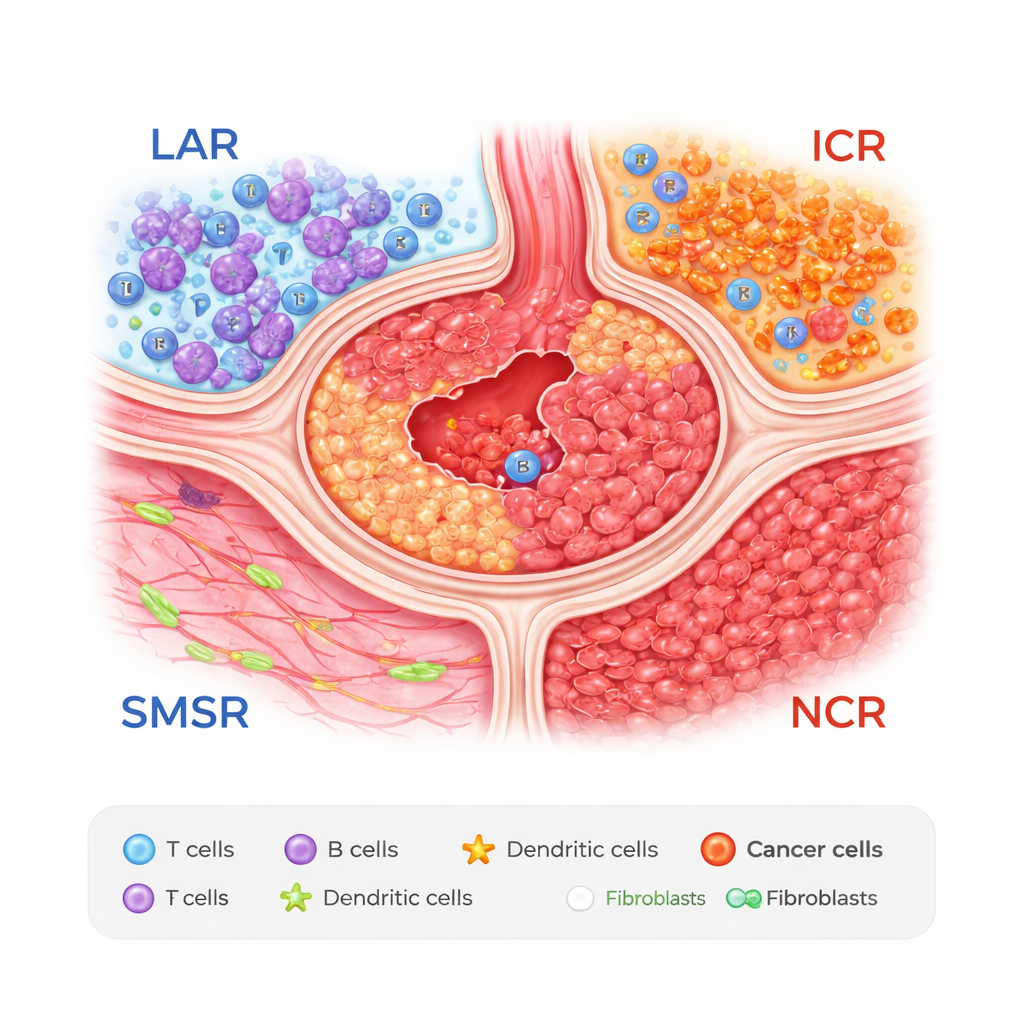
Cztery strefy wewnątrz guza żołądka
Naukowcy połączyli dwa potężne narzędzia: sekwencjonowanie RNA pojedynczych komórek, które odczytuje aktywność genów w pojedynczych komórkach, oraz transkryptomikę przestrzenną, która rejestruje, gdzie te komórki znajdują się w przekrojach tkankowych. Analizując próbki od 27 pacjentów, odkryli, że guzy żołądka można podzielić na cztery powtarzalne strefy. Jedną z nich jest obszar zagęszczenia limfocytów (LAR), bogaty w skupiska komórek T i B przypominające miniaturowe węzły chłonne. Inna to obszar mięśni gładkich i zrębu (SMSR), zdominowany przez mięśnie i tkankę łączną. Pozostałe dwie strefy to obszary bogate w komórki nowotworowe: immunogeniczny obszar raka (ICR), gdzie komórki nowotworowe mieszają się z niektórymi ochronnymi typami komórek żołądka, oraz negatywnie-immunogeniczny obszar raka (NCR), wypełniony komórkami złośliwymi i względnie niewielką liczbą komórek odpornościowych.
Ogniska odpornościowe powiązane z lepszymi wynikami
Zespół stwierdził, że strefa LAR jest wzbogacona w geny typowo występujące we węzłach chłonnych, gdzie komórki odpornościowe są szkolone i aktywowane. Należą do nich sygnały ułatwiające rekrutację limfocytów i organizowanie ich w struktury zwane wtórnymi strukturami limfoidalnymi. Analiza dużych publicznych zbiorów danych nowotworowych pokazała, że guzy o wyższej ekspresji genów powiązanych z LAR mają tendencję do lepszych przeżyć pacjentów i nieco wyższego prawdopodobieństwa odpowiedzi na terapie blokujące punkty kontrolne, które uwalniają hamulce z komórek T. Natomiast sygnatury genowe pochodzące ze stref bogatych w mięśnie lub silnie nowotworowych zwykle wiązały się z gorszymi wynikami w różnych typach nowotworów.
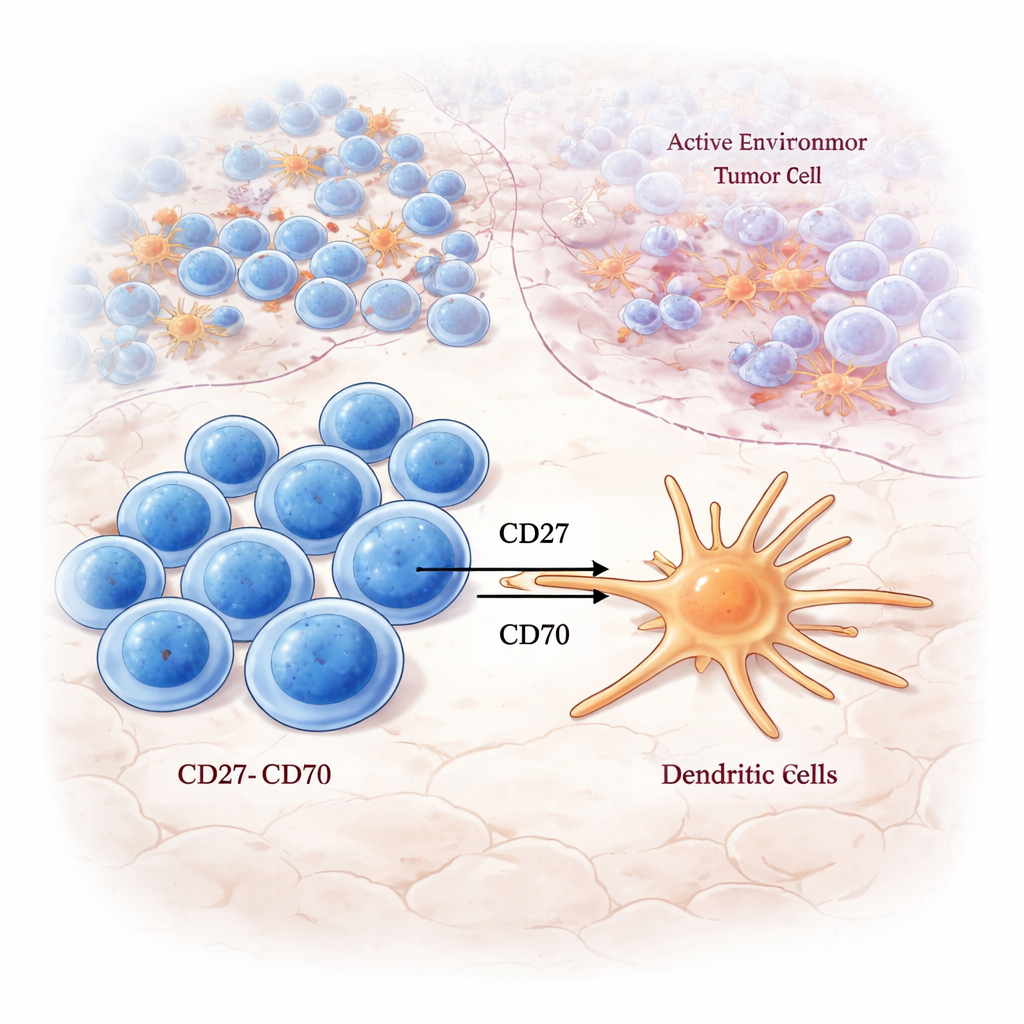
Gdzie niedojrzałe komórki T uczą się walczyć
Przybliżając obraz LAR, autorzy zaobserwowali silną aktywność szlaków sygnałowych kluczowych dla uruchamiania komórek T: sygnalizacji receptora komórki T, ścieżek kostymulacyjnych oraz przetwarzania antygenu. Naiwne komórki CD8 T — komórki, które jeszcze nie zadeklarowały ataku na konkretny cel — były szczególnie powiązane z tymi sygnałami aktywacji wewnątrz LAR, ale nie w innych miejscach. Dzięki wielobarwnemu barwieniu wykryto w LAR komórki CD8 niosące markery odnowy i proliferacji, co sugeruje, że ta strefa działa jako miejsce szkolenia i ekspansji na miejscu, gdzie przygotowywane są świeże komórki walczące z guzem.
Dwie odmiany immunologicznego sąsiedztwa
Nie wszystkie LAR były jednakowe. Gdy badacze pogrupowali pacjentów według składu komórkowego ich LAR, ujawnili dwa wzorce. W guzach „Grupy A” LAR przypominały klasyczne węzły chłonne, bogate w wyspecjalizowane komórki B i komórki dendrytyczne, a sąsiednie obszary nowotworu były wypełnione aktywowanymi, gotowymi do walki limfocytami. W „Grupie B” LAR były mniej rozwinięte, a przyległa tkanka nowotworowa zawierała więcej komórek T w stanie spoczynku, mniej zaangażowanych. Zaawansowane analizy komputerowe obrazów tkankowych potwierdziły, że aktywowane komórki odpornościowe fizycznie skupiają się wokół bardziej dojrzałych LAR, co sugeruje, że lokalna architektura może kierunkować intensywność odpowiedzi immunologicznej wobec guza.
Sygnały kontrolne w przestrzeni
Badanie śledziło także rozmieszczenie „przełączników” immunologicznych znanych jako cząsteczki punktów kontrolnych. Pary stymulujące, takie jak CD27–CD70, koncentrowały się w LAR, szczególnie w guzach Grupy A, łącząc wyczerpane, lecz reaktywne wobec guza komórki CD8 z komórkami dendrytycznymi, które mogą dodatkowo wzmocnić ich aktywność. Natomiast wiele hamujących par punktów kontrolnych, jak TIGIT–NECTIN2 i LAG3–LGALS3, było wzbogaconych w NCR, najbardziej zdominowanej przez nowotwór strefie. Sugeruje to, że nawet gdy sygnalizacja receptora komórki T jest obecna, otaczający krajobraz punktów kontrolnych może przesunąć lokalną odpowiedź immunologiczną w stronę ataku lub supresji, w zależności od strefy guza.
Co to oznacza dla pacjentów
Dla osoby niezaznajomionej z tematem kluczowy wniosek jest taki, że to, gdzie komórki odpornościowe i sygnały znajdują się w obrębie guza, może mieć tak samo duże znaczenie jak ich liczba. Praca ta pokazuje, że raki żołądka zawierają odrębne immunologiczne sąsiedztwa, a silne, przypominające węzły chłonne regiony przy guzie wiążą się z bardziej aktywnymi, lepiej ulokowanymi komórkami T i korzystniejszymi wynikami. Rozpoznając i ewentualnie wzmacniając te obszary zagęszczenia limfocytów, przyszłe terapie mogłyby być lepiej dopasowane — wybierając leki, kombinacje lub nawet ukierunkowane sposoby dostarczania, które wykorzystują wewnętrzne immunologiczne umocnienia guza.
Cytowanie: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Słowa kluczowe: rak żołądka, mikrośrodowisko guza, wtórne struktury limfoidalne, transkryptomika przestrzenna, immunoterapia nowotworów