Clear Sky Science · pl
Różnicowe starzenie się gruczołów mlekowych u samic nierodzących i rodzących ujawnia komórki nabłonkowe hybrydowe IL33+
Jak ciąża może przekształcić ryzyko zachorowania na raka piersi w ciągu życia
Dlaczego urodzenie dziecka we wczesnym życiu obniża ryzyko zachorowania na raka piersi w ciągu całego życia, podczas gdy samo starzenie się je zwiększa? W tym badaniu na myszach przyjrzano się „ekosystemowi” komórkowemu piersi w miarę upływu czasu, porównując zwierzęta, które nigdy nie były w ciąży, z tymi, które miały ciążę. Śledząc, jak poszczególne komórki zmieniają się wraz z wiekiem i rozmnażaniem, badacze odkryli rzadki, zmieniający kształt typ komórki, który może pomóc wyjaśnić długoterminową ochronę przed rakiem piersi wynikającą z ciąży.
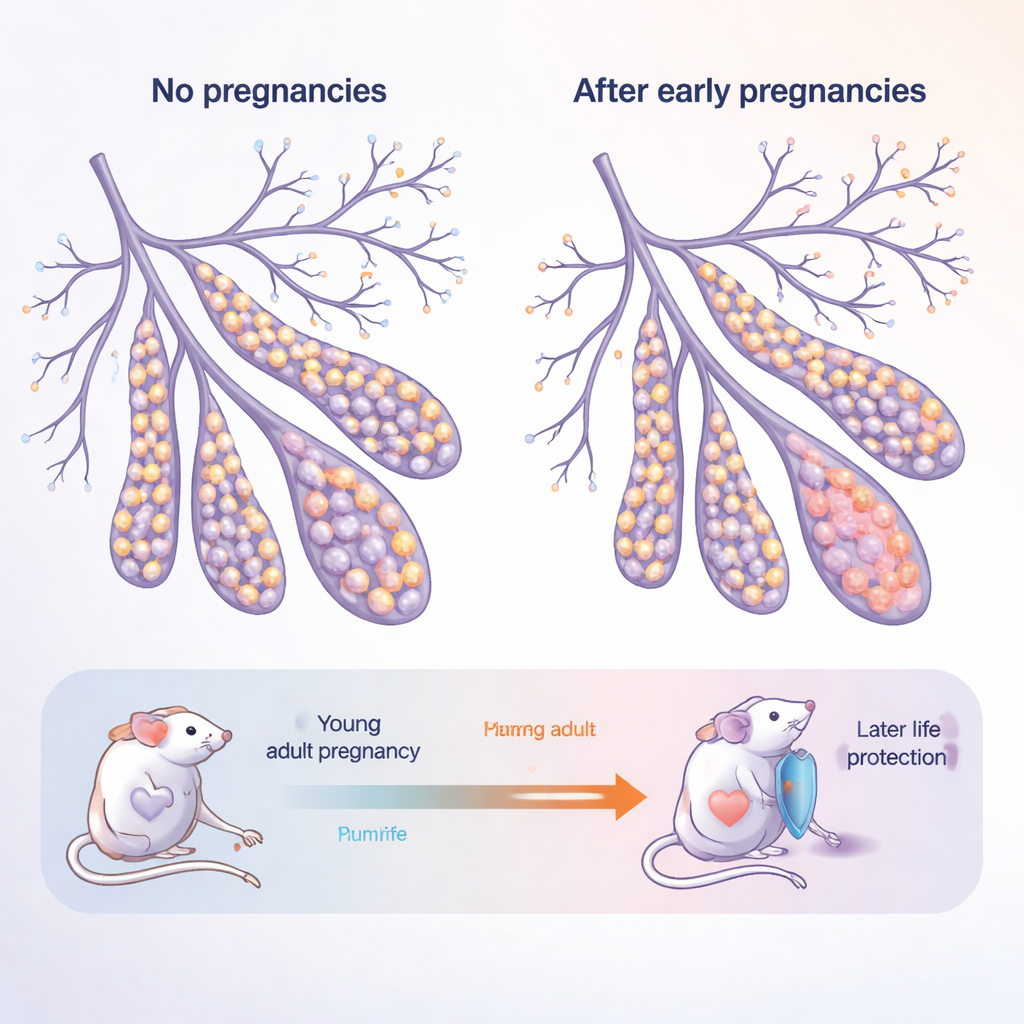
Piersi jako żywa, zmieniająca się tkanka
Gruczoł mlekowy nie jest narządem statycznym: rośnie i przebudowuje się dramatycznie w okresie dojrzewania, podczas ciąży i ponownie po zakończeniu produkcji mleka. Zbudowany jest z dwóch głównych warstw komórek nabłonkowych wyścielających przewody: wewnętrznych komórek „luminalnych”, które stykają się z mlekiem i hormonami, oraz zewnętrznych komórek „podstawnych” (basal), które zapewniają strukturę i zawierają komórki o cechach podobnych do macierzystych. Autorzy badali młode dorosłe myszy oraz starsze myszy „pseudomenopauzalne”, z których każda była albo nigdy niebrzemienna (nulliparous), albo przeszła przez wiele ciąż (parous). Projekt ten naśladuje sytuację kobiety, która rodzi w wieku dwudziestu kilku lat, a następnie starzeje się do pięćdziesiątki i dalej.
Jak starzenie i ciąża ciągną tkankę w różnych kierunkach
W miarę starzenia się myszy, które nigdy nie były w ciąży, ich gruczoły mlekowe przesuwały się w kierunku większego udziału komórek podstawnych i mniejszej liczby komórek luminalnych. Te starsze gruczoły u samic nigdy niebędących w ciąży wytwarzały też znacznie więcej organoidów — miniaturowych struktur 3D hodowanych z pojedynczych komórek — co wskazuje, że ich komórki były wyjątkowo gotowe do proliferacji. W przeciwieństwie do tego, myszy, które przeszły ciąże, wykazywały „normalizujący” balans: związany z wiekiem wzrost udziału komórek podstawnych został stłumiony, a ich komórki tworzyły mniej organoidów. Sugeruje to, że ciąża zostawia trwały ślad, który zarówno zmienia sposób, w jaki komórki wybierają swoje losy, jak i hamuje ich potencjał regeneracyjny, a wraz z nim potencjalnie podatność na nowotwory.
Odkrycie hybrydowych, zmieniających formę komórek
Aby przyjrzeć się głębiej, zespół zastosował sekwencjonowanie RNA pojedynczych komórek, aby odczytać, które geny są aktywne w tysiącach indywidualnych komórek gruczołu mlekowego. Wśród spodziewanych komórek luminalnych, podstawnych, odpornościowych i zrębowych znaleźli rzadką grupę, która nie pasowała jednoznacznie do żadnej z dwóch głównych warstw. Komórki te wyrażały markery obu linii — luminalnej i podstawnej — zyskując nazwę „hybrydowych” komórek nabłonkowych. Co uderzające, hybrydy te akumulowały się z wiekiem u myszy nigdy niebędących w ciąży, ale były znacznie rzadsze u równie starych myszy, które były w ciąży. Hybrydy silnie wyrażały gen o nazwie Il33, kodujący cząsteczkę sygnałową IL‑33, oraz markery związane z wczesnymi etapami rozwoju i wysoką plastycznością — zdolnością do zmiany tożsamości lub zachowania.
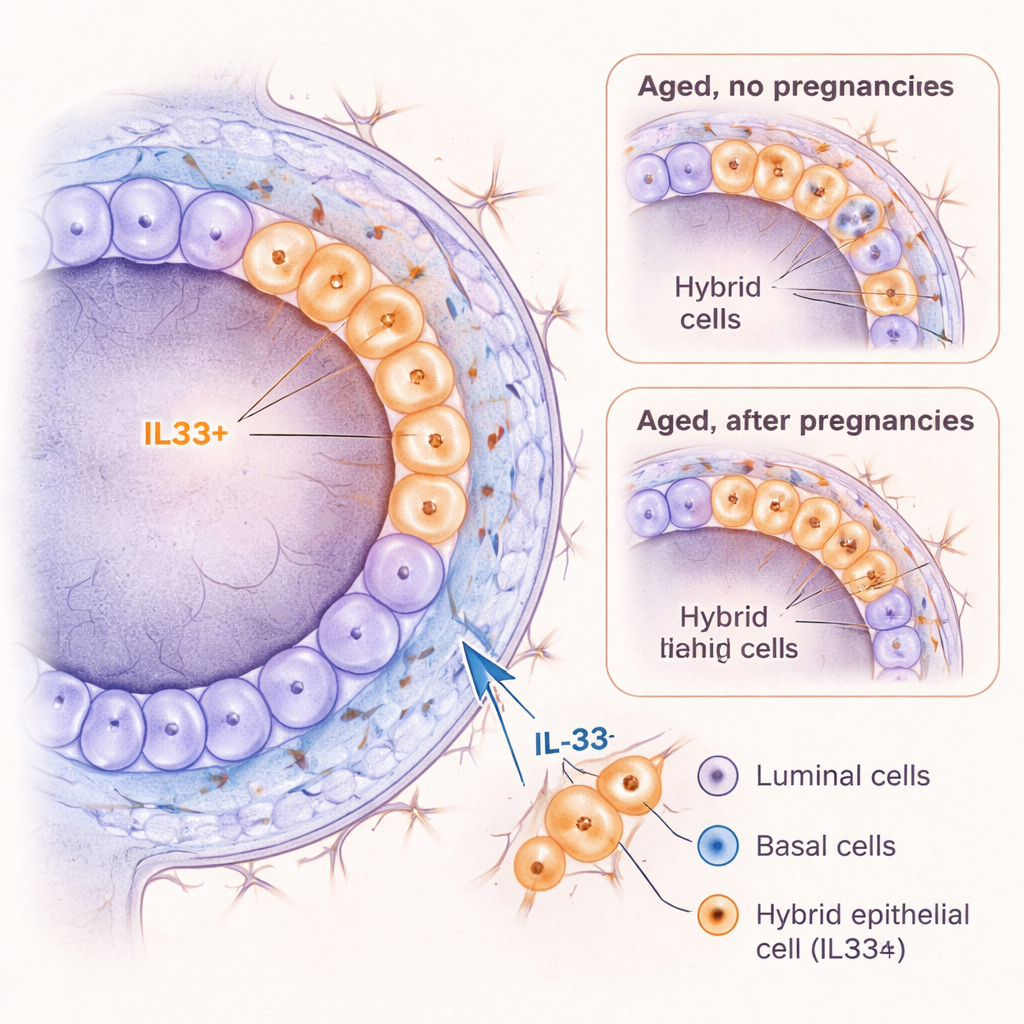
IL‑33 jako czynnik napędzający ryzykowne stany komórkowe
Ponieważ IL‑33 była powiązana z zapaleniem i rakiem w innych narządach, badacze sprawdzili, czy może aktywnie popychać komórki gruczołu mlekowego w kierunku stanu hybrydowego. Gdy traktowali młode mysie komórki mlekowe IL‑33 w hodowlach 3D, komórki warstwy podstawnej tworzyły więcej organoidów, zachowywały bardziej prymitywną tożsamość i wytwarzały więcej komórek z hybrydowym markerem KRT6A. U żywych młodych myszy krótkotrwałe wstrzyknięcia IL‑33 spowodowały poszerzenie przewodów i wywołały falę podziałów komórkowych, wraz z tymczasowym wzrostem liczby komórek hybrydowych pozytywnych dla KRT6A i przesunięciem w kierunku bardziej podstawnopodobnych komórek. Co ważne, gdy komórki nosiły mutację związaną z rakiem (utrata genu supresorowego nowotworu Trp53), IL‑33 dodatkowo zwiększała ich wzrost. Razem te wyniki sugerują, że IL‑33 pomaga tworzyć plastyczny, proliferacyjny stan komórkowy, który może być szczególnie podatny na transformację nowotworową.
Wskazówki z ludzkiej tkanki piersi
Aby sprawdzić, czy podobne komórki występują u ludzi, autorzy ponownie przeanalizowali kilka dużych zestawów danych pojedynczych komórek z normalnej tkanki piersi ludzkiej. Zidentyfikowali niewielką populację ludzkich komórek nabłonkowych, które, podobnie jak mysie hybrydy, wykazywały cechy zarówno luminalne, jak i podstawne oraz wyrażały IL33 i powiązane geny. Komórki IL33-dodatnie stawały się bardziej powszechne z wiekiem w kilku zestawach danych. W pierwotnych ludzkich komórkach gruczołu mlekowego hodowanych w laboratorium leczenie IL‑33 zwiększało tworzenie organoidów, przesuwało profil komórek w stronę cech podstawnopodobnych i wzbogacało populację komórek CD44-dodatnich — markera często kojarzonego z niedojrzałymi, podobnymi do macierzystych komórkami w raku piersi. Chociaż dostępne próbki ludzkie nie pozwoliły na jasne sprawdzenie, jak wczesna ciąża zmienia tę populację, podobieństwa między danymi od myszy i ludzi są wyraźne.
Co to oznacza dla zrozumienia ochrony przed rakiem piersi
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że ciąża wydaje się przeprogramowywać sposób, w jaki tkanka piersi się starzeje. U myszy wczesna ciąża zapobiega nagromadzeniu się bogatych w IL‑33 komórek hybrydowych, które zacierają granicę między głównymi warstwami komórek piersi i wykazują wysoką elastyczność oraz gotowość do wzrostu. Sama IL‑33 może popychać komórki w kierunku tego ryzykownego, zmieniającego formę stanu, zwłaszcza gdy obecne są mutacje związane z rakiem. Poprzez zmniejszenie liczby lub trwałości tych komórek hybrydowych ciąża może obniżać prawdopodobieństwo, że starzejąca się tkanka piersi zawiera „zły” typ komórki we „właściwym” czasie — taką, która jest gotowa przejść w stan nowotworowy. To mechanistyczne zrozumienie mogłoby w przyszłości pomóc opracować strategie naśladowania ochronnego efektu wczesnej ciąży bez konieczności zajścia w ciążę.
Cytowanie: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Słowa kluczowe: starzenie piersi, ciąża a rak piersi, komórki macierzyste gruczołu mlekowego, sygnalizacja IL-33, komórki nabłonkowe hybrydowe