Clear Sky Science · pl
Poszerzanie zakresu ładunków w koniugatów przeciwciało‑lek przez dostarczanie leków zawierających grupy hydroksylowe za pomocą samozniszczalnych fosforamidatów
Sprytniejsze pociski przeciw rakowi
Leki przeciwnowotworowe potrafią być niezwykle silne, ale często działają jak nalot dywanowy: uszkadzają tkanki zdrowe prawie tak mocno jak guzy. Koniugaty przeciwciało–lek (ADC) zostały wymyślone, by rozwiązać ten problem — przez przyłączenie silnego leku do przeciwciała, które trafia bezpośrednio do komórek nowotworowych, zamieniając terapię w naprowadzany pocisk. Ten artykuł opisuje nowy chemiczny „wtyk” między przeciwciałem a lekiem, który sprawia, że te pociski są jednocześnie bardziej precyzyjne i bardziej elastyczne, otwierając drzwi dla wielu typów leków przeciwnowotworowych, które dziś ADC-y trudno przenoszą.
Dlaczego dzisiejsze leki celowane nadal mają ograniczenia
ADC składają się z trzech części: przeciwciała rozpoznającego znacznik na komórkach nowotworowych, toksycznego leku („ładunku”) oraz chemicznego łącznika je wiążącego. Większość zatwierdzonych ADC opiera się na zaledwie kilku rodzajach ładunków, które uszkadzają DNA lub hamują podział komórek w podobny sposób. Jednym z głównych powodów jest łącznik: musi on trzymać lek mocno podczas krążenia we krwi, a następnie uwolnić go precyzyjnie wewnątrz komórki nowotworowej. Istniejące łączniki dobrze współpracują tylko z pewnymi grupami chemicznymi leków, zwłaszcza aminami, i często mają trudności z wieloma substancjami zawierającymi grupy hydroksylowe (–OH). W rezultacie wiele obiecujących środków przeciwnowotworowych pozostaje poza zasięgiem, ponieważ nie można ich bezpiecznie lub skutecznie dostarczyć obecnymi projektami ADC.
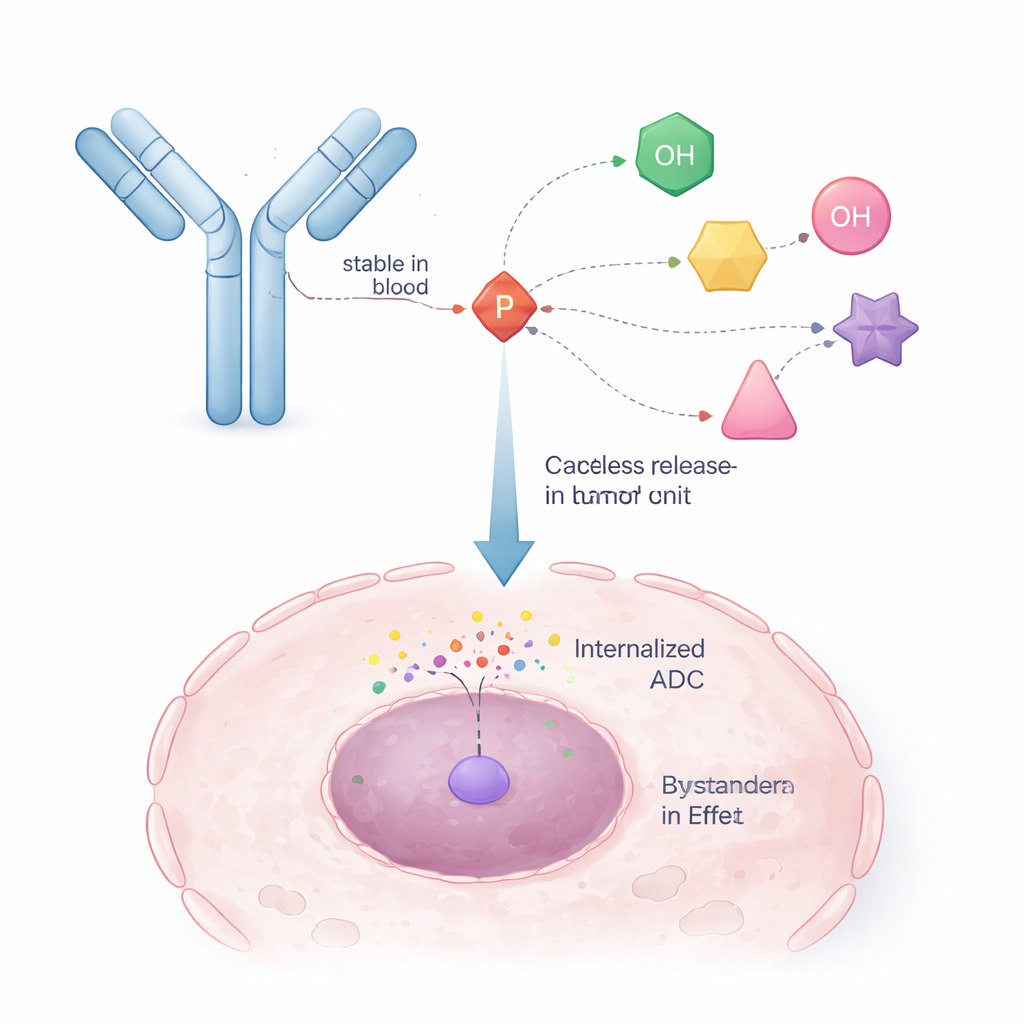
Zapożyczenie triku z leków przeciwwirusowych
Naukowcy sięgnęli po strategię już sprawdzoną w lekach przeciwwirusowych, zwaną ProTide. W tych lekach jednostka oparta na fosforze tymczasowo maskuje naładowaną grupę fosforanową leku, aby mogła wejść do komórki, a następnie rozpada się wewnątrz, uwalniając aktywną formę. Autorzy przeprojektowali ten pomysł tak, że jedno ramię rdzenia fosforowego służy do przyłączenia do przeciwciała, a pozostałe ramiona trzymają lek przeciwnowotworowy. Powstaje w ten sposób „samozniszczalny” łącznik: gdy wewnętrzny wyzwalacz (na przykład enzym w komórce nowotworowej) odcina małą część struktury, jednostka fosforowa zapada się w kontrolowany sposób i uwalnia pierwotną cząsteczkę leku z przywróconą, niezmienioną grupą hydroksylową.
Budowa wszechstronnego chemicznego wtyku
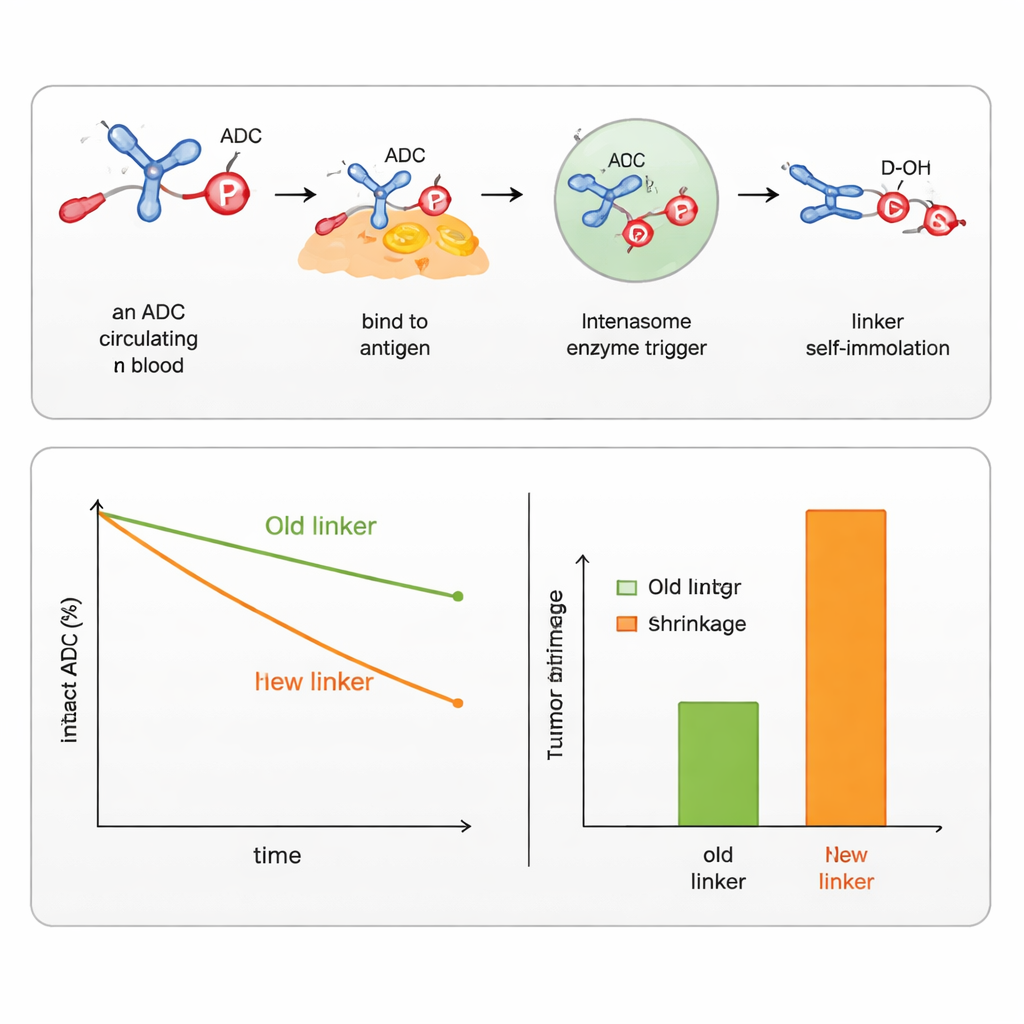
Zespół wykazał, że modyfikując grupy wokół atomu fosforu można precyzyjnie regulować stabilność łącznika we krwi oraz szybkość jego rozpadu w komórkach. Zaprojektowali wersje reagujące na kilka rodzajów wyzwalaczy powszechnych w komórkach nowotworowych, w tym esterazy i proteazy (enzymy tnące konkretne wiązania), a także enzymy rozpoznające grupy cukrowe czy warunki redukujące w przedziałach komórkowych. Korzystając z tych projektów, skutecznie przyłączyli i uwolnili zarówno aromatyczne alkohole (jak chemioterapeutyczny SN38), jak i alifatyczne alkohole (jak DXd, ładunek w zatwierdzonym ADC do raka piersi). W bezpośrednim porównaniu z istniejącymi komercyjnymi łącznikami dla SN38 i DXd, nowe łączniki fosforamidatowe utrzymywały leki przyłączone dłużej w surowicy, dostarczały więcej leku do guzów i powodowały silniejsze kurczenie się guzów u myszy, przy mniejszym wpływie na komórki zdrowe.
Odblokowanie wielu nowych ładunków przeciwnowotworowych
Aby sprawdzić szerokość zastosowań łącznika, badacze zbudowali ADC przenoszące dziesięć różnych leków, z których każdy zawiera co najmniej jedną grupę –OH, ale działa w bardzo odmienny sposób w komórkach nowotworowych. Były wśród nich inhibitory syntezy DNA, fałdowania białek (HSP90), metabolizmu energetycznego (NAMPT i DHODH) oraz translacji białek, jak również znane środki takie jak paklitaksel i gemcytabina. Pomimo dużej różnorodności struktur udało się uzyskać jednorodne ADC z wysokim stopniem załadowania leku dla wszystkich z nich. W badaniach komórkowych obejmujących różne typy nowotworów większość tych ADC wykazała aktywność w zakresie nanomolowym, a nawet subnanomolowym, oraz wyraźną selektywność wobec komórek wyrażających cel przeciwciała, potwierdzając, że łącznik konsekwentnie uwalnia aktywny lek wewnątrz właściwych komórek.
Gemcytabina jako pokazowy przykład
Gemcytabina jest powszechnie stosowaną chemioterapią, ale w formie konwencjonalnej jest tak szybko eliminowana z organizmu, że pacjenci muszą otrzymywać duże, powtarzane dawki, co ogranicza bezpieczną maksymalną podawaną ilość. Dzięki łącznikowi fosforamidatowemu autorzy przyłączyli gemcytabinę do przeciwciała celującego w HER2 w jednym z dwóch miejsc z grupą hydroksylową i wykazali, że obie wersje odzyskują pełną aktywność po wejściu do komórek nowotworowych. W modelach mysich z guzami HER2-dodatnimi pojedyncza dawka ADC z gemcytabiną — zawierająca około tysiąc razy mniej całkowitej gemcytabiny niż typowe schematy z lekiem wolnym — spowodowała silną i selektywną kontrolę guza. Zachowanie ADC we krwi było bardzo zbliżone do nagiego przeciwciała, a wysokie dawki były dobrze tolerowane u szczurów, co sugeruje szerokie okno bezpieczeństwa.
Co to oznacza dla przyszłego leczenia raka
Dla osób nietechnicznych główna wiadomość jest taka, że praca ta dostarcza nowego, wysoce adaptowalnego chemicznego łącznika, który pozwala przeciwciałom przenosić znacznie szerszy zestaw leków przeciwnowotworowych niż dotąd — i robić to bezpieczniej. Dzięki temu, że leki pozostają przyłączone podczas krążenia i są uwalniane czysto dopiero po tym, gdy ADC zostanie wciągnięty do wnętrza komórki nowotworowej, łączniki fosforamidatowe zwiększają ilość leku docierającą do guza i zmniejszają szkody poboczne dla tkanek zdrowych. Równie ważne jest to, że pozwalają istniejącym silnym małocząsteczkowym lekom — o bardzo różnych kształtach i mechanizmach działania — zostać ponownie wykorzystanymi jako terapie ukierunkowane. To może znacząco poszerzyć ofertę ADC dostępnych dla pacjentów i pomóc w zwalczaniu guzów, które stały się oporne na dzisiejszy ograniczony zestaw ładunków.
Cytowanie: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Słowa kluczowe: koniugaty przeciwciało–lek, dostarczanie leków przeciwnowotworowych, samozniszczalne łączniki, chemia fosforamidatów, celowana chemioterapia