Clear Sky Science · pl
Regiodywergentna i enantioseletywna cyjanacja C–H amin drugorzędowych kontrolowana ligandem
Dlaczego zmiany w małych wiązaniach mają znaczenie dla dużych leków
Wiele najlepiej sprzedających się leków zawiera niewielkie, azotowe fragmenty budulcowe zwane aminami. Subtelne zmiany w sposobie połączenia atomów wokół tych amin mogą zamienić słaby lek w silne, precyzyjne leczenie — albo w substancję nieaktywną, a nawet szkodliwą. W artykule opisano nowy sposób modyfikowania tych fragmentów aminowych wedle woli, pozwalający chemikom wybrać dokładnie, gdzie na cząsteczce ma zachodzić reakcja oraz którą formę lustrzaną uzyskać — oba te aspekty są kluczowe przy projektowaniu bezpieczniejszych i skuteczniejszych leków.
Wybieranie jednego miejsca na zatłoczonej cząsteczce
Aminy w lekach często mają kilka bardzo podobnych wiązań węgiel–wodór (C–H), które zwykle zachowują się niemal identycznie. Chemicy chcieliby wymienić tylko jeden z tych atomów wodoru na użyteczną grupę, taką jak grupa cyjanowa (–CN), nie naruszając reszty cząsteczki. To trudne, ponieważ standardowe reakcje dążą do najbardziej reaktywnego miejsca określonego przez strukturę cząsteczki, a nie przez wybór chemika. Autorzy pracują tutaj na prostych, elastycznych aminach drugorzędowych, które niosą na azocie dwa różne łańcuchy węglowe. Pokazują, że, wychodząc z tej samej aminy, można skierować reakcję na jedno z dwóch sąsiednich miejsc — albo przy małej grupie N‑metylowej (tzw. pozycja α′), albo o jeden atom węgla dalej na drugim łańcuchu (pozycja β) — po prostu zmieniając ligand otaczający katalizator miedziowy.
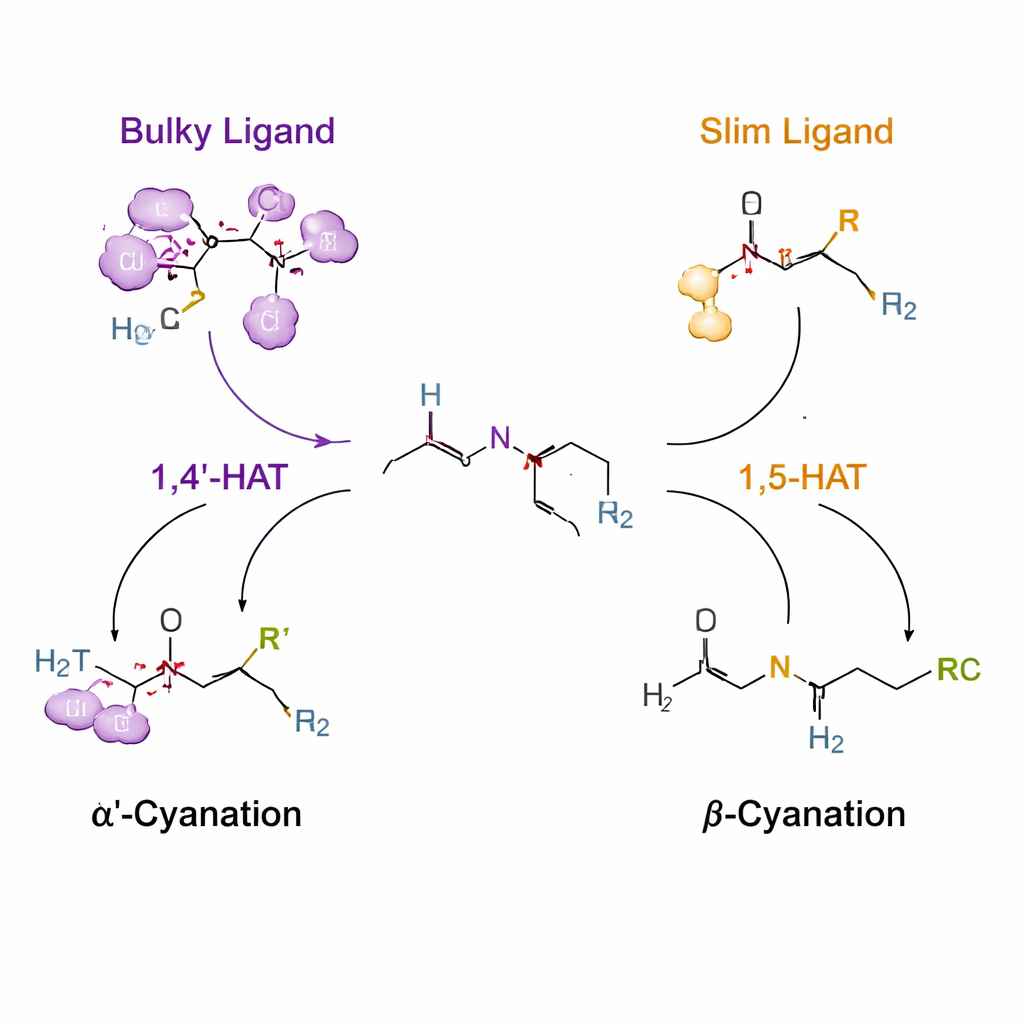
Wykorzystywanie kontrolowanych „skoków” wodoru do kierowania reaktywnością
Kluczowy trik opiera się na procesie zwanym transferem atomu wodoru (HAT), w którym krótkotrwały rodnik z centrum azotowego odrywa wodór z pobliskiego węgla. Zwykle takie rodniki preferują określoną odległość, faworyzując sześcioczłonowe „sięganie” znane jako 1,5‑HAT. Autorzy przyłączają tymczasowy fragment mocznikowy i uchwyt z chlorem do aminy, tak że pod katalizą miedzi tworzy się ten rodnik azotowy i może on zabrać wodór zarówno z pozycji α′, jak i β. Projektując ligandy — organiczne cząsteczki otulające miedź — przeprojektowują otoczenie rodnika. Bardzo masywny ligand (oznaczony L14) przemieszcza układ w stronę nietypowego kroku 1,4′‑HAT, który celuje w grupę N‑metylową, dając selektywną α′‑cyjanację. Węższe ligandy (takie jak L8) pozwalają na konwencjonalną ścieżkę 1,5‑HAT, kierując reakcję na pozycję β.
Od kontroli pozycji do kontroli „ręczności”
Ponad wyborem miejsca reakcji, zespół dąży także do kontroli nad «ręcznością», czyli chiralnością, co jest ważne, ponieważ wiele leków występuje w formach lewo‑ i prawoskrętnej, które różnie zachowują się w organizmie. Aby to osiągnąć, wprowadzają ligandy chiralne — cząsteczki, które same mają określoną «ręczność» — do kompleksu miedziowego. Dwa takie ligandy, L24 i L41, dają dużą preferencję dla jednego enancjomeru, gdy reakcja wprowadza grupę cyjanową na pozycjach β, obejmując zarówno miejsca benzyliczne (przy pierścieniach aromatycznych), jak i allyliczne (przy podwójnych wiązaniach C–C). W szerokim zakresie różnych amin wyjściowych metoda dostarcza produkty β‑cyjanowane z doskonałą selektywnością zarówno miejsca, jak i konfiguracji stereochemicznej, i działa w skali gramowej, co pokazuje, że proces jest praktyczny i solidny do syntezy.
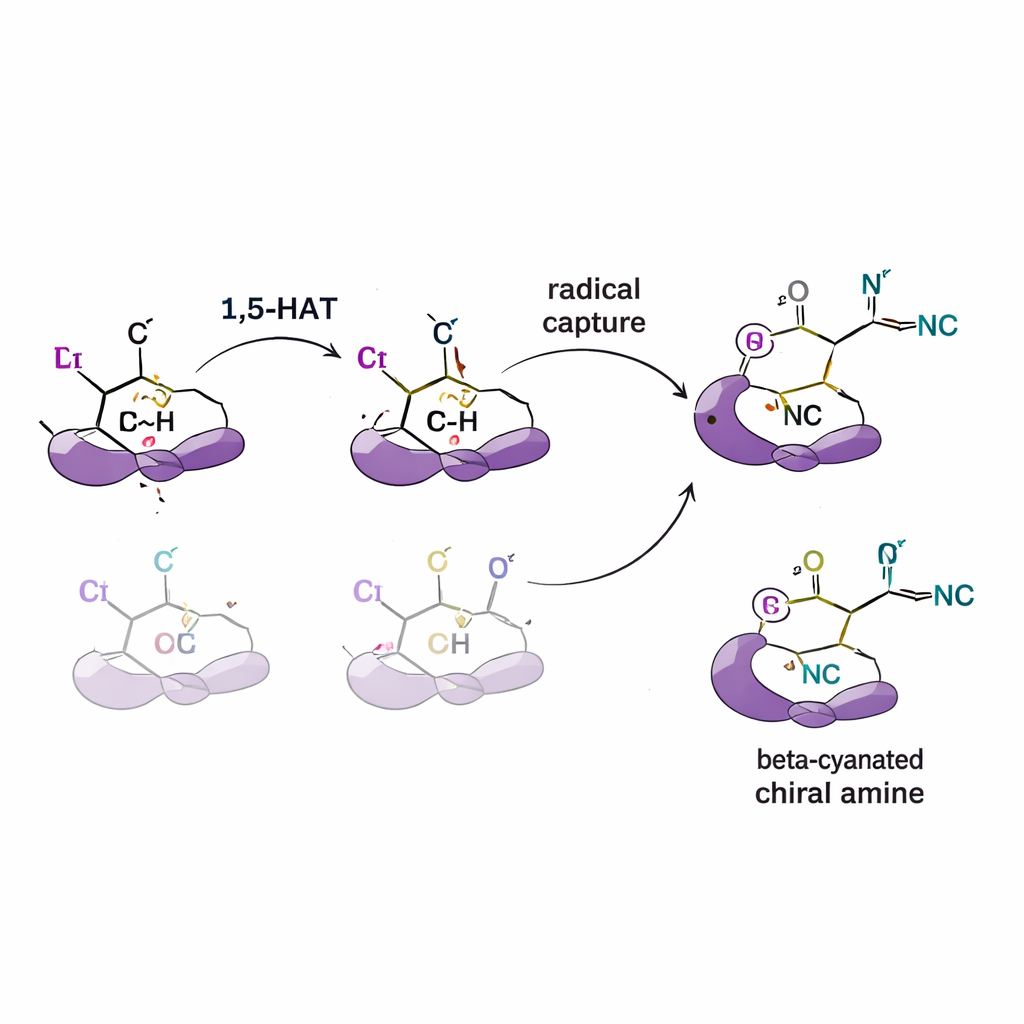
Testowanie mechanizmu stojącego za selektywnością
Aby ustalić, jak powstaje ta kontrola, autorzy przeprowadzają serię eksperymentów mechanistycznych. Poprzez dodanie pułapek na rodniki potwierdzają, że uczestniczą reaktywne pośrednie rodnikowe. Użycie substratów, w których niektóre atomy wodoru zastąpiono deuterem (cięższą formą wodoru), wykazuje efekt izotopowy kinetyczny wskazujący, że etap transferu wodoru jest powolnym i decydującym o selektywności krokiem reakcji. Eksperymenty z znakowaniem pokazują również, że wodór przemieszcza się w pojedynczym, jednokierunkowym kroku, a nie buforuje się między pozycjami. Uzupełniające symulacje komputerowe (teoria funkcjonału gęstości) wspierają te ustalenia, wskazując, że kształt i objętość ligandu zmieniają energię konkurujących ścieżek transferu wodoru oraz sposób, w jaki rodnik następnie łączy się z miedzią i cyjankiem, prowadząc do preferowanego enancjomeru.
Co to oznacza dla przyszłego projektowania leków
Podsumowując, praca wprowadza elastyczną strategię przekształcania powszechnych grup aminowych w dwóch blisko spokrewnionych miejscach, na żądanie, z precyzyjną kontrolą nad stereochemią. Poprzez samą wymianę ligandu na katalizatorze miedziowym chemicy mogą zdecydować, czy umieścić grupę cyjanową na małej jednostce N‑metylowej, czy na sąsiednim atomie węgla innego łańcucha bocznego, i mogą to robić w wielu złożonych, lekopodobnych cząsteczkach. Ponieważ grupy cyjanowe są użytecznymi punktami wyjścia do wielu innych funkcji, to podejście „wybierz‑miejsce” i „wybierz‑rękę” powinno ułatwić odkrywanie i optymalizację nowych leków zbudowanych na tych samych podstawowych szkielecikach aminowych.
Cytowanie: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Słowa kluczowe: funkcjonalizacja amin, transfer atomu wodoru, kataliza miedziowa, enantioselektywna cyjanacja, chemia medyczna