Clear Sky Science · pl
Podwójne lokalizacje genomowe i funkcje regulatorowe genu MBD‑2 z NuRD i bez niego u Caenorhabditis elegans pozbawionego metylacji DNA
Jak maleńkie robaki przepisują zasady kontroli genów
Nasze komórki używają chemicznych znaczników na DNA i białkach, by zapamiętać, które geny mają być aktywne, a które wyciszone. Jeden z najsłynniejszych znaczników, metylacja DNA, jest nieobecny u niektórych zwierząt — mimo to normalnie się rozwijają i rozmnażają. W artykule analizowano, jak niewielki robak Caenorhabditis elegans radzi sobie z regulacją genów bez metylacji DNA, ujawniając zaskakująco elastyczny system awaryjny, który może zmienić nasze spojrzenie na epigenetykę.
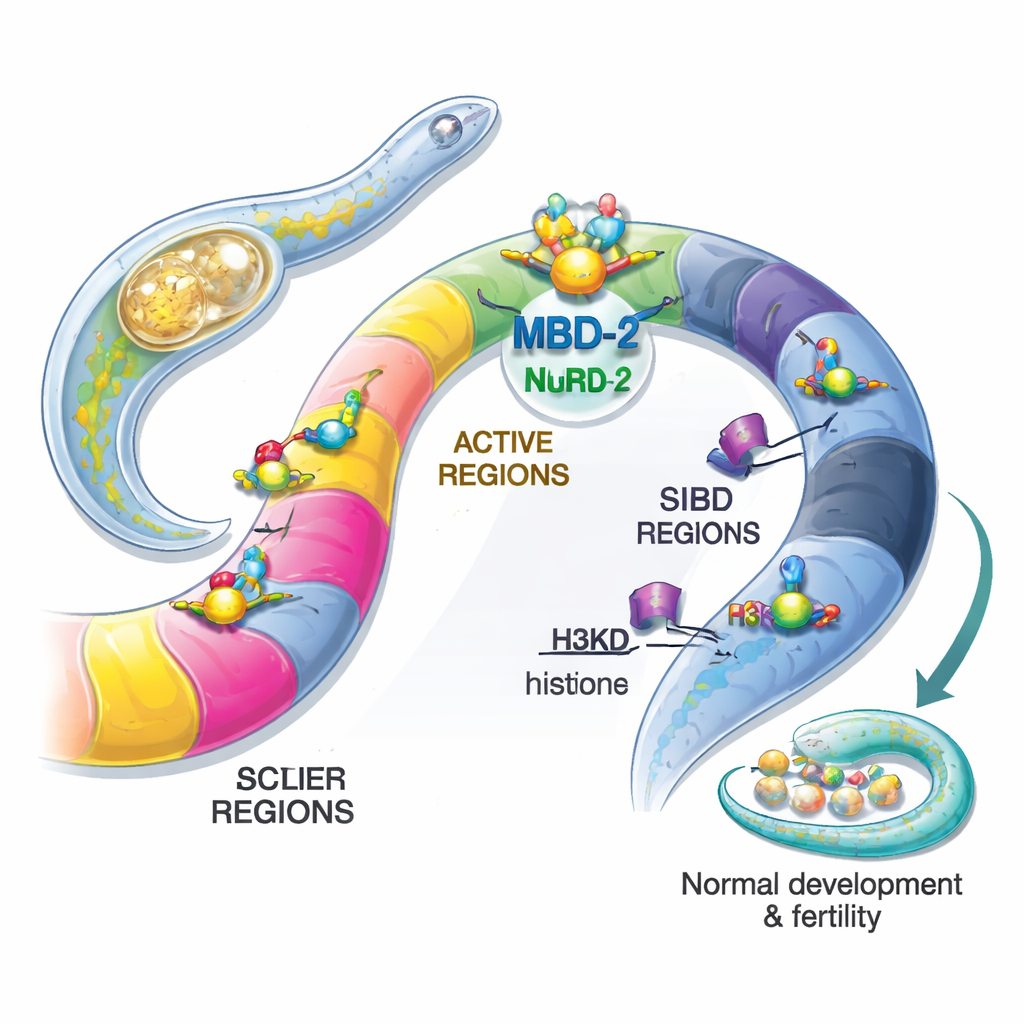
Brak znacznika DNA rodzi poważne pytanie
U ssaków chemiczny znacznik 5‑metylocytozyna (5mC) pomaga uciszać geny podczas rozwoju, inaktywacji chromosomu X i obrony przed transpozonami. Białka zwane MBD2 i MBD3 rozpoznają te znaczniki i rekrutują duży zespół białkowy — kompleks NuRD — który może przebudowywać chromatynę i wyciszać jej fragmenty. Dziwnym trafem wiele bezkręgowców, w tym C. elegans i muszka owocowa, utraciło 5mC i enzymy je tworzące — zachowały jednak białko podobne do MBD2/3. Powstaje zagadka: dlaczego utrzymać „czytnik metylacji DNA” w genomie, który już z niej nie korzysta, i co ono teraz robi?
Białko‑rusztowanie niezbędne robakom
Autorzy skupili się na robaczym odpowiedniku tego białka, nazwanym MBD‑2. W przeciwieństwie do ssaczych krewniaków, robakowe MBD‑2 utraciło klasyczną domenę wiążącą metylowaną cytozynę, ale zachowało elastyczne i skręcone fragmenty, które mogą wiązać inne białka. Oznaczając MBD‑2 markerami fluorescencyjnymi, zespół wykazał, że występuje ono w jądrach niemal wszystkich komórek przez całe życie robaka, co odpowiada szerokiej roli w regulacji genów. Dzięki inżynierii genetycznej stworzono robaki pozbawione MBD‑2 w całości albo pozbawione jedynie regionu koiled‑coil, który pośredniczy w kontakcie z NuRD. Obie mutacje powodowały poważne zaburzenia: zwierzęta były małe, słabiej się poruszały, miały zdeformowane narządy rozrodcze i w dużej mierze były bezpłodne. To dowodzi, że MBD‑2 jest niezbędne dla prawidłowego rozwoju i płodności, nawet przy braku metylacji DNA.
Odbudowa maszyny NuRD w świecie bez metylacji
Aby sprawdzić, czy robacze MBD‑2 wciąż współpracuje z NuRD, autorzy wyizolowali znakowane MBD‑2 z ekstraktów robaków i zidentyfikowali jego partnerów metodą spektrometrii mas. Większość znanych składników NuRD była obecna, co potwierdza, że MBD‑2 działa jako centralne rusztowanie w tym kompleksie, podobnie jak MBD2/3 u ssaków. Po usunięciu regionu koiled‑coil wiele z tych interakcji zanikło, szczególnie z białkami przebudowującymi nukleosomy. Równocześnie duże sekwencjonowanie RNA wykazało, że ponad jedna czwarta wszystkich genów robaka zmieniała aktywność w mutantach MBD‑2, przy czym więcej genów ulegało aktywacji niż wyciszeniu. Wzorzec ten wskazuje, że MBD‑2, często razem z NuRD, zwykle działa jako represor utrzymujący niepożądane geny w ciszy, a jednocześnie pomaga utrzymywać prawidłową aktywność pewnej podgrupy silnie eksprymowanych genów.
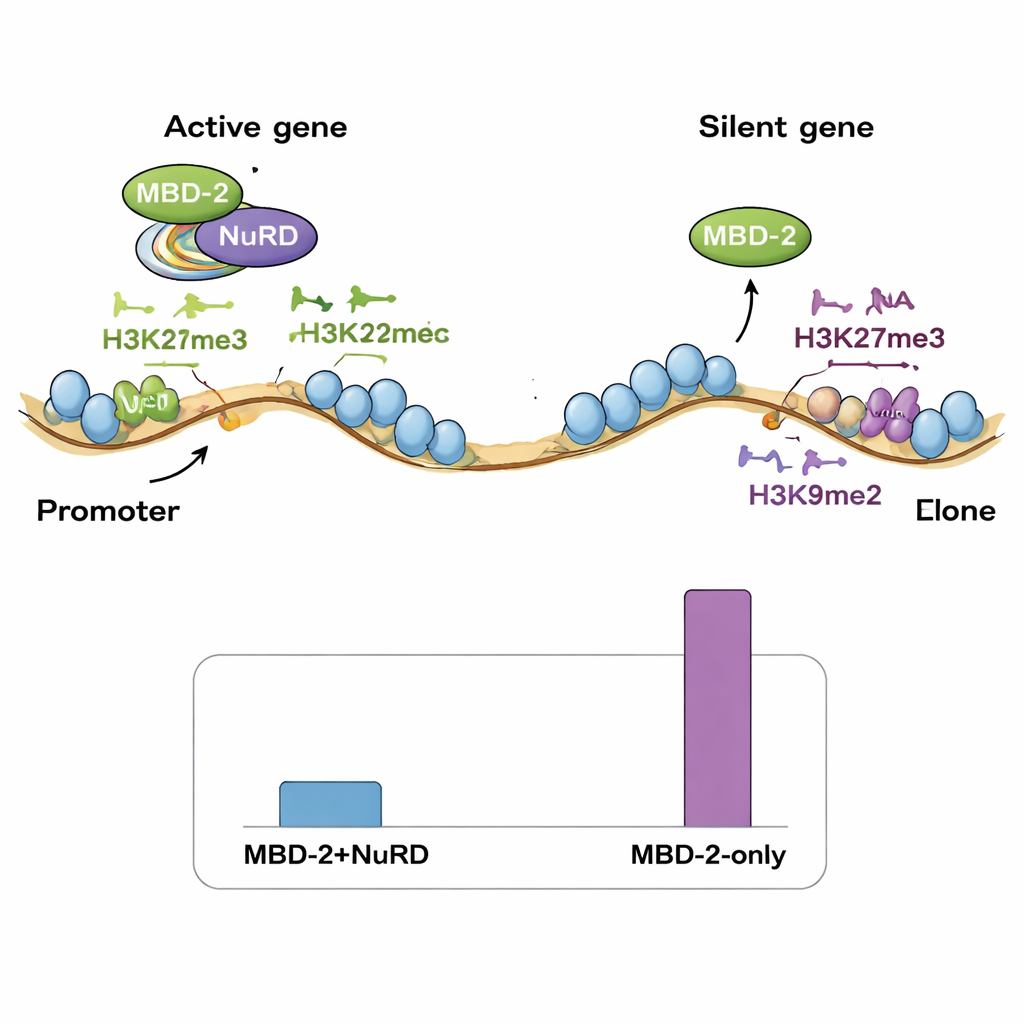
Dwa tryby wiązania w genomie
Następnie zespół zmapował miejsca występowania MBD‑2 w genomie przy użyciu ChIP‑seq i porównał te lokalizacje z istniejącymi mapami składników NuRD oraz różnymi znakami histonowymi. Ku zaskoczeniu tylko niewielka część miejsc MBD‑2 pokrywała się ściśle z białkami NuRD i znakami otwartej, aktywnej chromatyny. Zdecydowana większość miejsc MBD‑2 znajdowała się gdzie indziej — w „ramionach” chromosomów bogatych w represyjne znaki histonowe, takie jak H3K27me3 i H3K9me2/3. Innymi słowy, MBD‑2 wykazuje podwójne zachowanie: w mniejszości miejsc współwędruje z NuRD, by korygować aktywne geny, lecz na znacznie większej liczbie miejsc wiąże się niezależnie w regionach już uciszonych. Również wzorzec wiązania wewnątrz genów ma znaczenie — gdy MBD‑2 skupia się w pobliżu miejsc startu genów, utrata białka ma tendencję do ich aktywacji, natomiast wiązanie głębiej w obrębie ciał genów często wiąże się ze spadkiem ekspresji po usunięciu MBD‑2.
Ewolucyjne zabezpieczenie na wypadek utraty metylacji DNA
Autorzy proponują, że u gatunków, które utraciły metylację DNA, represyjne znaki histonowe — zwłaszcza H3K27me3 — mogły się rozszerzyć, aby wypełnić podobną niszę regulacyjną. Robacze MBD‑2 zdaje się zostać przekształcone: zamiast odczytywać 5mC na DNA, teraz wiąże się z regionami chromatyny oznaczonymi specyficznymi modyfikacjami histonów, przy jednoczesnym kotwiczeniu kompleksu NuRD przez zachowane domeny interakcji białko–białko. Praca ta pokazuje, że starożytne narzędzia uciszania genów mogą zostać przeprojektowane w toku ewolucji: chemiczny znacznik na DNA może zniknąć, ale związane z nim białkowe maszyny przetrwają, przełączając się na alternatywne sygnały. Dla czytelników niebędących specjalistami kluczowy wniosek brzmi: regulacja genów jest niezwykle elastyczna — komórki mogą utracić główny znak epigenetyczny, a mimo to zachować złożoną kontrolę nad tysiącami genów, bardziej polegając na innych znakach chromatyny i wszechstronnej roli białkowych rusztowań, takich jak MBD‑2.
Cytowanie: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Słowa kluczowe: epigenetyka, chromatyna, regulacja genów, C. elegans, modyfikacja histonów