Clear Sky Science · pl
Wysoce dynamiczny mononuklearny enzym żelazowy bez hemu do dwuetapowej biosyntezy izonitrylu
Jak bakterie konstruują egzotyczne narzędzia chemiczne
Izonitryle to małe, ale potężne grupy chemiczne, które zachowują się jak scyzoryk: potrafią wiązać metale, uczestniczyć w różnych reakcjach i często stanowią „głowicę” silnych naturalnych antybiotyków i toksyn. Niektóre patogenne bakterie, w tym sprawca gruźlicy Mycobacterium tuberculosis, przyłączają izonitryle do cząsteczek tłuszczowych, aby pomagać sobie w wykradaniu metali od gospodarza. Artykuł opisuje, jak jeden z ich enzymów, nazwany Rv0097, przeprowadza to wyjątkowo wymagające przekształcenie w dwóch starannie zaplanowanych krokach.
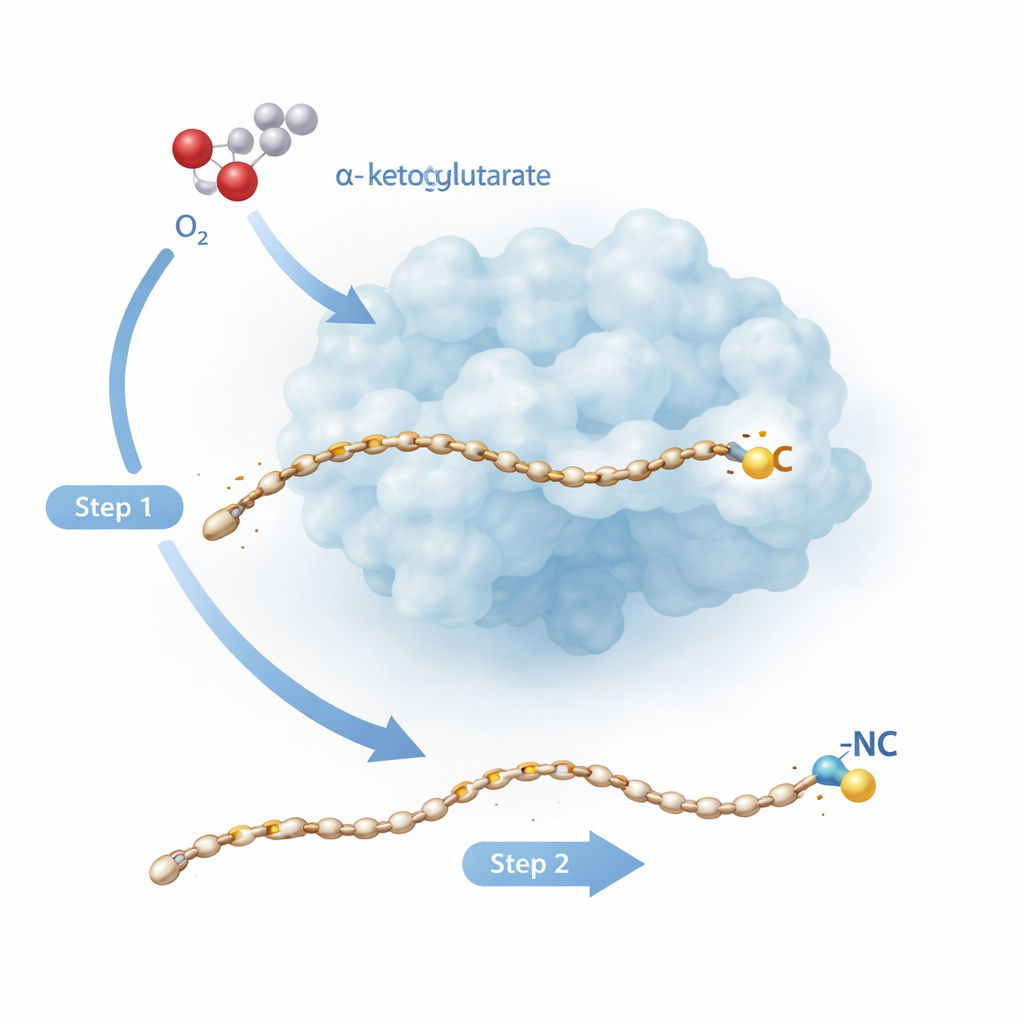
Dwuetapowa przeróbka molekularna
Rv0097 należy do dużej rodziny enzymów zależnych od żelaza, które zazwyczaj wykonują prostsze zadania, takie jak wprowadzenie tlenu w jedno miejsce na cząsteczce. Tutaj zadanie jest trudniejsze: zaczynając od bloku budulcowego „glicyl–kwas tłuszczowy”, enzym musi utworzyć nową grupę izonitrylową, przy czym oba kluczowe atomy — węgiel i azot — pochodzą z tej samej małej reszty glicyny. Wcześniejsze badania nad spokrewnionym enzymem ScoE sugerowały, że nie da się tego zrobić jednym ruchem. Zamiast tego potrzebne są dwa oddzielne „półcykle” reakcyjne, zasilane przez gatunek żelazo–tlen powstający, gdy enzym rozrywa pomocniczą cząsteczkę α‑ketoglutaran i łączy ją z tlenem z powietrza. Nowe badanie skupia się na enzymie gruźlicy Rv0097, aby zobaczyć, w rozdzielczości atomowej, jak enzym łączy te dwa rodnikowe kroki na tym samym substracie, nie tracąc kontroli.
Zamrażanie enzymu w akcji
Za pomocą krystalografii rentgenowskiej badacze uchwycili szesnaście wysokorozdzielczych migawek Rv0097 w różnych stanach: pusty, związany z substratem tłuszczowym (dziesięciowęglowa cząsteczka nazwana CADA), związany z pomocnikiem α‑ketoglutaranem oraz w kombinacjach naśladujących ulotne pośrednie produkty reakcji. Struktury te pokazują, że Rv0097 ma podzieloną osobowość. W spoczynku jego centrum aktywne jest w dużej mierze zamknięte, a kluczowy aminokwas (fenyloalanina 102) przechodzi między dwiema orientacjami, które utrzymują suchą kieszeń dla długiego ogona tłuszczowego, przygotowaną do hydrofobowego wiązania. Gdy CADA wiąże się, reszta ta zatrzaskuje się w jednej orientacji, a polarna „głowa” substratu jest zakotwiczona przez naładowane łańcuchy boczne, podczas gdy tłusty ogon układa się w dopasowanym tunelu. Mutacje w tym parującym zamku reszt (F102 i pobliskie G204) albo blokują kieszeń, albo wpuszczają za dużo wody, co ostro zmniejsza aktywność i zmienia preferencje enzymu względem długości łańcuchów.
Ruchome klapy i dynamiczne pętle
Powyżej kieszeni substratowej Rv0097 zachowuje się jak mała maszyna z ruchomymi drzwiami. Zespół zaobserwował konformacje „otwartą” i „zamkniętą”, w których dwie przypominające klapy regiony rozchylają się lub zbliżają nad centrum aktywnym. Otwarcie odsłania centrum żelazowe i tworzy ścieżkę dla α‑ketoglutaranu i substratu; zamknięcie osłania chemię przed otaczającą wodą, gdy reakcja już przebiega. Dwie elastyczne pętle powierzchniowe, nazywane pętlą His i pętlą Arg od histydyny i argininy, które niosą, działają jako dodatkowa brama. W niektórych strukturach pętle te odchylają się do wewnątrz, tak że reszta argininy może złapać α‑ketoglutaran; w innych odchylają się na zewnątrz, najwyraźniej tworząc boczny kanał, przez który mogą opuszczać zużyte fragmenty pomocnika (szczawian i dwutlenek węgla) i przez który świeży α‑ketoglutaran może wejść do drugiego kroku — a wszystko to, podczas gdy pochodny substratu pozostaje zaciskany na miejscu.
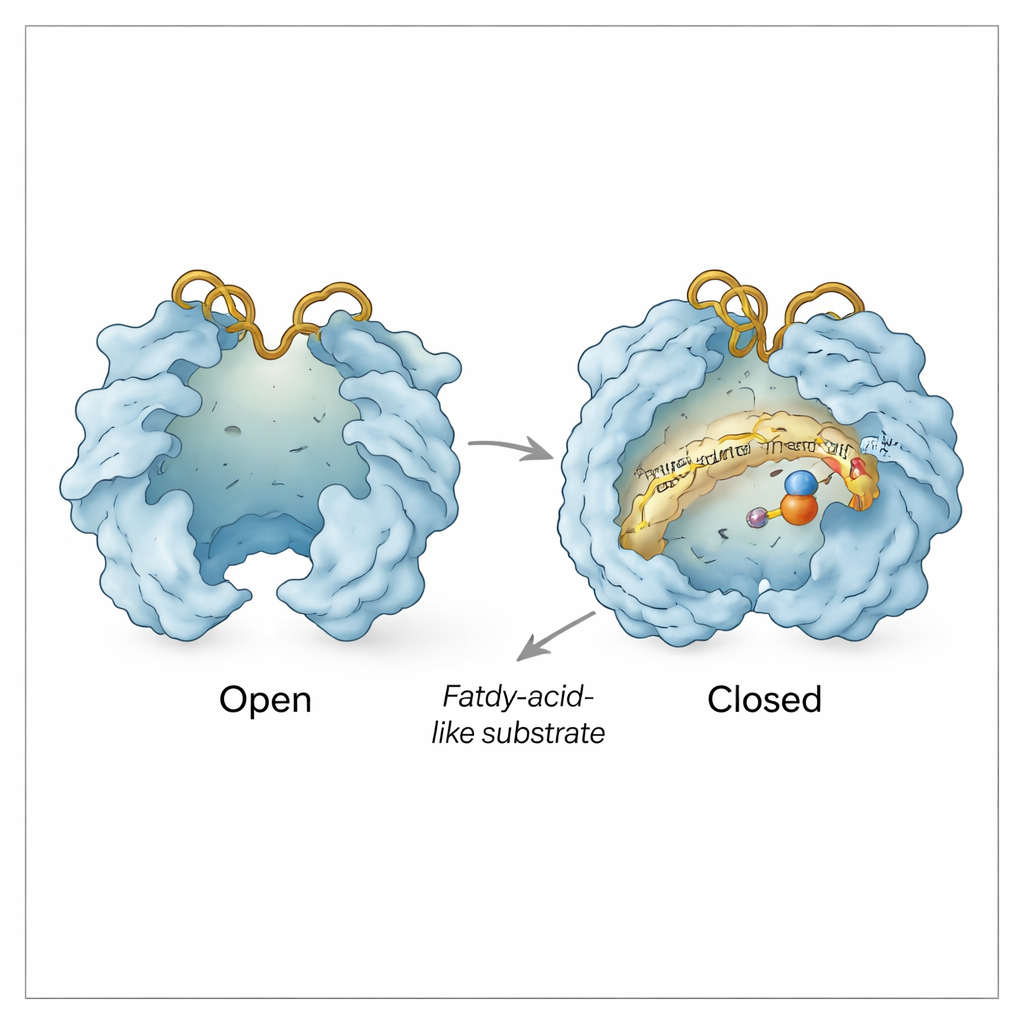
Ochrona kruchego pośredniego produktu
Analizy biochemiczne wspierają ten obraz strukturalny. Pierwsza połowa reakcji przekształca CADA w wysoce reaktywny pośredni iminy, który szybko rozpadłby się, gdyby wydostał się do roztworu. Poprzez chemiczne wychwycenie produktu rozpadu autorzy pokazują, że większość tego pośredniego związku wykrywa się tylko wtedy, gdy enzym nadal jest obecny, co sugeruje, że pozostaje związana i chroniona wewnątrz Rv0097 między dwiema połowami reakcji. Struktury wyjaśniają, jak: subtelne przemieszczenia pętli His i Arg, wraz z niewielkimi przesunięciami pobliskich reszt, wydają się uszczelniać pośredni związek w osłoniętej wnęce, jednocześnie umożliwiając wymianę małych cząsteczek, takich jak α‑ketoglutaran, szczawian i dwutlenek węgla, przez kontrolowane kanały.
Dlaczego to ma znaczenie dla gruźlicy i nie tylko
Razem te wyniki ukazują Rv0097 jako wysoce dynamiczną, jednostkową linię montażową, która używa żelazowej chemii dwukrotnie z rzędu na tym samym substracie, nigdy nie uwalniając niebezpiecznego półproduktu. Dla bakterii gruźlicy ta precyzja jest podstawą wytwarzania cząsteczek ozdobionych izonitrylem, które pomagają im pozyskiwać niezbędne metale w organizmie, a badania genetyczne wskazują, że szlak ten jest ważny dla ich przetrwania podczas infekcji. Dla chemików i projektantów leków praca ta oferuje plan działania do inżynierii pokrewnych enzymów w celu budowy nowych związków zawierających izonitryl i sugeruje, że zakłócanie ruchomych klap i wrót Rv0097 może być sposobem na opracowanie nowych antybiotyków.
Cytowanie: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Słowa kluczowe: biosynteza izonitrylu, enzym żelazowy bez hemu, Mycobacterium tuberculosis, dynamika enzymu, naturalne produkty chelatujące metale