Clear Sky Science · pl
Zakłócenie homeostazy żelaza uwrażliwia raka trzustki na nieodwracalną elektrooporację
Włączenie elektryczności i żelaza przeciwko śmiertelnemu nowotworowi
Rak trzustki jest jednym z najtrudniejszych nowotworów do leczenia, a nawet agresywne terapie miejscowe często nie zapobiegają nawrotom. W tym badaniu zbadano nowy sposób, by istniejącą procedurę — nieodwracalną elektrooporację, która niszczy guzy przy pomocy krótkich, silnych impulsów elektrycznych — uczynić skuteczniejszą i bezpieczniejszą. Poprzez sprytne zakłócenie sposobu, w jaki komórki nowotworowe gospodarują żelazem, badacze pokazują, że można doprowadzić ocalałe komórki do destrukcyjnej formy śmierci, co potencjalnie zmniejsza ryzyko nawrotu guza.
Dlaczego same impulsy elektryczne nie wystarczają
Nieodwracalna elektrooporacja (IRE) leczy guzy przez wprowadzenie cienkich elektrod do wnętrza lub wokół nowotworu i wystrzelenie szybkich, wysokonapięciowych impulsów. Impulsy te tworzą trwałe otwory w błonach komórkowych, zabijając wiele komórek nowotworowych i wywołując odpowiedź immunologiczną. Pole elektryczne nie jest jednak idealnie jednorodne. Obszary, które otrzymują nieco słabsze impulsy, mogą pozostawić przy życiu komórki nowotworowe, a te ocalałe mogą zasiedlać nowy guz. Gdy zespół szczegółowo przeanalizował komórki raka trzustki i guzy myszy wystawione na podśmiertelne pole elektryczne, odkrył, że zamiast umierać przez proces zależny od żelaza zwany ferroptozą, komórki te uruchamiają szeroki program obrony antyoksydacyjnej. Kluczowe geny ochronne, w tym te pomagające neutralizować uszkodzenia związane z żelazem, były aktywowane, co pozwalało komórkom przetrwać i odzyskać funkcję.
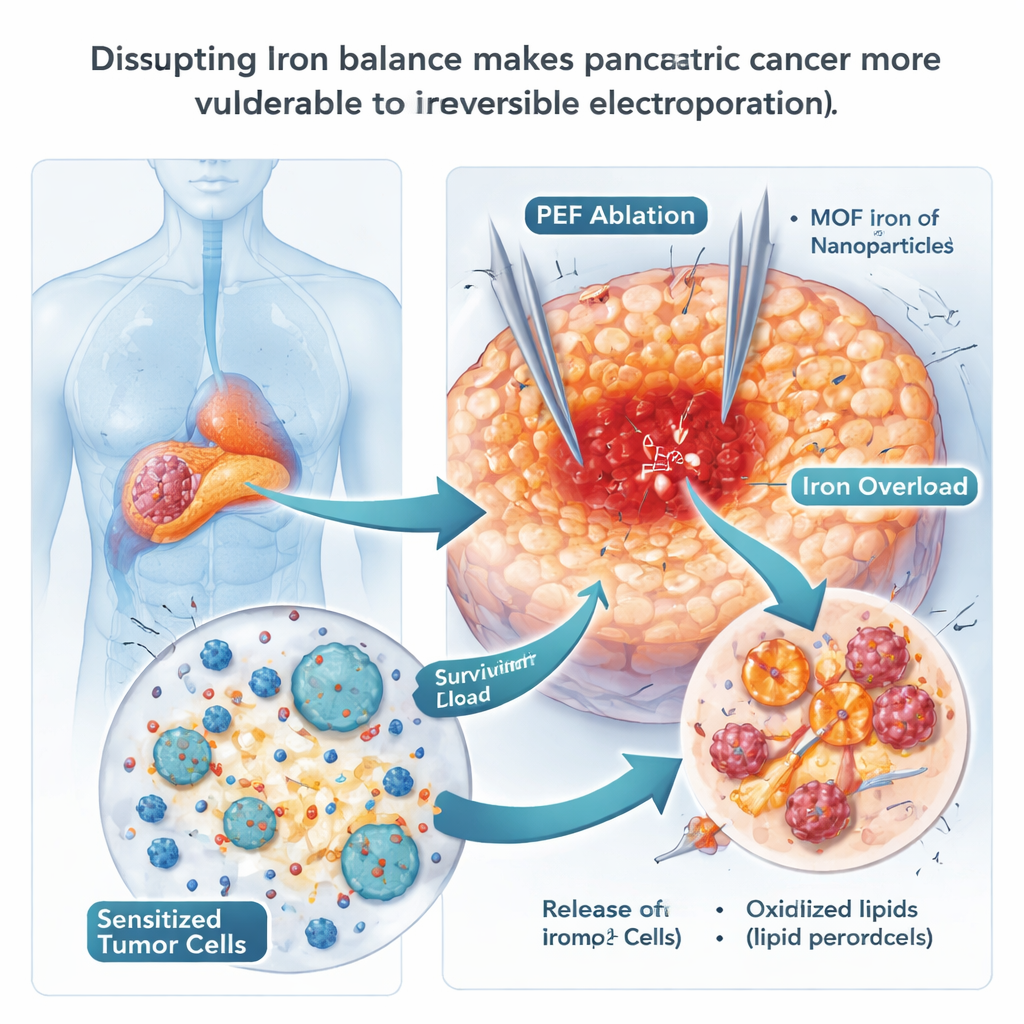
Wykorzystanie nanocząstek żelaza do pchnięcia komórek ku destrukcji
Ponieważ ferroptoza zależy od żelaza, naukowcy sprawdzili, czy bogate w żelazo nanocząstki mogą zmusić komórki nowotworowe do przekroczenia progu śmierci. Użyli specjalnie zaprojektowanych cząstek z metalo‑organicznej ramy zawierających żelazo (MOF‑Fe), które szybko uwalniają żelazo we wnętrzu kwaśnych pęcherzyków komórkowych. W hodowlach komórkowych komórki raka trzustki, które wchłonęły te cząstki, akumulowały wolne żelazo i utlenione tłuszcze w błonach — klasyczne cechy ferroptozy — i tworzyły znacznie mniej kolonii. U myszy połączenie MOF‑Fe z IRE opóźniało odrost guza dłużej niż każde z tych leczeń osobno, a guzy wykazywały więcej oznak uszkodzeń oksydacyjnych. Jednak korzyść ta była tymczasowa: po około trzech tygodniach guzy zaczęły się odbijać, co sugeruje, że nowotwór znalazł sposób na adaptację do nadmiaru żelaza.
Atak na „sejf” żelaza komórki
Aby zrozumieć tę oporność, zespół przeanalizował, które białka zmieniały się po leczeniu MOF‑Fe. Wyróżniał się ciężki łańcuch ferrytyny 1 (FTH1), część kompleksu magazynującego żelazo w komórce — molekularny odpowiednik ognioodpornego sejfu na nadmiar żelaza. Gdy poziomy FTH1 były eksperymentalnie podnoszone, komórki nowotworowe stawały się bardziej odporne na ferroptozę; gdy FTH1 obniżano, stawały się bardziej podatne. Wskazywało to na FTH1 jako główną tarczę przeciwko śmierci zależnej od żelaza. Badacze następnie stworzyli zaprojektowaną cząsteczkę, C20U4V, zbudowaną z kwasu arachidonowego (wysoce podatnego na utlenianie tłuszczu) połączonego ze szkieletem „PROTAC”, który kieruje wybrane białka do komórkowego systemu degradacji. W obecności MOF‑Fe C20U4V wiązał ferrytynę i rekrutował ją do znakowania i niszczenia, gwałtownie obniżając poziomy FTH1 i uniemożliwiając komórce bezpieczne zamknięcie żelaza.
Od hodowli komórek do mini‑guzów i myszy
Gdy MOF‑Fe i C20U4V zastosowano razem, komórki raka trzustki wykazywały wyższy stres oksydacyjny, więcej uszkodzonych tłuszczów błonowych, chore mitochondria i znacznie zmniejszoną zdolność do odrastania. Ta synergia pojawiła się również w trójwymiarowych organoidach pochodzących od pacjentów — małych struktur przypominających guzy hodowanych z materiału pacjentów — gdzie para leków doprowadziła do kurczenia się rozmiaru i liczby organoidów. Ponieważ C20U4V jest oleisty i nierozpuszczalny w wodzie, zespół zapakował go w małe micelle wrażliwe na reaktywne formy tlenu (M‑C20U4V), które krążą we krwi i mogą uwalniać lek w zestresowanej, uszkodzonej tkance guza. W modelach mysich z guzami umieszczonymi pod skórą i w samej trzustce potrójne połączenie IRE, MOF‑Fe i M‑C20U4V zmniejszało guzy znacznie skuteczniej i wydłużało przeżycie w porównaniu z każdym leczeniem pojedynczym lub podwójnym. Leczone guzy miały mniej dzielących się komórek, więcej markerów ferroptozy i silniejszy naciek komórek T oraz innych komórek układu odpornościowego, co wskazuje, że strategia nie tylko bezpośrednio zabija komórki nowotworowe, lecz także pomaga układowi odpornościowemu rozpoznać i zaatakować guz.
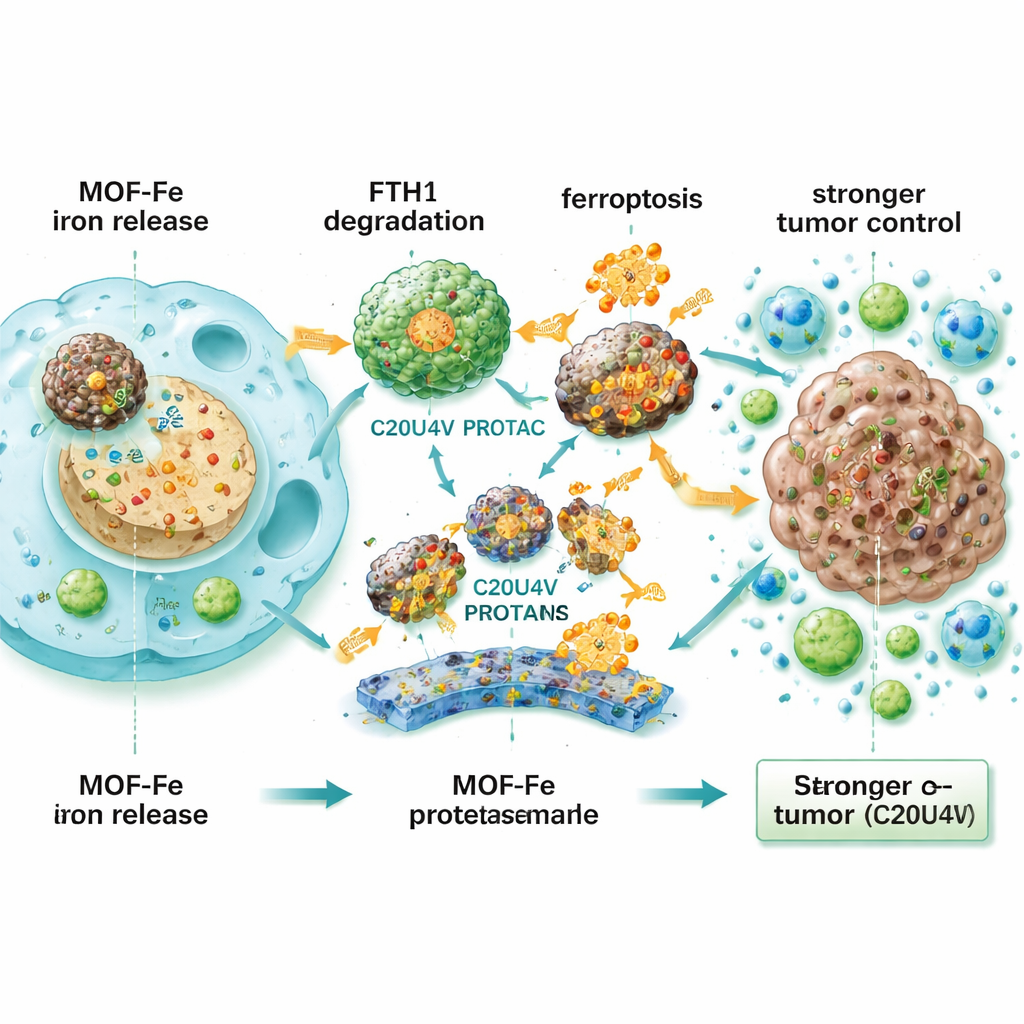
Co to może znaczyć dla pacjentów
Dla osoby nietechnicznej kluczowa idea jest prosta: guzy trzustki często uciekają po ablacji impulsami elektrycznymi, ponieważ niektóre komórki nowotworowe przeżywają i szybko się adaptują. Ta praca pokazuje, że załadowanie tych komórek żelazem i równoczesne dezaktywowanie ich „sejfu” na żelazo może zmusić je do samozniszczenia, któremu trudno się oprzeć. Chociaż podejście to jest wciąż w fazie eksperymentalnej i wymaga obszernego testowania pod kątem bezpieczeństwa i praktyczności u ludzi, sugeruje, że precyzyjne manipulowanie sposobem, w jaki guzy obchodzą się z podstawowym pierwiastkiem jakim jest żelazo, może zamienić niedoskonałe leczenie miejscowe w bardziej decydujący cios przeciw jednemu z najbardziej śmiertelnych nowotworów.
Cytowanie: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Słowa kluczowe: rak trzustki, nieodwracalna elektrooporacja, ferroptoza, nanocząstki żelaza, terapia PROTAC