Clear Sky Science · pl
HIF podtrzymuje obwód regulacji transkrypcyjnej ekspresji EPAS1 w raku płaskonabłonkowym nerki
Dlaczego rak nerki zasługuje na bliższą uwagę
Rak jasnokomórkowy nerki jest najczęstszą postacią raka nerki, a wielu pacjentów otrzymuje obecnie leki blokujące białko zwane HIF‑2α. Te leki mogą zmniejszać guzy, ale nie działają równie dobrze u wszystkich. W badaniu postawiono proste, ale istotne pytanie: co sprawia, że niektóre guzy nerek produkują tak dużo HIF‑2α i czy zrozumienie tego „włącznika” pozwoli lepiej przewidzieć, kto najbardziej skorzysta z leczenia i jak projektować nowe terapie?
Czujnik tlenu, który zbuntował się
Zdrowe komórki nerek korzystają z białka zabezpieczającego nazwanego VHL, które utrzymuje czynniki reagujące na tlen, znane jako HIF, pod ścisłą kontrolą. Gdy tlenu jest dużo, VHL oznacza białka HIF do zniszczenia, zapobiegając włączaniu genów sprzyjających tworzeniu naczyń krwionośnych i podziałom komórek. W raku jasnokomórkowym nerki VHL jest zwykle utracone lub uszkodzone. W efekcie jeden z członków rodziny HIF, HIF‑2α (kodowany przez gen EPAS1), unika degradacji i gromadzi się. Wcześniejsze badania wykazały, że wysoka aktywność HIF‑2α wiąże się z szybszym wzrostem guza i gorszymi wynikami, oraz że blokowanie HIF‑2α może spowolnić lub zatrzymać guzy u niektórych pacjentów. Jednak molekularne kroki zwiększające aktywność genu EPAS1 w guzach nerek nie były dobrze poznane.
Ukryty przełącznik DNA dla genu nowotworowego
Korzystając z próbek guzów od pacjentów, danych jednokomórkowych i modeli komórek nowotworowych, autorzy pokazują, że mRNA HIF‑2α jest wyraźnie wyższe w guzach raka jasnokomórkowego niż w normalnej tkance nerki czy innych typach guzów nerek. Następnie skanują region EPAS1 w genomie pod kątem chemicznych i strukturalnych znaków sygnalizujących aktywne DNA regulacyjne. Odkrywa to potężny enhancer — rodzaj przełącznika genowego działającego na odległość — zlokalizowany około 70 000 par zasad powyżej EPAS1, który jest specyficznie aktywny w guzach jasnokomórkowych. W komórkach nowotworowych chromatyna w tym enhancerze jest otwarta, ozdobiona znakami aktywacji i fizycznie pętlami łączy się z promotorem EPAS1, podczas gdy w normalnych komórkach kanalików nerkowych ten region jest w dużej mierze cichy. Aktywność tego enhancera koreluje z wyższymi poziomami EPAS1 w dużych zbiorach danych nowotworowych. 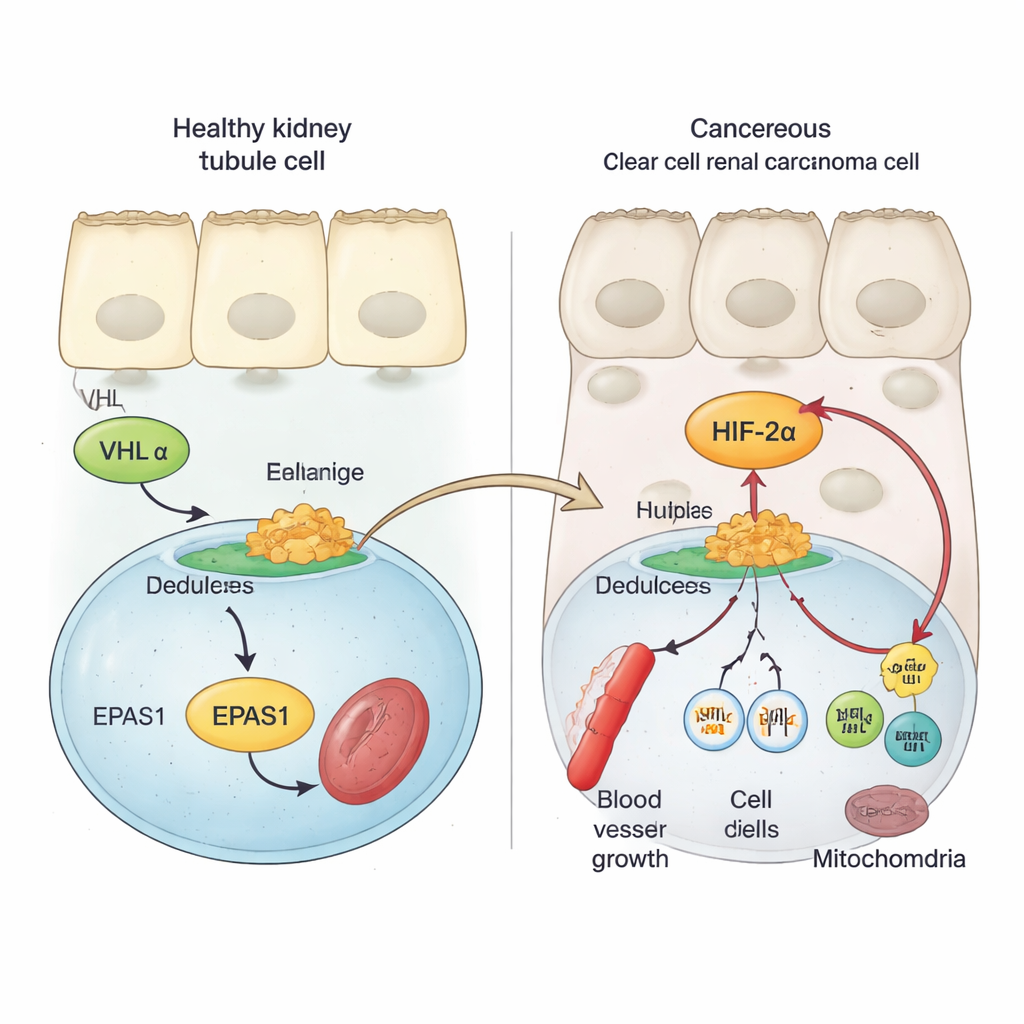
Samo-wzmacniająca pętla napędzana przez czynniki tożsamości nerek
Badanie wykazuje, że białka HIF robią więcej niż reagują na niski poziom tlenu — w rzeczywistości pomagają napędzać własną produkcję. Gdy badacze przywracają VHL lub usuwają kluczowe białko współpracujące z HIF (HIF‑1β), poziomy EPAS1 spadają, a enhancer staje się mniej dostępny. Bezpośrednie mapowanie kontaktów białko–DNA pokazuje, że HIF wiąże się z dwoma regionami enhancera powyżej EPAS1, w tym z enhancerem specyficznym dla raka jasnokomórkowego. W komórkach nowotworowych nerek enhancer ten jest także zajęty przez PAX8 i HNF‑1β, czynniki transkrypcyjne definiujące tożsamość komórek nerek i znane z wspierania wzrostu guza. Zakłócenie PAX8 lub HNF‑1β albo mutacja ich miejsc wiązania w enhancerze zmniejsza RNA i białko HIF‑2α oraz osłabia aktywność enhancera. Razem te ustalenia ujawniają obwód auto-regulacyjny: HIF‑2α, współdziałając z czynnikami linii nerkowej, zwiększa aktywność enhancera EPAS1, co z kolei napędza większą produkcję HIF‑2α.
Ryzyko genetyczne i zachowanie guza zbiegają się w tym samym obwodzie
Region EPAS1 od dawna był wskazywany w badaniach całego genomu jako „hotspot” ryzyka raka nerki, z pewnymi odziedziczonymi wariantami powiązanymi z wyższą zapadalnością na raka i z mutacjami VHL w guzach. Łącząc dane genetyczne z pomiarami ekspresji genów, autorzy pokazują, że osoby noszące wysokiego ryzyka wersję kluczowego wariantu EPAS1 mają tendencję do wyższych poziomów HIF‑2α w swoich guzach — a nawet w normalnych komórkach kanalików nerkowych, gdy HIF jest eksperymentalnie stabilizowany. Sugeruje to, że odziedziczone różnice w DNA mogą modulować, jak silnie enhancer reaguje, „primując” niektóre nerki do silniejszego zwiększenia HIF‑2α po utracie VHL. Eksperymenty w komórkach glejaka pokazują, że ten sam enhancer może być także zaangażowany w niektórych nowotworach mózgu, co sugeruje, że ten moduł regulacyjny może być wykorzystywany również w innych nowotworach, gdzie HIF‑2α odgrywa ważną rolę. 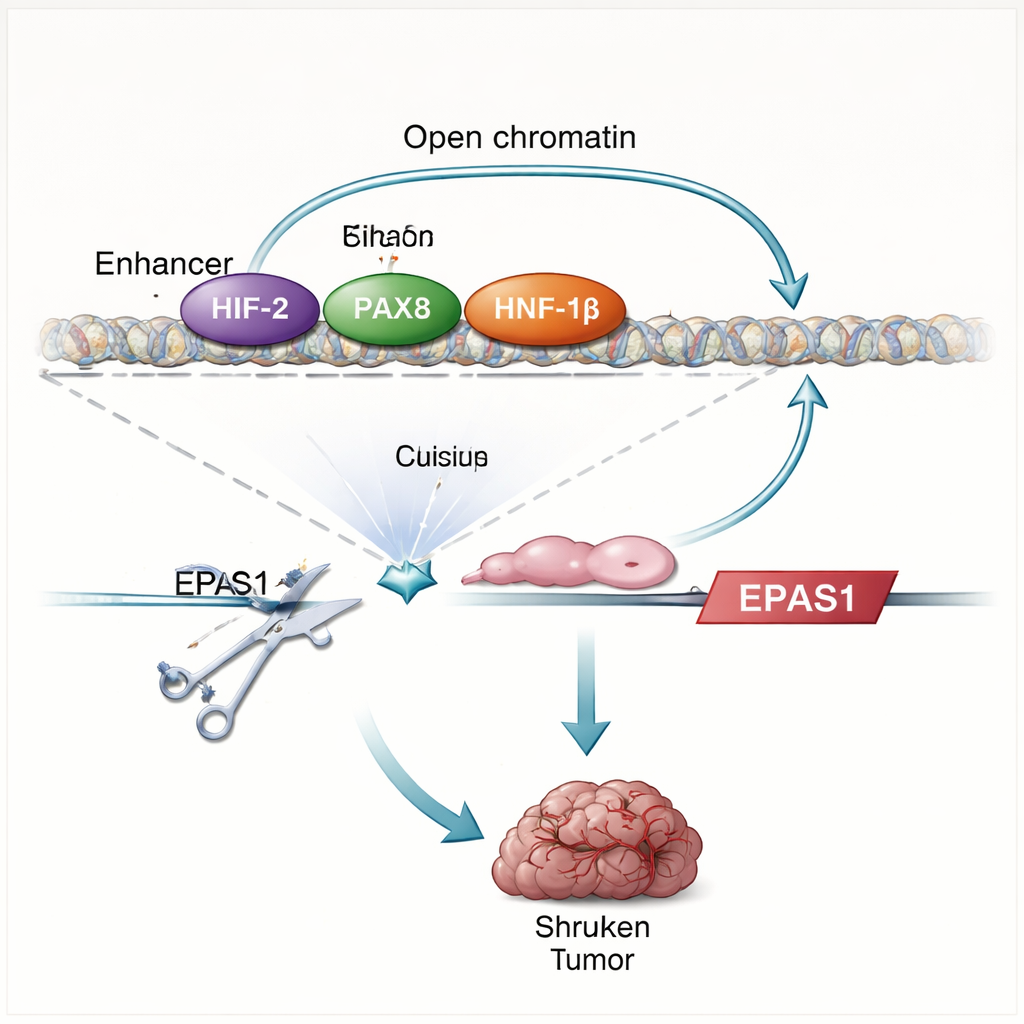
Przerwanie pętli, by zatrzymać wzrost guza
Aby sprawdzić, jak kluczowy jest ten enhancer, zespół używa edycji genomu CRISPR do uszkodzenia motywów wiążących HIF w jego obrębie w liniach komórkowych raka nerkowego i świeżych komórkach guzów pacjentów. To cięcie zmniejsza RNA HIF‑2α o około jedną trzecią do połowy, obniża poziomy dobrze znanych genów będących celami HIF‑2α, takich jak CCND1 i VEGFA, oraz osłabia szerszy program genów odpowiedzi na hipoksję. Gdy zmodyfikowane komórki są wszczepiane do myszy, w dużej mierze nie tworzą guzów, w ostrym kontraście do komórek kontrolnych. Wzorzec zmian genowych po zakłóceniu enhancera wiernie odzwierciedla efekty bezpośredniego blokowania HIF‑2α lekiem klinicznym, podkreślając, że ten pojedynczy element DNA jest głównym motorem ścieżki HIF‑2α w tych nowotworach.
Co to oznacza dla pacjentów i terapii
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że autorzy odkryli samo-wzmacniający się przełącznik DNA, który utrzymuje włączone jedno z głównych białek sprzyjających nowotworowi, HIF‑2α, w guzach raka jasnokomórkowego nerki. Ten przełącznik zależy zarówno od utraty hamulca bezpieczeństwa VHL, jak i od nerkowo-specyficznych białek pomocniczych, i jest modulowany przez odziedziczone warianty genetyczne. Ponieważ enhancer jest wysoce aktywny w wielu guzach jasnokomórkowych i ściśle związany z siłą działania ścieżki HIF‑2α, pomiar jego aktywności — lub bezpośrednie ukierunkowanie na niego — może pomóc w identyfikacji pacjentów, którzy najwięcej skorzystają z obecnych inhibitorów HIF‑2α, i zaoferować nowe sposoby wyłączenia tej ścieżki, gdy guzy stają się oporne na leki.
Cytowanie: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Słowa kluczowe: rak jasnokomórkowy nerki, HIF-2α, enhancer EPAS1, mutacja VHL, genetyka raka nerki