Clear Sky Science · pl
Atroposelektywna przerywana reakcja CuAAC z użyciem cyklicznych diaryliodoniowych
Dlaczego ta nowa chemia ma znaczenie
Chemicy od dawna polegają na prostej reakcji „click”, która szybko i czysto łączy elementy konstrukcyjne molekuł — trik wspierający wszystko, od odkrywania leków po materiały samonaprawiające się. Ten artykuł opisuje sprytne urozmaicenie klasycznej reakcji click, które pozwala badaczom budować bardziej złożone, trójwymiarowe molekuły z precyzyjną „ręcznością” — struktury cenione w nowoczesnych lekach i zaawansowanych materiałach.
Nadanie klasycznej reakcji click nowej roli
Punktem wyjścia jest miedziowa katalizowana cykloadycja azyd–alkin, często nazywana po prostu CuAAC. Łączy ona dwa małe składniki — azyd i alkin — w pięcioczłonowy pierścień zwany triazolem w łagodnych warunkach i z niezwykłą niezawodnością. Tradycyjnie, po utworzeniu pierścienia triazolowego przy udziale miedzi reakcja na tym się kończy. W ostatnich latach jednak chemicy nauczyli się „przerywać” ten proces, chwytając ulotny miedź–triazolowy pośrednik przy pomocy trzeciego partnera, by otrzymać bardziej rozbudowane produkty. Do tej pory takie przerwania nie potrafiły ogólnie kontrolować chiralności molekularnej, co ograniczało ich użyteczność przy tworzeniu wyrafinowanych, chiralnych związków.
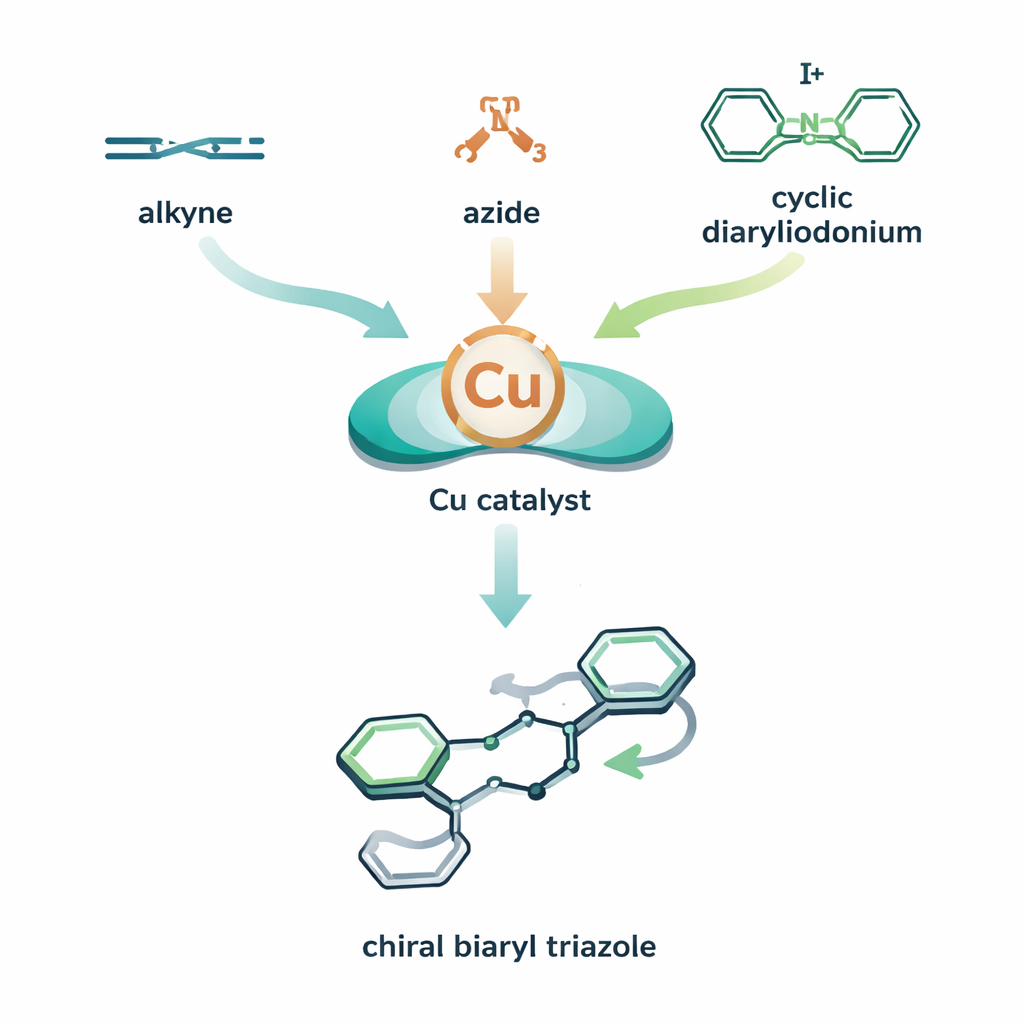
Trójskładnikowa układanka molekularna z obrotem
Autorzy łączą dwa miedziowe cykle reakcyjne w jeden, skoordynowany proces. W ich koncepcji katalizator miedzi najpierw pomaga alkinowi i azydowi utworzyć miedź–triazolowy pośrednik. Zanim pośrednik zostanie zneutralizowany, wprowadza się trzeci składnik — pierścieniową, bardzo reaktywną cząsteczkę zawierającą jod, zwaną cyklicznym diaryliodonium. Miedź wstawia się w ten pierścień i następnie go otwiera, przyłączając jeden z pierścieni aromatycznych do triazolu. Wynikiem jest biarylowy triazol: dwa układy pierścieniowe połączone wokół wiązania, które może funkcjonować jako oś chiralna, podobnie jak śmigło mogące skręcać w lewo lub w prawo. Poprzez sparowanie miedzi z starannie dobranym ligandem chiralnym, zespół faworyzuje powstawanie jednego skrętu znacznie częściej niż drugiego, osiągając wysoką atroposelektywność (kontrolę, która „osiowa ręka” powstaje).
Testowanie elastyczności i niezawodności metody
Aby ocenić, jak ogólna może być ta reakcja, badacze systematycznie zmieniali każdy z trzech elementów budulcowych. Pokazali, że wiele różnych alkinów, w tym te z pierścieniami elektrono-donorowymi, elektronowo-akceptorowymi oraz heteroaromatycznymi, może uczestniczyć, zachowując dobre wydajności i wyraźne uprzywilejowanie jednej formy chiraloicznej. Niektóre masywne podstawienia poprawiały selektywność, lecz mogły obniżać wydajność, ujawniając kompromis między utrudnieniem sterycznym a efektywnością. Partnerzy azydowi najlepiej sprawdzali się, gdy pochodziły z prostych estrów lub amidów albo z pozycji benzylowych; szeregi takich azydów dostarczały silnie wzbogaconych produktów chiralnych. Składnik cyklicznego diaryliodonium również można było dostroić: niektóre podstawienia zachowywały zarówno wydajność, jak i selektywność, podczas gdy inne, zwłaszcza w pobliżu reaktywnego centrum jodowego, spowalniały reakcję lub obniżały jej osiągi. Ogólnie badanie dostarczyło szerokiej kolekcji nowych atropisomerycznych biarylowych triazoli dostępnych jednym etapem.
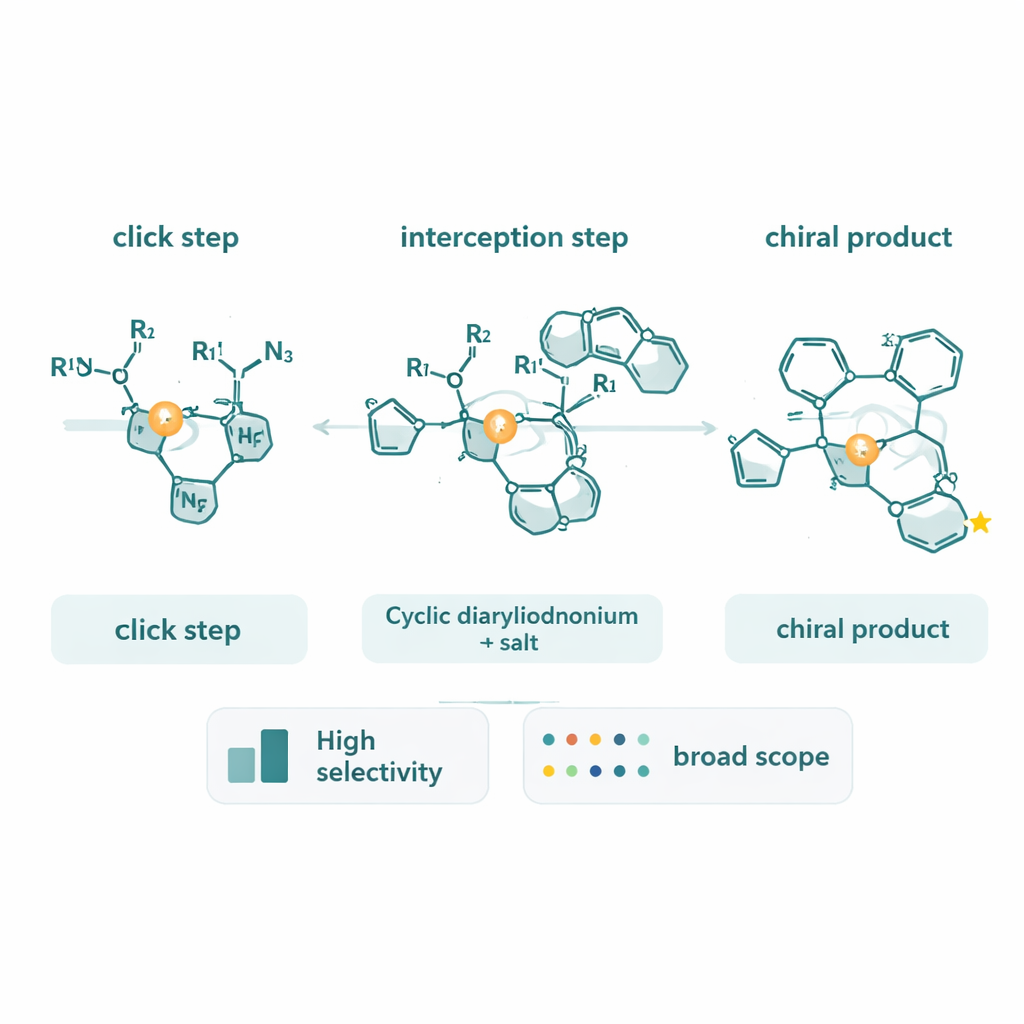
Zajrzeć pod maskę reakcji
Poza wytwarzaniem nowych molekuł zespół poświęcił dużo wysiłku, by ustalić, jak reakcja faktycznie przebiega. Używając alkinów znakowanych deuterem, zaobserwowali nietypowy odwrotny izotopowy efekt kinetyczny, co wskazuje na etap ograniczający szybkość, w którym atom węgla alkinu zmienia charakter wiązań, zamiast jedynie pękania wiązania C–H. Analiza postępu reakcji oparta na kalorymetrii wykazała, że szybkość reakcji silnie zależy od stężeń alkinu i azydu, ale tylko słabo od cyklicznego diaryliodonium. Pomiary te wspierają obraz, w którym tworzenie i przekształcanie kompleksu miedź–triazol oraz jego addycja oksydacyjna do pierścienia diaryliodonium wspólnie determinują tempo reakcji. Stwierdzono także, że chiralne produkty triazolowe same mogą przylegać do miedzi i spowalniać katalizator, co sugeruje możliwości dalszej optymalizacji systemu.
Co to oznacza na przyszłość
Mówiąc prościej, badacze nauczyli dobrze znaną reakcję click nowego triku: zamiast jedynie łączyć dwa kawałki, teraz pomaga ona zmontować trzy składniki w złożone, śmigłopodobne molekuły, wybierając niemal wyłącznie jeden preferowany skręt. To zapewnia skalowalną drogę do chiralnych biarylowych triazoli — struktur wartościowych jako potencjalne związki lecznicze, katalizatory i materiały funkcjonalne. Wnikliwości mechanistyczne — zwłaszcza dotyczące tego, jak przechwytuje się kluczowy pośrednik i jak produkt może zatruwać katalizator — oferują mapę drogową do zaprojektowania jeszcze bardziej wydajnych i selektywnych odmian tej chemii. Dla niespecjalistów najważniejszy wniosek jest taki, że już potężne narzędzie „klocków” molekularnych stało się bardziej wszechstronne, umożliwiając chemikom budowanie bardziej skomplikowanych i użytecznych kształtów z precyzyjną kontrolą ich formy trójwymiarowej.
Cytowanie: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Słowa kluczowe: chemia klik, kataliza miedziowa, chiralny biaryl, atropizomer, triazol