Clear Sky Science · pl
Biomarkery odpowiedzi na neoadiuwantową terapię palbocyklibem plus anastrozolem w opornym na terapię hormonalną raku piersi z receptorami estrogenowymi dodatnimi/HER2‑ujemnym: badanie fazy 2
Dlaczego to badanie ma znaczenie dla pacjentów i ich bliskich
Wiele kobiet z powszechnym podtypem raka piersi początkowo dobrze reaguje na leki blokujące hormony, lecz z czasem ich guzy stają się oporne i znów zaczynają rosnąć. Badanie stawia ważne pytanie: czy dodanie nowszego leku hamującego cykl komórkowy do standardowej terapii hormonalnej może pomóc w tych trudnych przypadkach i czy w guzie można znaleźć sygnały ostrzegawcze, które przewidują, kto skorzysta, a kto nie?
Uważniejsze spojrzenie na oporne raki piersi
Badanie skoncentrowano na nowotworach z receptorami estrogenowymi dodatnimi i HER2‑ujemnych, najczęstszym podtypie. Wszyscy 34 pacjenci byli wcześniej leczeni standardową przedoperacyjną terapią hormonalną (inhibitorem aromatazy), ale wciąż wykazywali aktywność podziałów komórek guza, co oznaczało, że nowotwór był uznany za „oporny na terapię hormonalną”. Następnie pacjentów leczono przed operacją kombinacją leku hormonalnego anastrozolu i inhibitora cyklu komórkowego palbocyklibu. Tempo podziałów komórek nowotworowych oceniano za pomocą markera Ki67. Jeśli Ki67 spadł do bardzo niskich wartości po dwóch tygodniach, mówiono o „całkowitym zatrzymaniu cyklu komórkowego”, co wskazywało, że podziały komórek nowotworowych zostały skutecznie zahamowane.
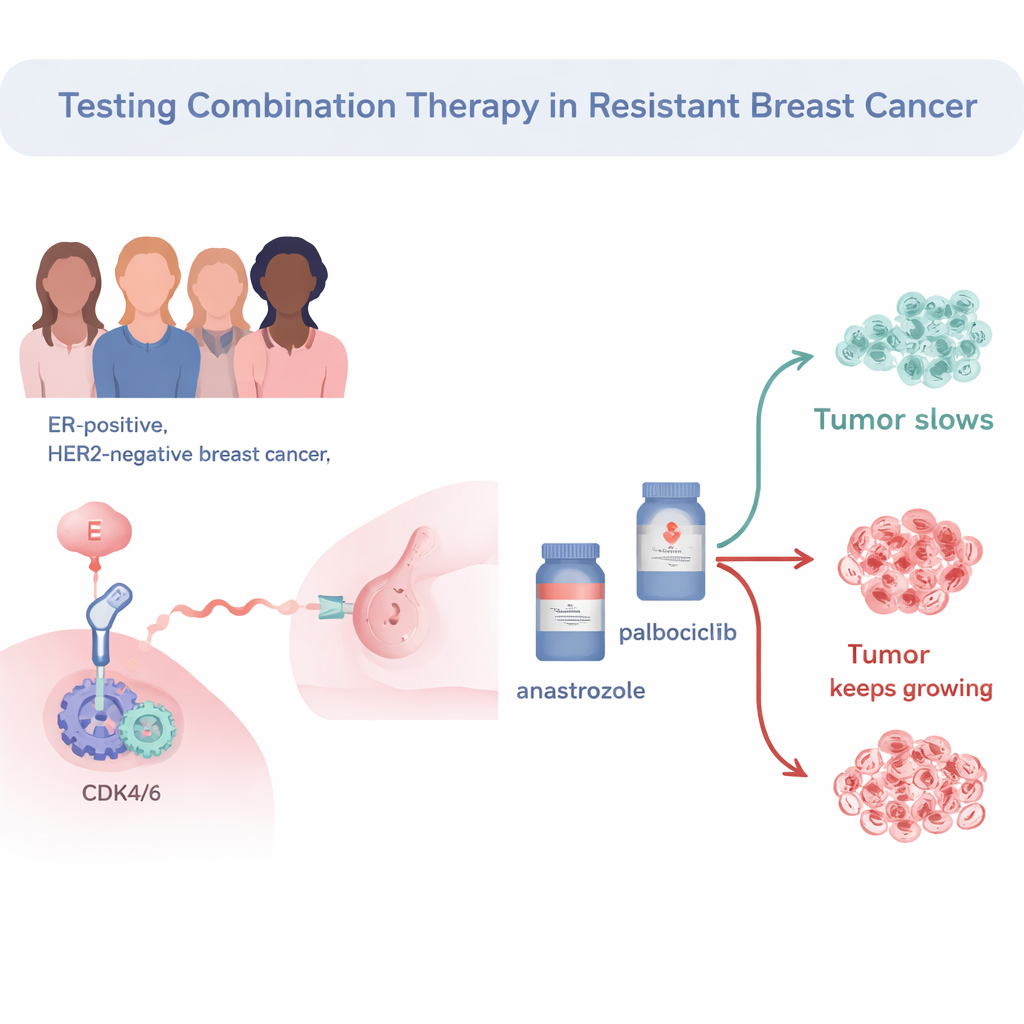
Kto odpowiedział na kombinację leków?
Wśród 33 pacjentów, których guzy można było w pełni ocenić, 57,6% osiągnęło całkowite zatrzymanie cyklu komórkowego już po dwóch tygodniach skojarzonego leczenia. Przy łagodniejszym progu — klasyfikując guzy jako „wrażliwe”, jeśli Ki67 spadł poniżej 10% — około dwóch trzecich guzów uznano za reagujące. Pacjenci, których guzy pozostawały wysoce aktywne pod względem Ki67, mieli zwykle bardziej agresywne nowotwory: wyższy stopień złośliwości, większy rozmiar i wyższe wartości wyjściowe Ki67. Częściej również należeli do tzw. molekularnych podtypów „nie‑luminalnych”, które ogólnie zachowują się bardziej agresywnie niż klasyczne, hormonozależne guzy „luminal A”.
Co sprawia, że niektóre guzy są oporne na leczenie?
Zespół poszedł dalej niż proste wskaźniki odpowiedzi i przeprowadził dogłębną analizę próbek guza z użyciem sekwencjonowania DNA, sekwencjonowania RNA oraz profilowania białek. Guzy oporne nie były określone przez jedną, pojedynczą mutację; zamiast tego wykazywały wzorzec „nadaktywnego okablowania”. W porównaniu z guzami wrażliwymi, nowotwory oporne miały osłabioną sygnalizację receptora estrogenowego, ale silniejszą aktywność szlaków napędzających podziały i wzrost komórek, takich jak geny cyklu komórkowego, ścieżka wzrostu mTOR oraz kilka sieci związanych z zapaleniem i interferonami. Wykazywały też wyższe poziomy immunologicznych „hamulców”, znanych jako punkty kontrolne odporności, w tym geny takie jak IDO1 i PD‑L1, które mogą pomagać guzom uciekać przed obroną organizmu.
Od szlaków do potencjalnych nowych terapii
Aby sprawdzić, czy te nadaktywne szlaki można wykorzystać przeciwko nowotworowi, badacze stworzyli laboratoryjne modele komórkowe, które stały się oporne na inhibitory CDK4/6, takie jak palbocyklib. Te oporne komórki wykazywały ten sam sygnaturowy wzorzec wzmocnionej sygnalizacji cyklu komórkowego oraz interferonowo‑zapalnej, jak obserwowano w guzach pacjentów. Po wystawieniu na działanie leków blokujących sygnalizację JAK‑STAT — kluczową drogę pośredniczącą w sygnalizacji interferonowej — jeden z preparatów, pacrytynib, okazał się szczególnie skuteczny w spowalnianiu wzrostu komórek opornych oraz organoidów pochodzących od pacjentów. Sugeruje to, że łączenie inhibitorów CDK4/6 z niektórymi lekami celującymi JAK może być obiecującą strategią dla pacjentów, których nowotwory przechytrzyły obecne kombinacje.
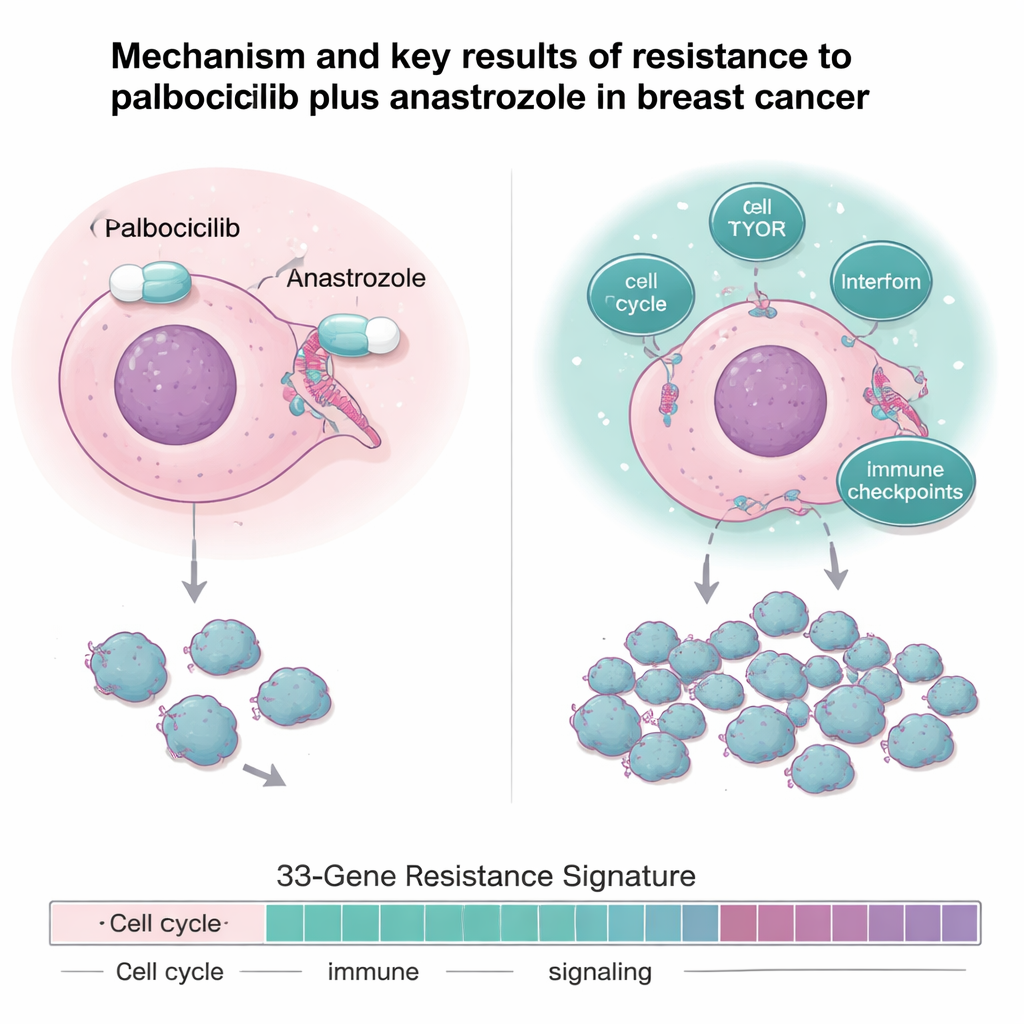
Genetyczny odcisk palca, który przewiduje wynik
Porównując guzy wrażliwe i oporne w dwóch powiązanych badaniach, badacze zbudowali 33‑genową „sygnaturę oporności”, obejmującą geny zaangażowane w podziały komórkowe, naprawę DNA, sygnalizację wzrostu, metabolizm oraz odpowiedzi immunologiczne/zapalne. Ten genowy odcisk palca bardzo trafnie odróżniał guzy wrażliwe od opornych w badaniu. Co ważne, gdy tę samą 33‑genową sygnaturę zastosowano do niezależnej grupy 151 pacjentów z przerzutowym rakiem piersi leczonych w praktyce rutynowej inhibitorami CDK4/6 plus terapią hormonalną, osoby, których nowotwory uzyskały wysoki wynik dla sygnatury oporności, miały krótszy czas do progresji choroby i krótsze całkowite przeżycie. Innymi słowy, ten wzorzec genowy mierzony przed leczeniem mógł wskazać pacjentów mniej prawdopodobnych do długotrwałego skorzystania z standardowych schematów opartych na CDK4/6.
Co to oznacza dla przyszłej opieki
Dla osób zmagających się z hormonozależnym, opornym na terapię rakiem piersi z receptorami estrogenowymi, to badanie daje zarówno poczucie ulgi, jak i mapę drogową. Pokazuje, że dodanie palbocyklibu do anastrozolu nadal może zahamować wzrost guza w ponad połowie opornych przypadków. Jednocześnie ujawnia, że niektóre guzy polegają na alternatywnych szlakach wzrostu i mechanizmach związanych z odpornością, co utrudnia ich kontrolę. Nowo zdefiniowana 33‑genowa sygnatura oraz odkrycie, że leki celujące JAK, takie jak pacrytynib, mogą hamować komórki oporne wskazują drogę do bardziej spersonalizowanego leczenia: identyfikowania tych, którzy najpewniej nie odpowiedzą na standardowe kombinacje, i szybszego kierowania ich do badań klinicznych testujących nowe partnerstwa lekowe, które bezpośrednio atakują zapasowe szlaki przeżycia guza.
Cytowanie: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
Słowa kluczowe: Rak piersi z receptorami ER dodatnimi, Inhibitory CDK4/6, Oporność na terapię hormonalną, Biomarkery guza, palbocyklib anastrozol