Clear Sky Science · pl
Przełamywanie ściany komórkowej dla efektywnego dostarczania DNA do okrzemek
Glony jako mikroskopijne zielone fabryki
Okrzemki — mikroskopijne glony unoszące się w oceanie — cicho wytwarzają około jednej piątej organicznego węgla na planecie, pomagając zasilać morskie sieci pokarmowe i pochłaniać dwutlenek węgla. Naukowcy chcą przekształcić te odporne, szybko rosnące organizmy w maleńkie zielone fabryki produkujące paliwa, żywność i związki specjalistyczne. Istniała jednak istotna przeszkoda: zaskakująco trudno jest niezawodnie wprowadzić nowe DNA do komórek okrzemek. W tym badaniu autorzy zajmują się tym praktycznym problemem wprost, opisując nowe sposoby wprowadzania instrukcji genetycznych i narzędzi do edycji genomu przez twardą zewnętrzną ścianę okrzemki.
Zmiękczanie pancerza mikrobów oceanicznych
Praca koncentruje się na modelowej okrzemce Phaeodactylum tricornutum, chętnie używanej w laboratoriach, ponieważ jej genom jest dobrze zmapowany i dysponuje już podstawowymi narzędziami genetycznymi. Autorzy założyli, że ściana komórkowa — pierwsza fizyczna bariera, którą musi pokonać każde DNA — jest kluczowym wąskim gardłem. Poprzez traktowanie komórek enzymem o nazwie alcalase częściowo lub całkowicie usunęli tę ścianę, tworząc kruche „sferoplasty” i „protoplasty”, które są znacznie łatwiejsze do penetracji. Gdy następnie zastosowali elektroporację — krótkie impulsy elektryczne otwierające tymczasowe pory — liczba udanych transformantów wzrosła dramatycznie, w przybliżeniu o dwie rzędy wielkości w porównaniu do wcześniejszych metod. Nawet bardzo niewielkie ilości DNA, już od jednego nanograma, wystarczały do odzyskania zmodyfikowanych komórek. 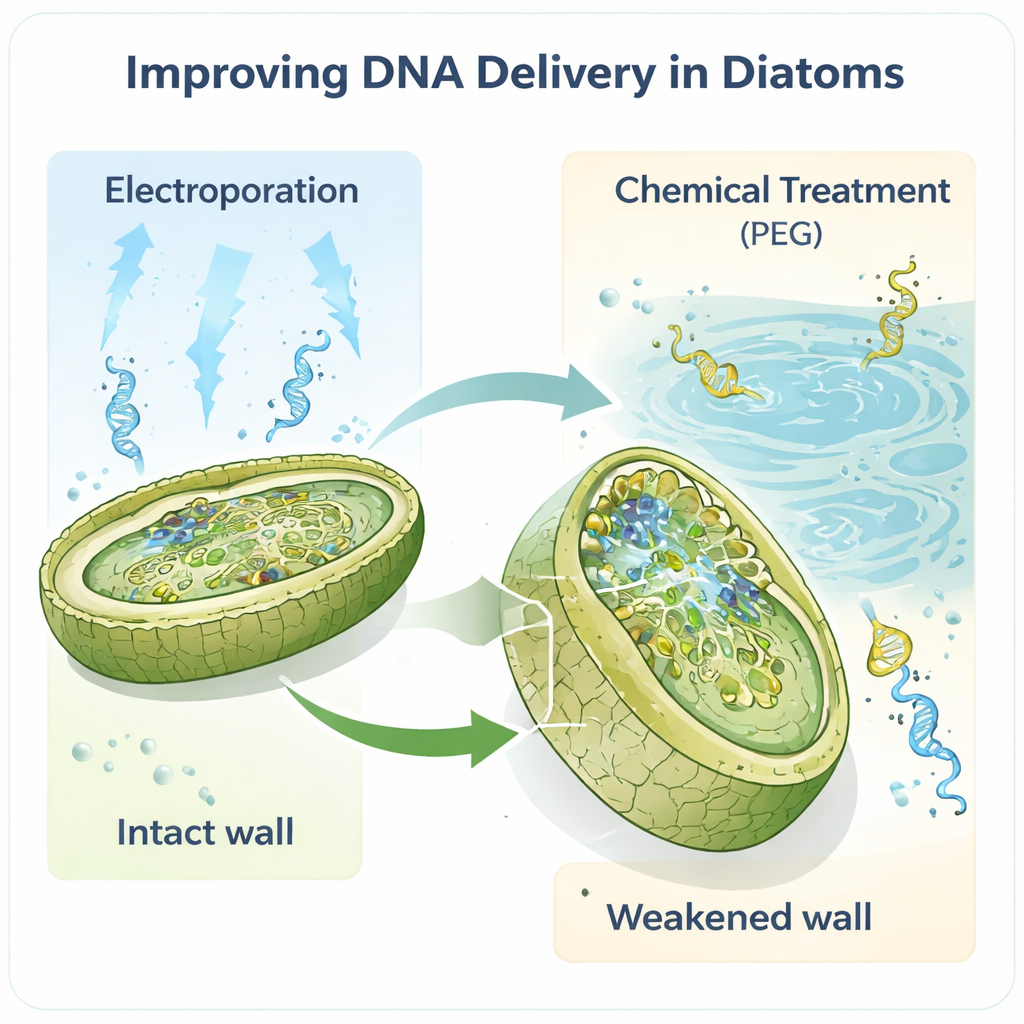
Szybkie dostarczanie DNA bez pośrednictwa bakterii
Tradycyjne metody modyfikacji okrzemek często polegają na bakteryjnych „kurierach” przenoszących duże, koliste cząsteczki DNA zwane episomami do glonów. Choć skuteczne, podejście to jest powolne, technicznie wymagające i może niestabilizować delikatnych konstrukcji DNA. Nowe protokoły pokazują, że zarówno elektroporacja, jak i dopracowana metoda chemiczna z polietylenoglikolem (PEG) potrafią wprowadzać episomy bezpośrednio do okrzemek, omijając etap bakteryjny. Co niezwykłe, dostarczono i odzyskano nienaruszone episomy o długości do 55,6 tysiąca par zasad. Te same strategie zadziałały także w drugim gatunku, Thalassiosira pseudonana, który ma mocniej zmineralizowaną ścianę, sugerując, że jest to szeroko użyteczny zestaw narzędzi, a nie trik ograniczony do jednego gatunku.
Pozwalając komórce zbudować własne kręgi DNA
Badając zachowanie DNA wprowadzonego elektroporacją, zespół natrafił na zaskakującą zdolność: okrzemki potrafią same sklejać fragmenty DNA. Liniowe kawałki episomów wchodziły do komórki i były naprawiane w kręgi albo przez niedokładne łączenie „bez homologii” (non‑homologous joining), albo przez dokładniejsze naprawy ukierunkowane na homologię (homology‑directed repair). Autorzy nazwali ten proces „in vivo assembly okrzemek”, w skrócie DIVA. Projektując nakładające się fragmenty, skłaniali komórki do składania dwóch, trzech lub czterech części w pełne episomy z wysokimi wskaźnikami powodzenia, czasami nawet włączając niewielkie syntetyczne kasety dodające znaczniki fluorescencyjne lub nowe funkcje. Ta zdolność zamienia jądro okrzemki w miniaturowy warsztat DNA, potencjalnie zastępując pracochłonne etapy składania zwykle wykonywane w drożdżach lub E. coli.
Edycja genomu wyłącznie przy użyciu kompleksów białkowych
Poza dodawaniem episomów, badacze pokazali, że mogą wprowadzać gotowe kompleksy białko‑RNA CRISPR–Cas9 bezpośrednio do komórek okrzemek przy użyciu zoptymalizowanej elektroporacji. Celując w gen o nazwie PtAPT, który kontroluje wrażliwość na toksyczny analog adeniny, wygenerowali tysiące odpornych mutantów bez wprowadzania dodatkowego DNA do genomu. Wielu z tych mutantów nosiło małe insercje lub delecje w miejscu docelowym; niektóre nawet przechwyciły fragmenty „nośnikowego” DNA, które dodano jako bufor przed impulsem elektrycznym. Zespół następnie współdostarczył kompleksy CRISPR i episomy w jednym kroku, stwierdzając, że około jedna na dziesięć kolonii zawierała jednocześnie edycję genomu i selekcjonowalny episom — efektywny sposób śledzenia inaczej niewidocznych zmian genowych. 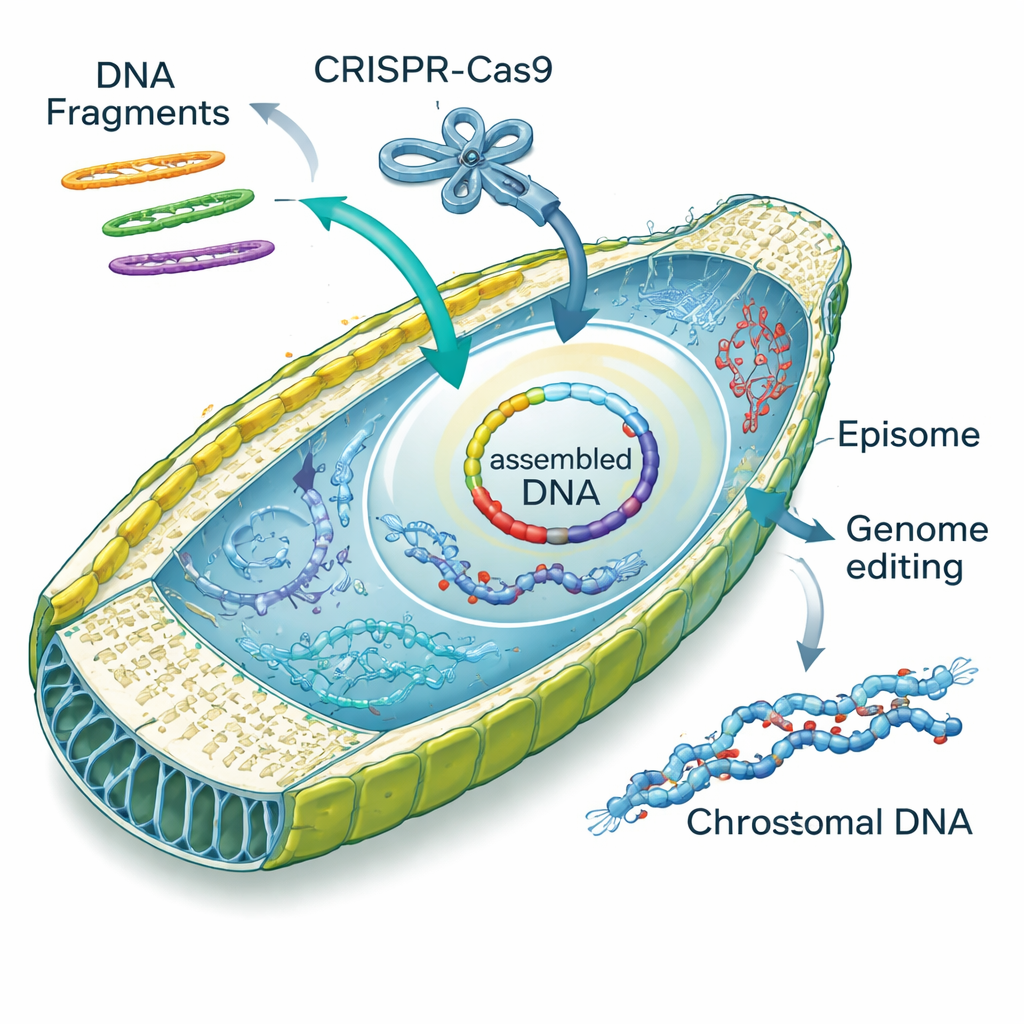
W stronę projektowanych okrzemek dla zrównoważonej przyszłości
Dla osób niezajmujących się tą dziedziną kluczowy przekaz jest taki, że okrzemki stają się znacznie bardziej praktycznymi, programowalnymi organizmami. Poprzez delikatne przełamywanie lub zmiękczanie ściany komórkowej autorzy przekształcili kapryśny, o niskiej wydajności proces w solidny pipeline wykorzystujący niewielkie ilości DNA, działający z dużymi konstrukcjami genetycznymi, a nawet pozwalający komórce na składanie i edycję własnego DNA. Te postępy skracają drogę od zaprojektowanej na komputerze sekwencji do żywej, przetestowanej szczepu. W dłuższej perspektywie takie narzędzia mogą przyspieszyć wysiłki na rzecz budowy okrzemek z całkowicie syntetycznymi chromosomami oraz wykorzystania tych oceanicznych mikroorganizmów do produkcji czyściejszych paliw, chemii przyjaznej klimatu i nowych odkryć biologicznych.
Cytowanie: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Słowa kluczowe: biotechnologia okrzemek, transformacja genetyczna, edycja genomu CRISPR, biologia syntetyczna, inżynieria mikroalg