Clear Sky Science · pl
Struktury telomerazy ludzkiej związanej z nukleotydami na kilku etapach cyklu dodawania powtórzeń DNA telomerowego
Dlaczego końce naszych chromosomów mają znaczenie
Za każdym razem, gdy komórka się dzieli, ochronne czapeczki na końcach chromosomów — zwane telomerami — stają się nieco krótsze. Gdy stają się zbyt krótkie, komórki przestają się dzielić lub działają nieprawidłowo, co przyczynia się do starzenia i chorób. Maszyneria molekularna zwana telomerazą potrafi odbudować te czapeczki i jest nietypowo aktywna w większości nowotworów. To badanie ujawnia z bezprecedensową szczegółowością, jak ludzka telomeraza chwyta i wydłuża telomery krok po kroku, dostarczając wskazówek, jak moglibyśmy kiedyś precyzyjnie modulować ten enzym w zaburzeniach związanych ze starzeniem i w raku.
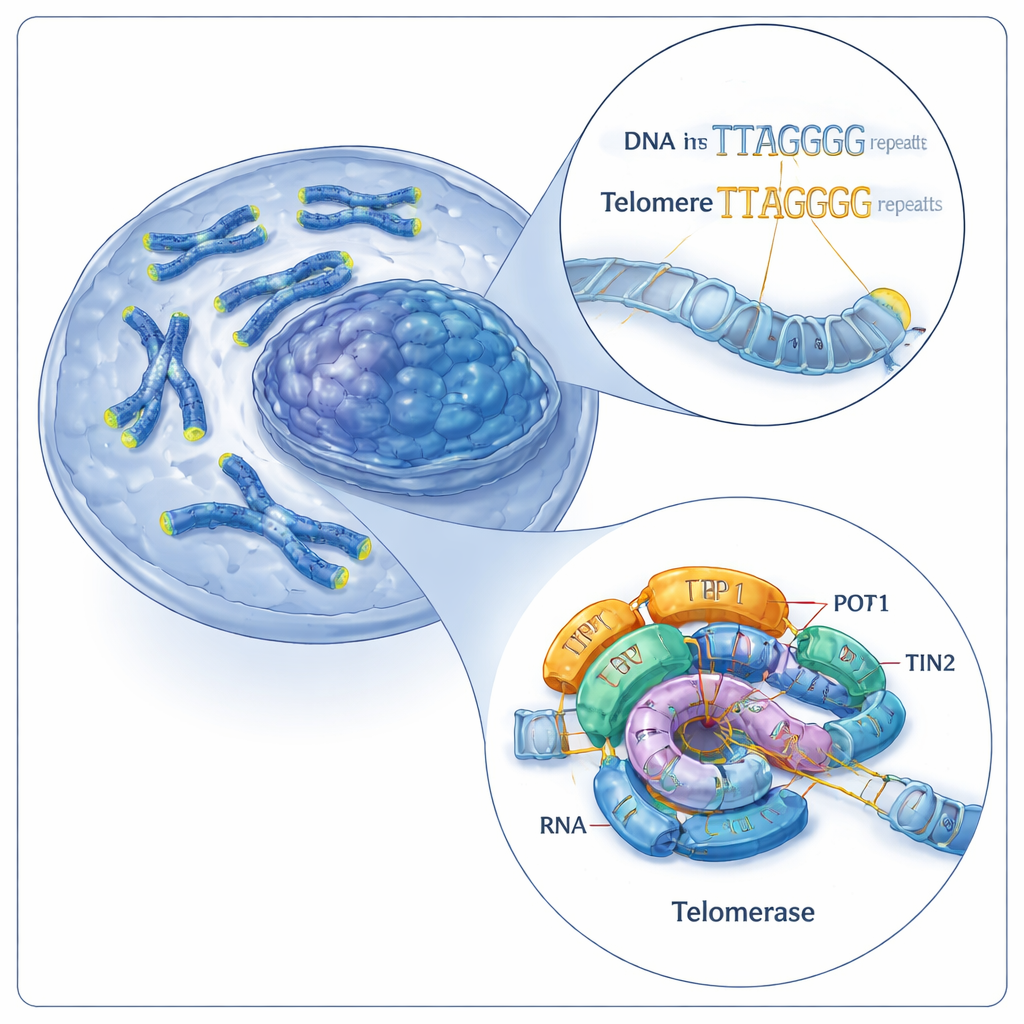
Zespół naprawczy osłon chromosomalnych
Telomery składają się z krótkich, powtarzających się sekwencji DNA (u ludzi sześcioliterowy wzorzec: TTAGGG). Telomeraza wydłuża telomery, dodając na końce chromosomów kolejne takie powtórzenia. Robi to przy pomocy dwóch głównych składników: białka zwanego telemerazową odwrotną transkryptazą (TERT) oraz wbudowanej cząsteczki RNA (hTR), która służy jako matryca. Razem tworzą rdzeń katalityczny, któremu dodatkowo pomagają białka pomocnicze znane jako shelterin, w tym trójka TPP1–POT1–TIN2. Poprzednie prace wizualizowały ludzką telomerazę tylko w jednym stanie pracy, pozostawiając istotne pytanie: jak ta maszyna wielokrotnie dodaje nowe powtórzenia, nie odrywając się od DNA?
Zamrażanie telomerazy w akcji
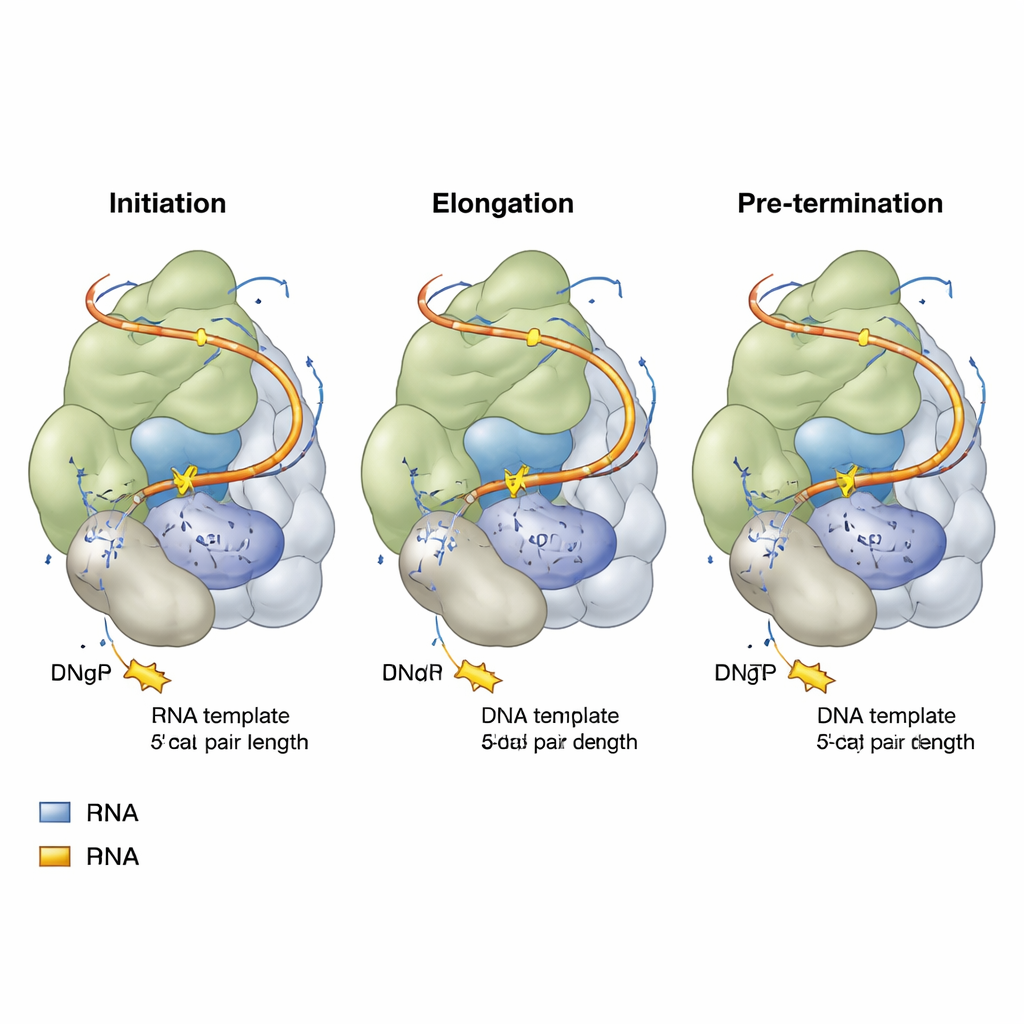
Naukowcy odtworzyli ludzką telomerazę w komórkach ludzkich, a następnie zmontowali ją z celowo zaprojektowanymi fragmentami DNA telomerowego oraz niereaktywnymi analogami nukleotydów — cząsteczkami przypominającymi litery DNA, ale niezdolnymi do pełnej inkorporacji. Przy użyciu wysokorozdzielczej krioelektronowej mikroskopii (cryo‑EM) uzyskali migawki telomerazy na trzech kluczowych etapach cyklu dodawania powtórzeń: startu (inicjacji), środka kopiowania (wydłużania) oraz tuż przed ukończeniem powtórzenia (przed‑zakończeniem). Każda migawka ukazywała rdzeń katalityczny telomerazy obejmujący krótki hybryd DNA–RNA, z nadchodzącym nukleotydem ustawionym w miejscu aktywnym, gotowym do dołączenia do rosnącego łańcucha DNA.
Malutki zamek błyskawiczny, który kontroluje wielki proces
We wszystkich trzech stanach pojawił się zaskakujący motyw: hybryd DNA–RNA wewnątrz telomerazy zachowuje w zasadzie tę samą długość — tylko cztery pary zasad, tymczasowo wydłużane do pięciu, gdy pojawia się nowy nukleotyd. Konkretne aminokwasowe resztę w TERT, nazwaną roboczo „głowicą zamka”, konsekwentnie wyznacza koniec tego krótkiego hybrydu i zapobiega jego dalszemu wydłużaniu. W miarę dodawania nowych liter DNA jedna para zasad na odległym końcu ulega rozdzieleniu, więc hybryd nigdy nie rozszerza się poza to ciasne okno czterech–pięciu par. Ta kompaktowa konstrukcja prawdopodobnie ułatwia rozdzielenie i przesuwanie nici, pozwalając enzymowi przesuwać się i rozpocząć następne powtórzenie bez całkowitego odpuszczenia DNA. Subtelne różnice w tym, które litery DNA i RNA zajmują to krótkie miejsce, wyjaśniają, dlaczego niektóre sekwencje końców telomerowych wiążą się z telomerazą silniej niż inne.
Elastyczne łączniki RNA i ruchome elementy
Matrycowy RNA w telomerazie nie jest swobodny; jest przywiązany przez elastyczne odcinki po obu stronach, zwane łącznikami matrycy 5′ i 3′. W miarę jak telomeraza przechodzi od inicjacji do przed‑zakończenia, górny (5′) łącznik jest napięty niczym lina bungee, ostatecznie osiągając w pełni rozciągnięty stan, który pomaga sygnalizować koniec powtórzenia. Tymczasem dolny (3′) łącznik wybrzusza się na zewnątrz i zbliża do innej struktury RNA (pętli P6.1) oraz pobliskich regionów białkowych. Jeśli te łączniki staną się zbyt krótkie lub zbyt długie, albo jeśli P6.1 zostanie zmienione, zdolność telomerazy do dodawania powtórzenie po powtórzeniu spada gwałtownie. Co ważne, niektóre regiony białkowe — domena TEN i specyficzny dla telomerazy wkład zwany klinem TRAP — działają jako regulowane prowadnice, stykając się zarówno z DNA, jak i z tymi łącznikami RNA. Mutacje zmniejszające rozmiar klina TRAP mogą w rzeczywistości zwiększać procesywność enzymu, co sugeruje, że klin zwykle działa jako kontrolowana bariera, odmierzająca ruch matrycy.
Nowe spostrzeżenia dotyczące celu terapeutycznego
Łącząc strukturalne migawki z testami funkcjonalnymi ukierunkowanych mutacji, badanie proponuje szczegółowy model mechaniczny wyjaśniający, jak ludzka telomeraza wielokrotnie wydłuża telomery. Enzym utrzymuje bardzo krótki hybryd DNA–RNA, używa reszty przypominającej zamek błyskawiczny, by wymusić tę długość, i polega na elastycznych łącznikach RNA oraz ruchomych elementach białkowych, by przesuwać matrycę i utrzymywać DNA zakotwiczone podczas wielu cykli kopiowania. Dla nie‑specjalistów kluczowy wniosek jest taki, że telomeraza nie działa jako statyczna maszyna kopiująca, lecz jako precyzyjnie wyregulowane, sprężynowe urządzenie, którego geometria i ruchome elementy determinują, jak długo i jak skutecznie może utrzymywać telomery. Zrozumienie tej choreografii otwiera drogę do leków, które mogłyby albo stłumić telomerazę w nowotworach, albo stabilizować jej funkcję w chorobach przedwczesnego starzenia.
Cytowanie: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Słowa kluczowe: telomeraza, telomery, cryo-EM, stabilność genomu, biologia nowotworów