Clear Sky Science · pl
Przestrzenno‑czasowa regulacja ładunku energetycznego determinuje funkcję limfocytów T
Dlaczego „baterie” naszego układu odpornościowego mają znaczenie
Nasz układ odpornościowy opiera się na limfocytach T — białych krwinkach tropiących komórki zakażone lub nowotworowe. Jak wszystkie aktywne komórki, limfocyty T potrzebują paliwa. W tym badaniu postawiono pozornie proste pytanie: ile energii mają pojedyncze limfocyty T w różnych miejscach w organizmie i o różnych porach dnia — i czy ten poziom energii wpływa na ich sprawność? Odpowiedzi wskazują, że limfocyty T działają jakby na wewnętrznym „naładowaniu baterii”, które wzrasta i spada wraz z dostępnością składników odżywczych i rytmami dobowymi, a to naładowanie bezpośrednio kształtuje ich siłę działania.
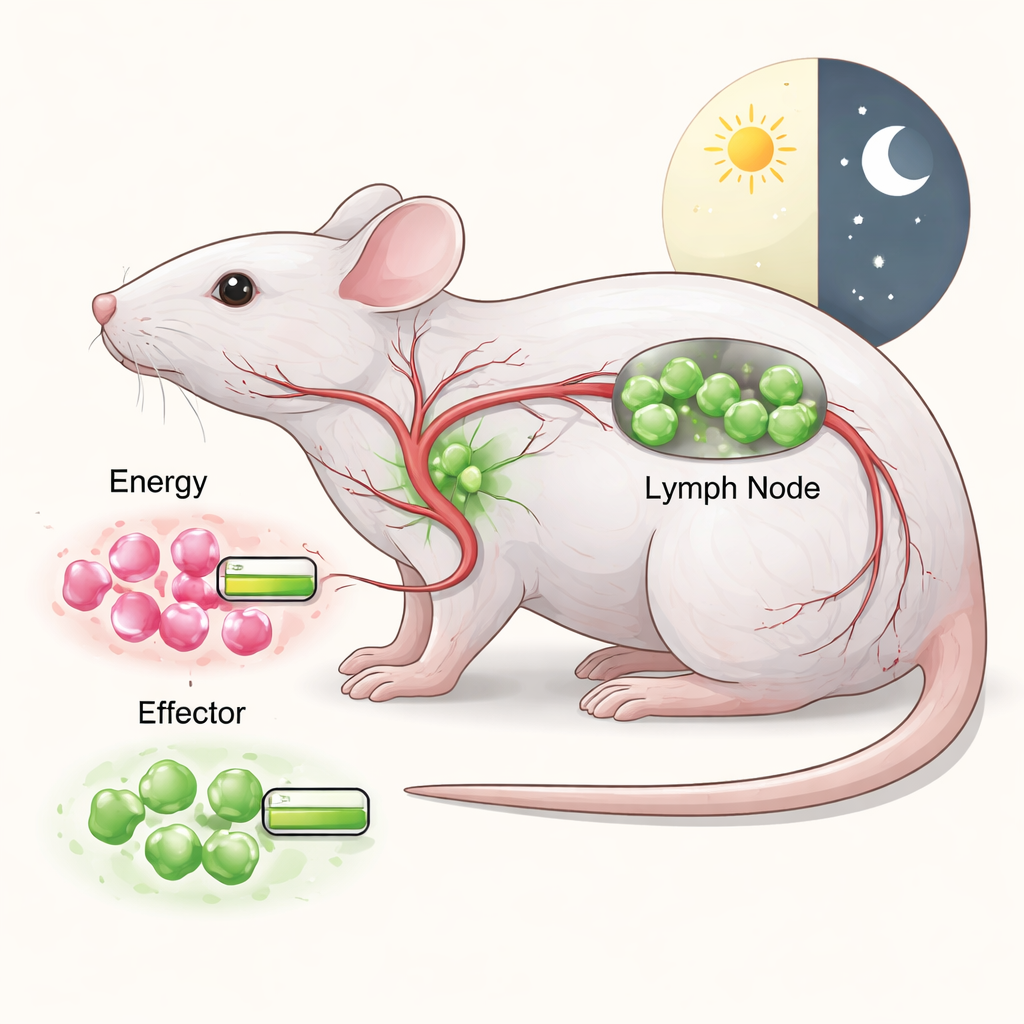
Pomiary wewnętrznego wskaźnika paliwa w komórkach odpornościowych
Naukowcy wykorzystali specjalną linię myszy, których komórki odpornościowe nosiły fluorescencyjny sensor raportujący stosunek ATP do ADP — dwóch cząsteczek działających jak naładowane i częściowo rozładowane „baterie” wewnątrz komórek. Wysoki stosunek ATP:ADP oznacza, że komórka jest energetycznie zasobna; niższy stosunek wskazuje na bardziej wyczerpane rezerwy. Przy użyciu metody nazwanej SPICE‑Met zespół mógł jednocześnie odczytywać ten stosunek energii w wielu typach komórek odpornościowych za pomocą cytometrii przepływowej, jednocześnie krótko blokując konkretne szlaki zaopatrzenia w paliwo, takie jak oddychanie mitochondrialne czy rozkład cukrów. Pozwoliło to zobaczyć nie tylko ile energii mają różne komórki, ale też które paliwa — glukoza, tłuszcze czy aminokwasy — są najważniejsze dla utrzymania wysokiego poziomu energii.
Różne zadania odpornościowe, różne poziomy energii
Analiza komórek krwi wykazała, że komórki odpornościowe nie mają jednolitego ładunku energetycznego. Limfocyty B, neutrofile, a zwłaszcza limfocyty „efektorowe” T oraz komórki NK (natural killers) — te aktywnie gotowe do ataku — miały najwyższe stosunki ATP:ADP. Natomiast spokojniejsze limfocyty „naiwne” i centralne pamięci, które czekają w pogotowiu na napotkanie zagrożenia, miały niższy ładunek energetyczny. Komórki o najwyższej energii mocno polegały na glikolizie, czyli szybkim spalaniu glukozy, podczas gdy limfocyty spoczynkowe opierały się bardziej na oddychaniu mitochondrialnym. Istotne było to, że samo stwierdzenie, iż komórka „używa mitochondriów” lub „używa glikolizy”, nie wystarczało: kluczowe było, jak duży wkład dany szlak rzeczywiście wnosił do ostatecznego stosunku energii.
Jak lokalizacja i dostępność cukru zmieniają moc limfocytów T
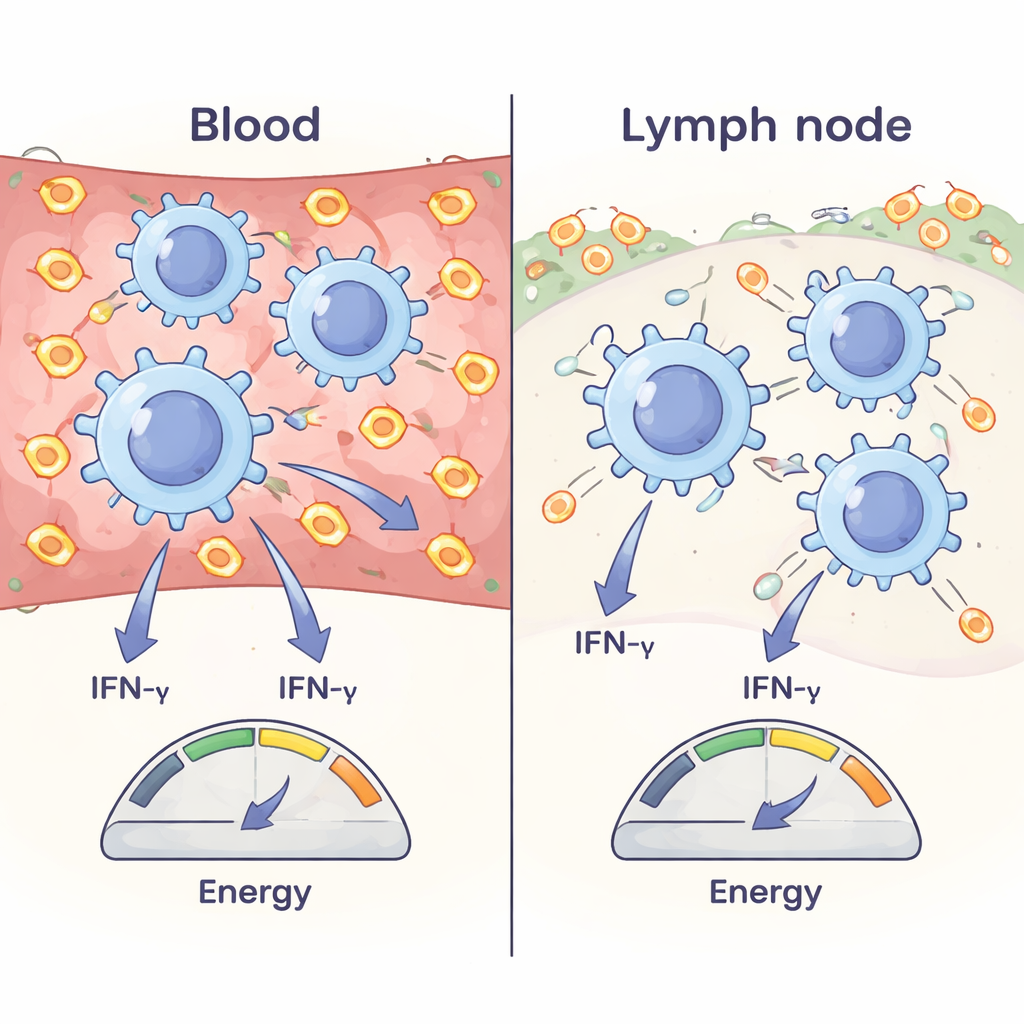
Kluczowe odkrycie polegało na tym, że ten sam typ limfocytu efektorowego T miał różny ładunek energetyczny w zależności od miejsca pobytu. Limfocyty efektorowe we krwi miały znacznie wyższy stosunek ATP:ADP niż ich odpowiedniki w węzłach chłonnych, nawet gdy rozpoznawały ten sam antygen szczepionkowy. Przez przenoszenie limfocytów z węzłów chłonnych do nowych myszy i analizowanie ich zaledwie kilka godzin później zespół wykazał, że ta różnica nie jest zaprogramowana na stałe: gdy limfocyty efektorowe przemieszczają się do krwi, ich ładunek energetyczny rośnie; kiedy siedzą w węzłach chłonnych, spada. Główną przyczyną jest dostępność glukozy. Krew jest stosunkowo bogata w cukier, podczas gdy węzły chłonne są stosunkowo ubogie. W węzłach chłonnych limfocyty efektorowe zwiększają ekspresję transportera glukozy GLUT1 — co stanowi reakcję awaryjną na niski poziom glukozy — i wykazują oznaki łagodnego stresu energetycznego. Gdy wchłanianie glukozy zostaje zablokowane, limfocyty efektorowe we krwi szybko tracą ładunek energetyczny, podczas gdy komórki w węzłach chłonnych lepiej rekompensują to spalaniem tłuszczów i aminokwasów.
Rytmy dobowości kształtują siłę odporności
Zespół badał także, jak pora dnia wpływa na energię komórek odpornościowych. Myszy utrzymywane w ściśle kontrolowanym cyklu światło–ciemność wykazywały silne oscylacje okołodobowe w ładunku energetycznym limfocytów T: limfocyty efektorowe, komórki NK i pokrewne miały mniej więcej dwukrotnie wyższy ładunek energetyczny w niektórych porach niż w innych, z szczytami na początku fazy odpoczynku. Te oscylacje odpowiadały zmianom stężenia glukozy we krwi i utrzymywały się nawet w stałej ciemności, co wskazuje na działanie wewnętrznego zegara. Krótkotrwałe posty u myszy obniżały poziom glukozy we krwi, a ładunek energetyczny limfocytów efektorowych i komórek NK malał, podczas gdy limfocyty naiwnie pozostawały w dużej mierze niezmienione — podkreślając, jak bardzo aktywni „bojownicy” zależą od obfitych składników odżywczych.
Ładunek energetyczny jako regulator siły ataku limfocytów T
Na koniec autorzy zapytali, czy zmiana tego ładunku energetycznego rzeczywiście modyfikuje wydajność limfocytów T. Limfocyty efektorowe pobrane z krwi były większe i produkowały więcej kluczowego dla przeciwwirusowej i przeciwnowotworowej odpowiedzi IFN‑γ oraz więcej perforyny niż odpowiadające im komórki z węzłów chłonnych. W ciągu dnia zdolność limfocytów do wytwarzania IFN‑γ była największa, gdy ich ładunek energetyczny był największy. W eksperymentach in vitro badacze systematycznie obniżali energię limfocytów przy użyciu inhibitorów metabolicznych; w miarę spadku stosunku ATP:ADP produkcja IFN‑γ, rozmiar komórek i poziomy perforyny malały równolegle. Razem te ustalenia pokazują, że wewnętrzny ładunek energetyczny limfocytu T nie jest tylko biernym odczytem — to regulowany przycisk, który łączy dostępność składników odżywczych i rytmy dobowości z siłą odpowiedzi układu odpornościowego.
Cytowanie: Chikina, A.S., Corre, B., Lemaître, F. et al. Spatiotemporal regulation of energetic charge dictates T cell function. Nat Commun 17, 770 (2026). https://doi.org/10.1038/s41467-026-68559-1
Słowa kluczowe: metabolizm limfocytów T, energia odpornościowa, glukoza i odporność, odporność okołodobowa, stosunek ATP do ADP