Clear Sky Science · pl
Metylacja DNA i lncRNA kontrolują niesynchroniczne replikowanie DNA w specyficznych domenach imprintowanych genów
Dlaczego harmonogram kopiowania DNA przez komórkę ma znaczenie
Za każdym razem, gdy komórka się dzieli, musi skopiować cały swój DNA, ale nie wszystkie regiony są duplikowane w tym samym momencie. Niektóre odcinki są kopiowane wcześnie, inne późno, według precyzyjnego „rozkładu” genomu. W pracy tej badano, dlaczego w kilku specjalnych klastrach genów, które pamiętają, od którego rodzica pochodzą, kopie matczyne i ojcowskie są kopiowane w różnych momentach. Zrozumienie tej nietypowej terminowości rzuca światło na to, jak chemiczne znaczniki na DNA i długie RNA niekodujące (lncRNA) pomagają organizować genom i mogą wpływać na rozwój oraz choroby.
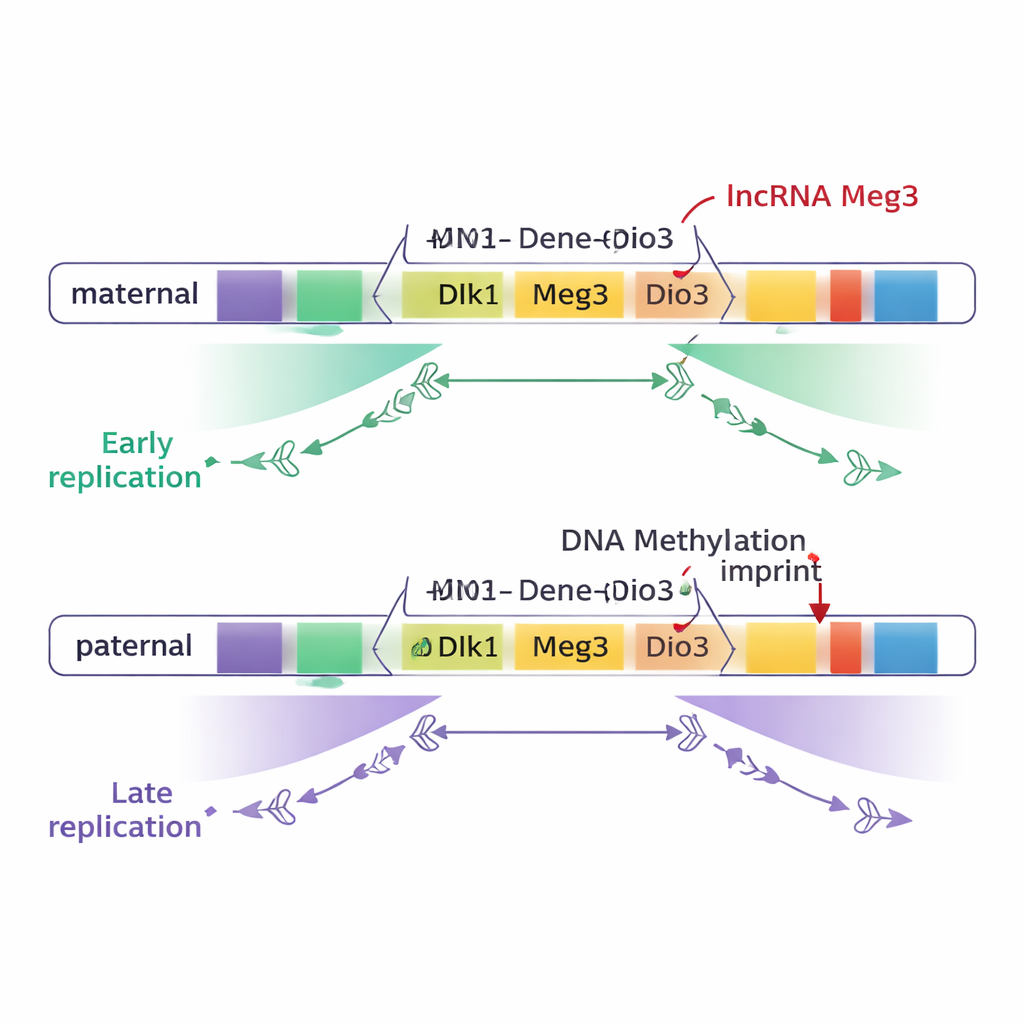
Rodzicielskie pamięci zapisane na DNA
U ssaków niewielka liczba domen genów „imprintowanych” zachowuje się odmiennie w zależności od tego, czy została odziedziczona po matce, czy po ojcu. Efekt pochodzenia rodzicielskiego kontrolowany jest przez metylację DNA — drobne chemiczne znaczniki dodawane w określonych regionach zwanych różnicowo metylowanymi regionami (DMR) — oraz przez zmiany w upakowaniu chromosomów. Autorzy badali mysie komórki macierzyste embrionalne, które przypominają bardzo wczesne komórki embrionalne. Porównali komórki zawierające jedynie genomy matki, jedynie genomy ojca oraz normalne hybrydy posiadające po jednym genomie każdego z rodziców. Śledząc, kiedy fragmenty DNA były kopiowane w cyklu komórkowym, odwzorowali terminowość replikacji w całym genomie i przyjrzeli się znanym regionom imprintowanym.
Dwie domeny imprintowane łamią reguły
Większość genomu, w tym większość domen imprintowanych, okazała się być kopiowana w tym samym czasie na chromosomach matczynych i ojcowskich. Jednak dwie duże domeny imprintowane wyróżniały się: domena Dlk1–Dio3 na chromosomie 12 oraz region Snrpn na chromosomie 7. W tych strefach szeroki fragment DNA — około trzech czwartych miliona par zasad w Dlk1–Dio3 — był kopiowany wcześnie na jednym chromosomie rodzicielskim, a późno na drugim. Co istotne, różnica ta wynikała z pochodzenia rodzicielskiego, a nie z tła szczepowego: matyczna kopia kluczowych genów, takich jak Dlk1 i gen lncRNA Meg3, konsekwentnie replikowała się wcześnie, podczas gdy kopie ojcowskie replikowały się późno.
Metylacja DNA ustawia przełącznik czasowy
Aby sprawdzić, co powoduje tę różnicę w terminowości, badacze zaprojektowali komórki macierzyste, w których normalny wzór metylacji w DMR był albo wymazany, albo wymuszony na obu chromosomach rodzicielskich. Gdy obie kopie DMR w Dlk1–Dio3 były zmethylowane, cały region replikował się późno na obu chromosomach. Gdy metylacja była w dużej mierze usunięta z obu kopii, ten sam region replikował się wcześnie na obu. Podobne eksperymenty w regionie Snrpn także spowodowały utratę różnic w terminowości. Wyniki te pokazują, że specyficzna dla rodzica metylacja DNA jest niezbędna do stworzenia kontrastu wczesnej i późnej replikacji między chromosomami matczynymi i ojcowskimi, przynajmniej w tych dwóch domenach.
Długie RNA dopracowuje wczesną replikację
Jednak sama metylacja DNA nie wyjaśniała całej historii. Region Dlk1–Dio3 produkuje także długie RNA niekodujące zwane Meg3 w ramach dużego „polycistronowego” transkryptu. Na chromosomie matczym niemetylowane DMR pozwalają na ekspresję Meg3; na chromosomie ojcowskim metylacja utrzymuje go w stanie nieaktywnym. Tworząc precyzyjne delecje wyłączające Meg3 przy jednoczesnym zachowaniu metylacji DNA, autorzy pokazali, że utrata RNA Meg3 powodowała przesunięcie części domeny matczynej z wczesnej na późniejszą replikację. Innymi słowy, RNA Meg3 pomaga promować wczesne kopiowanie przyległych fragmentów matczynego chromosomu, dodając drugą warstwę kontroli obok metylacji DNA.
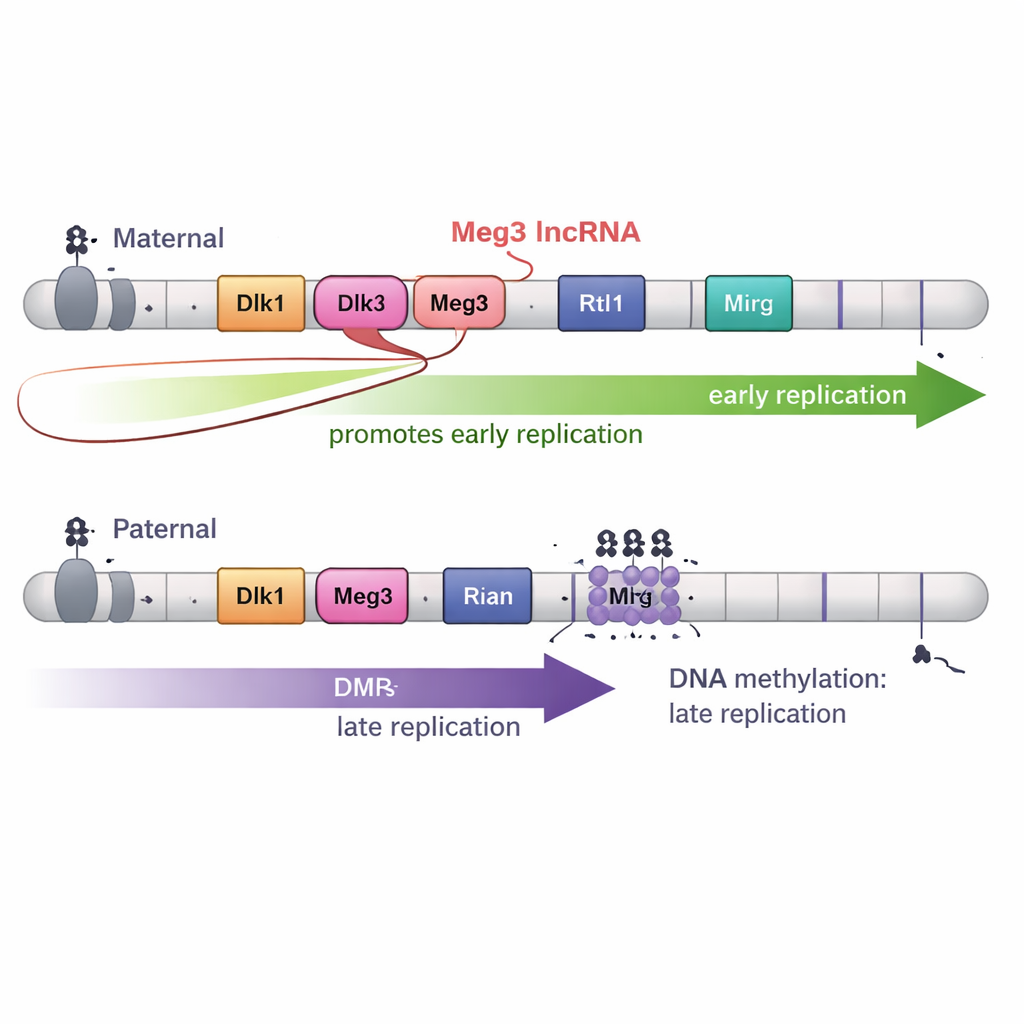
Składanie 3D i rozwój wprowadzają dalsze zawirowania
Ponieważ upakowanie genomu w trzech wymiarach często wiąże się z terminowością replikacji, zespół szczegółowo odwzorował architekturę chromosomów 3D. Ku zaskoczeniu, w regionie Dlk1–Dio3 granice domen 3D nie pokrywały się z granicami wczesnej i późnej replikacji. Nawet gdy wzory metylacji zostały zmienione i terminowość replikacji uległa zmianie, podstawowe jednostki składania — topologicznie asocjujące się domeny (TAD) — zmieniały się w inny sposób. Wreszcie, gdy komórki macierzyste zostały zróżnicowane w kierunku progenitorów nerwowych, wyraźne różnice w terminowości między kopiami matczynymi i ojcowskimi w większości zanikły, mimo że znaki imprintingu i wiele aspektów struktury 3D pozostało. Sugeruje to, że sygnały rozwojowe mogą nadpisywać specjalny wzorzec wczesne-wobec-późnego obserwowany w komórkach macierzystych.
Co to oznacza prostymi słowami
Badanie to pokazuje, że w kilku specjalnych sąsiedztwach genów, które pamiętają, od którego rodzica pochodzą, harmonogram kopiowania DNA przez komórkę jest kontrolowany przez kombinację chemicznych znaczników na DNA i długich RNA niekodujących. Metylacja DNA w kontrolnych regionach imprintowanych ustawia podstawowy stan wczesnego lub późnego kopiowania dla każdej kopii rodzicielskiej, a lncRNA Meg3 dodatkowo przesuwa pobliskie matczyne DNA w kierunku wcześniejszej replikacji. Efekty te działają w dużej mierze niezależnie od sposobu składania chromosomu w 3D. W trakcie rozwoju, gdy komórki się specjalizują, ten nietypowy rytm zanika, co pokazuje, że jest on cechą stanu pluripotentnych komórek macierzystych. Razem praca wyjaśnia, jak rodzicielskie epigenetyczne «pamięci» i niekodujące RNA mogą lokalnie nadpisywać zwykły rozkład terminów replikacji genomu.
Cytowanie: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Słowa kluczowe: imprinting genomowy, metylacja DNA, terminowość replikacji, długie RNA niekodujące, komórki macierzyste embrionalne