Clear Sky Science · pl
Mikrobialna aktywacja receptora GLP-2 łagodzi zapalenie przewodu pokarmowego
Dlaczego białko przyjazne jelitom ma znaczenie
W miarę jak świat szuka zrównoważonych sposobów żywienia rosnącej populacji, naukowcy patrzą poza farmy i pola w stronę wielkich stalowych zbiorników, w których hoduje się mikroby jako źródło pożywienia. Badanie to sprawdza, czy jedno z takich mikrobiologicznych białek może robić więcej niż tylko nas odżywiać. Autorzy postawili pytanie: czy białko pochodzące z nieszkodliwych bakterii może jednocześnie zaspokajać potrzeby żywieniowe i aktywnie chronić jelito przed zapaleniem — kluczowym problemem w chorobach takich jak nieswoiste zapalenia jelit czy uszkodzenia jelit wywołane chemioterapią?
Nowy rodzaj białka z mikroorganizmów
Białko będące w centrum tej pracy pochodzi z bakterii glebowej Methylococcus capsulatus Bath (McB). Zamiast spożywać żywe bakterie, McB jest przetwarzany do lizatu mikrobiologicznego — w praktyce proszkowej mieszanki rozbitych komórek bakteryjnych — sprzedawanej komercyjnie pod nazwą FeedKind®. Myszy otrzymywały diety, w których ten lizat dostarczał większość białka, w wariancie prostym lub w bardziej przypominającym dietę ludzką „złożonym” jadłospisie. Zespół śledził, jak taka dieta zmienia skład mikrobioty jelitowej, komórki odpornościowe patrolujące jelito oraz odporność jelita na różne rodzaje urazów.
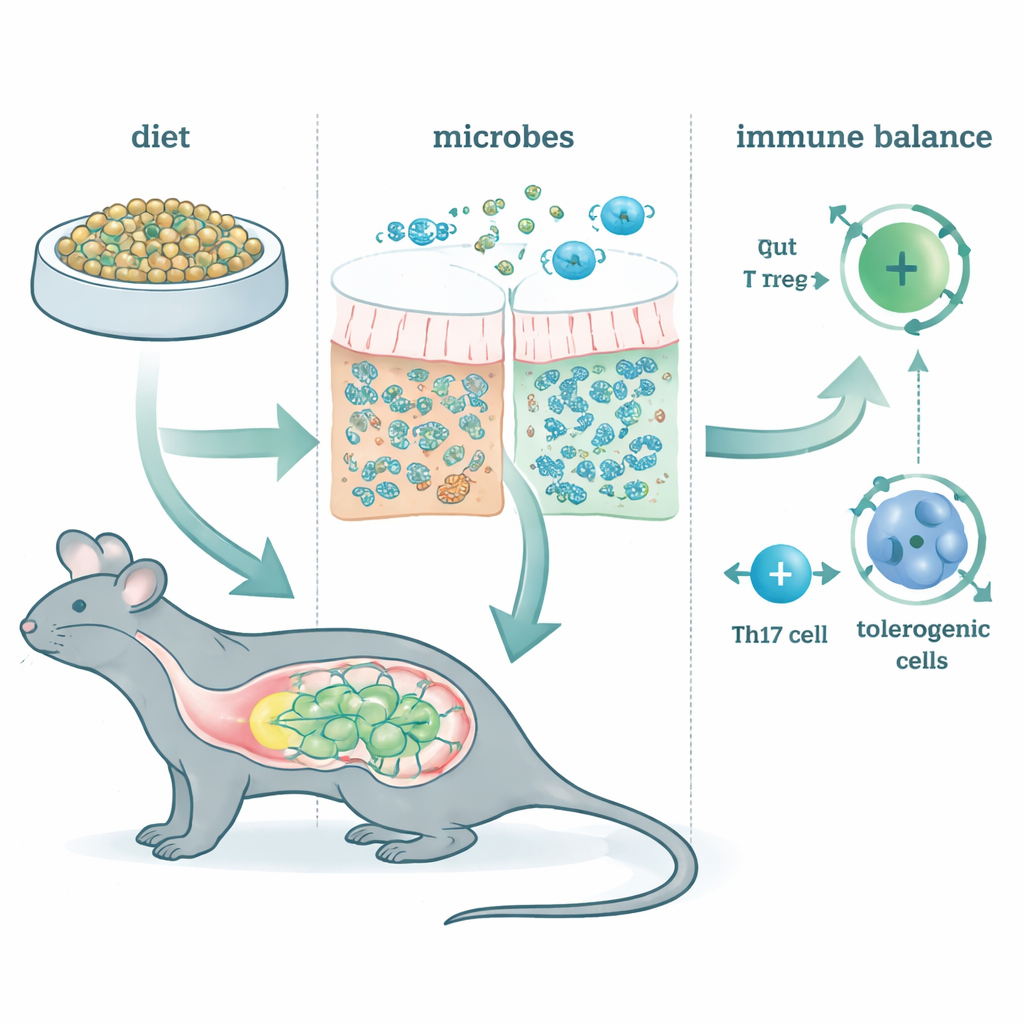
Przekształcanie mikrobiologicznego sąsiedztwa
Podawanie McB szybko i utrwale zmieniało mikrobiotę jelitową, niezależnie od tego, jaką podstawową dietę stosowały zwierzęta. Tylko niewielka część samego McB pojawiała się w kale, co oznacza, że materiał był niemal całkowicie wykorzystany w jelicie. Zamiast niego rozkwitło kilka gatunków bakterii z rodzin takich jak Lachnospiraceae i Bacteroidaceae. Analizy genetyczne wykazały, że te społeczności były wzbogacone w szlaki fermentacji prowadzące do produkcji krótkołańcuchowych kwasów tłuszczowych — małych cząsteczek już znanych z odżywiania komórek jelitowych i wpływu na odporność. Innymi słowy, McB działał mniej jak konwencjonalne białko, a bardziej jak ukierunkowane paliwo, które zmienia funkcje miejscowych mikroorganizmów.
Nauka tolerancji układu odpornościowego
Autorzy zbadali następnie kluczowe typy komórek T, które decydują, czy jelito reaguje spokojnie czy agresywnie na to, co przez nie przechodzi. Jedna grupa, obwodowo indukowane regulatorowe komórki T (pTreg), pomaga zapobiegać nadreakcji na pokarm i „przyjazne” mikroby. Inna grupa, komórki Th17, może albo napędzać szkodliwe zapalenie, albo pomagać utrzymać zdrową barierę, w zależności od ich „nastroju”. Karmienie McB wyraźnie zwiększało liczbę pTreg w całym przewodzie pokarmowym, nawet gdy większość mikrobioty została zniszczona przez antybiotyki. Natomiast wpływ McB na komórki Th17 zależał od obecności i prawidłowej funkcji bakterii jelitowych. U myszy z nienaruszoną mikrobiotą McB przesuwał Th17 w stronę bardziej uspokajającego, produkującego IL-10, mniej zapalnego stanu. Gdy fermentacja była zablokowana, ten tolerogenny przesunięcie znikało, co podkreśla, że McB działa częściowo przez zmianę komunikacji między mikrobiotą a układem odpornościowym.
Ochrona jelita podczas urazu
Aby sprawdzić, czy te zmiany przekładają się na realną ochronę, badacze wystawili myszy na dwa silne uszkodzenia jelit. Jednym z nich był lek chemioterapeutyczny 5‑fluorouracyl, który powoduje rozległe uszkodzenia i skurczenie włosowatych kosmków odpowiedzialnych za wchłanianie składników odżywczych. Drugim był związek chemiczny (DSS), wywołujący zapalenie okrężnicy jako model stanu zapalnego jelita grubego. Myszy na diecie z McB mniej traciły na wadze, zachowały dłuższe kosmki i większą długość jelita grubego, miały mniej krwawiących zmian i niższe oceny mikroskopowego uszkodzenia w obu modelach. Korzyści te utrzymywały się nawet po eksperymentalnym usunięciu komórek CD4, co sugeruje, że ochronne działanie McB nie wynika wyłącznie z komórek odporności adaptacyjnej, lecz obejmuje także bezpośrednie efekty na wyściółkę jelita.
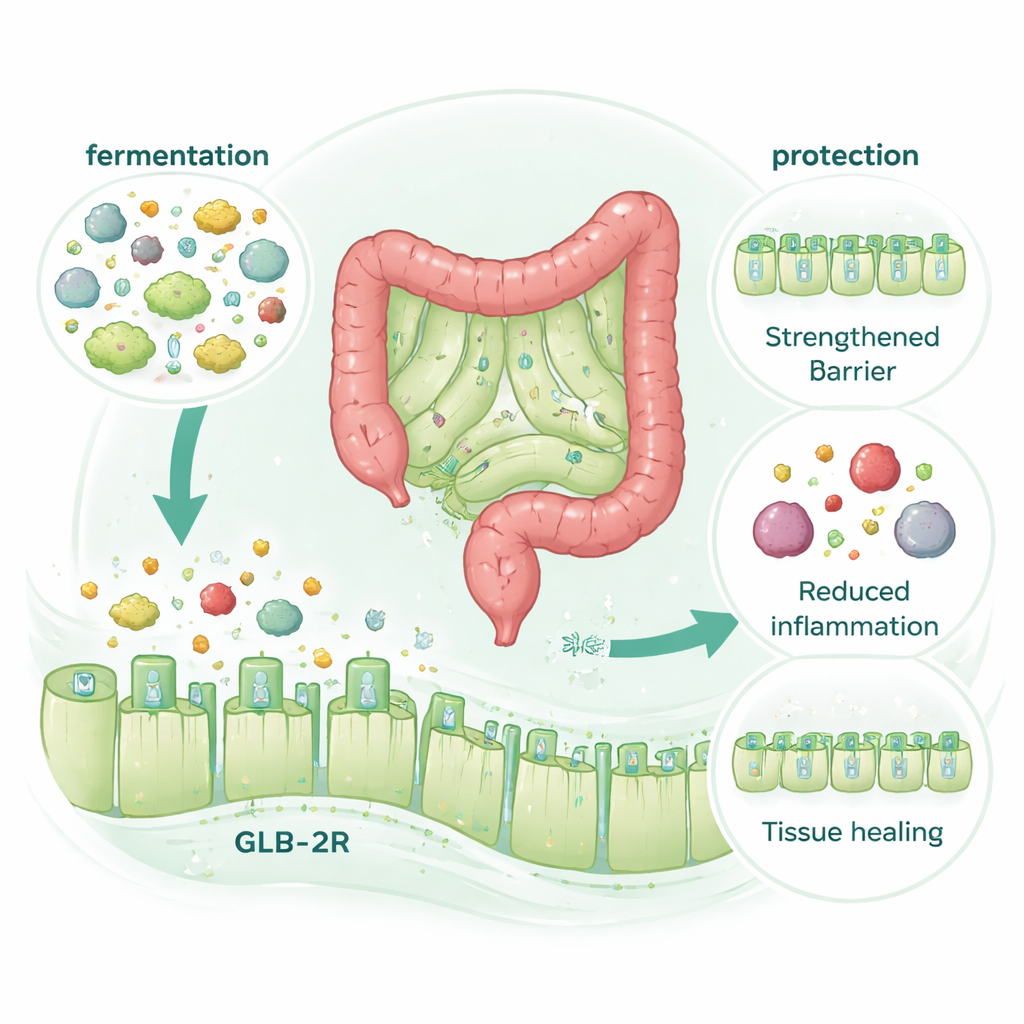
Receptor hormonu, ale bez dodatkowego hormonu
Zaskakującym odkryciem było to, że ochronny efekt McB absolutnie wymagał receptora jelitowego dla hormonu sprzyjającego naprawie zwanego GLP‑2 (receptor GLP‑2, GLP‑2R), ale nie wymagał związanego receptora GLP‑1. Gdy myszy pozbawione były GLP‑2R, McB przestał ich chronić przed uszkodzeniami po chemioterapii lub w modelu kolitis. Jednocześnie sam McB nie podnosił poziomów GLP‑2 we krwi, nawet gdy trawienie i rozkład hormonów były starannie kontrolowane. Zamiast tego korzyści znikały, gdy chemicznie zablokowano fermentację w okrężnicy, mimo że ogólny skład mikrobioty zmienił się bardzo niewiele. Wskazuje to na mechanizm, w którym mikrobialny rozkład McB generuje małe związki działające jak „mimetyki” GLP‑2, aktywujące jego receptor i wzmacniające barierę oraz sprzyjające naprawie bez dodatkowego uwalniania hormonu.
Co to może znaczyć dla przyszłych pokarmów
Dla czytelnika niebędącego specjalistą kluczowa informacja jest taka, że niektóre przyszłe źródła białka mogą być zaprojektowane nie tylko pod kątem niskiego wpływu na klimat, lecz także tak, by aktywnie wspierać zdrowie jelit. U myszy skalowalny komercyjnie lizat McB zarówno przebudowywał odporność w kierunku tolerancji, jak i pomagał jelitu wytrzymać poważne uszkodzenia, poprzez dwa częściowo niezależne mechanizmy: bezpośrednie wzmocnienie regulatorowych komórek T oraz fermentacyjnie napędzaną aktywację receptorów GLP‑2, która wspiera naprawę tkanek. Chociaż konieczne są badania u ludzi, praca sugeruje, że białka pochodzenia mikrobiologicznego mogą stworzyć nową klasę „inteligentnych” pokarmów — zdolnych nas odżywiać, współdziałać z własnymi mikroorganizmami i dyskretnie wzmacniać naturalne mechanizmy ochronne jelit przed zapaleniem.
Cytowanie: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Słowa kluczowe: zapalenie jelit, białko mikrobiologiczne, mikrobiom, receptor GLP-2, komórki T regulatorowe