Clear Sky Science · pl
Lipidy eterowe wpływają na los komórek nowotworowych poprzez modulację pobierania żelaza
Jak mało znany tłuszcz może odsłonić słaby punkt raka
Nowotwór bywa określany jako „choroba genów”, jednak to badanie pokazuje, że tłuszcze tworzące zewnętrzną powłokę komórki mogą być równie istotne. Naukowcy wykryli, w jaki sposób szczególna klasa tłuszczów, zwana lipidami eterowymi, pomaga niebezpiecznym komórkom nowotworowym pobierać żelazo z otoczenia — napędzając zarówno ich zdolność do rozprzestrzeniania się, jak i wrażliwość na nowo rozpoznany rodzaj śmierci komórkowej. Zrozumienie tego ukrytego związku między błonami komórkowymi, żelazem i zachowaniem guza może otworzyć drogę do terapii selektywnie eliminujących najbardziej agresywne komórki nowotworowe.
Inny sposób myślenia o komórkach nowotworowych
Większość badań nad rakiem koncentruje się na mutacjach w DNA i białkach, które one kodują. Ta praca przesuwa uwagę na błonę komórkową — cienką oleistą powłokę otaczającą każdą komórkę. W tej powłoce występuje wiele rodzajów lipidów (tłuszczów), z odmiennymi kształtami i właściwościami fizycznymi. Autorzy skupiają się na lipidach eterowych, które stanowią około jednej piątej fosfolipidów w wielu komórkach ssaków, ale były stosunkowo słabo zbadane. Stwierdzili, że komórki nowotworowe o wysoce przerzutowym, przypominającym komórki macierzyste typie, nasycają swoje błony lipidami eterowymi, co nadaje tym błonom niskie napięcie i wysoką płynność. Te cechy fizyczne z kolei zmieniają sposób, w jaki komórki importują żelazo — metal mogący napędzać zarówno wzrost guza, jak i destrukcyjny proces zwany ferroptozą, żelazozależną formę śmierci komórkowej.
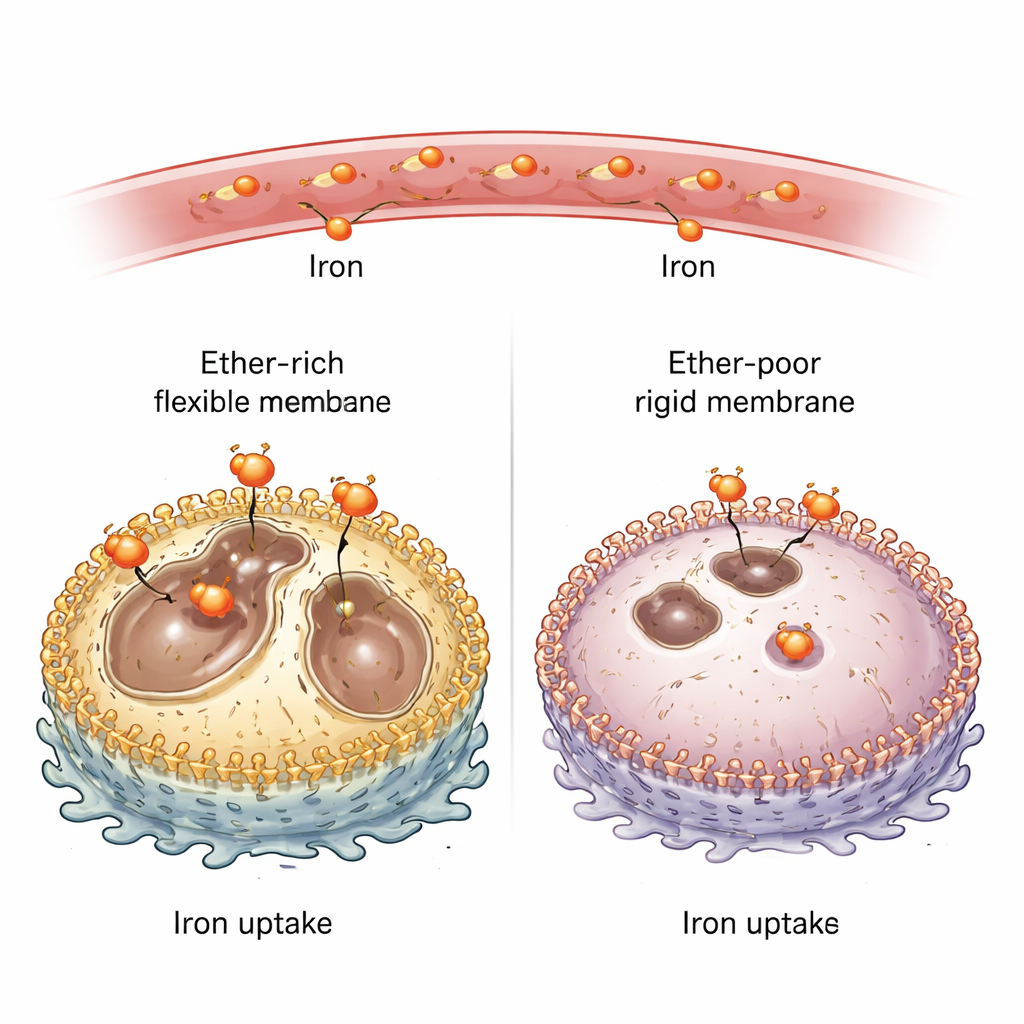
Powiązanie tłuszczów błonowych z pobieraniem żelaza
Aby zbadać rolę lipidów eterowych, zespół usunął kluczowe enzymy niezbędne do ich syntezy w kilku liniach komórkowych mysich i ludzkich. Bez tych enzymów zawartość lipidów eterowych w błonie plazmatycznej spadła z około jednej czwartej wszystkich lipidów do zaledwie kilku procent. Co zaskakujące, komórki ubogie w lipidy eterowe miały znacznie mniej „redoks‑aktywnego” żelaza — postaci chemicznie reaktywnej, uczestniczącej w reakcjach utleniania — zarówno w hodowlach, jak i w implantowanych guzach u myszy. Gdy naukowcy dostarczyli dodatkowe żelazo z zewnątrz, poziomy żelaza w komórkach znów wzrosły i odzyskały one wrażliwość na leki indukujące ferroptozę. To wykazało, że lipidy eterowe robią więcej niż służą jako łatwo utlenialne paliwo — aktywnie kontrolują, ile żelaza dostaje się do wnętrza komórki.
Specjalizowana brama żelazowa: szlak CD44
Następnie badacze zapytali, jak skład błony zmienia pobieranie żelaza. Komórki zwykle importują żelazo przez dobrze znany receptor transferynowy, ale agresywne, przypominające komórki macierzyste komórki nowotworowe polegają także na innym szlaku: białku powierzchniowym o nazwie CD44, które pobiera żelazo związane z polisacharydem hialuronianem. Śledząc fluorescencyjne sondy, zespół pokazał, że usunięcie lipidów eterowych niemal nie wpłynęło na pobieranie przez receptor transferynowy, ale znacząco spowolniło endocytozę zależną od CD44 — alternatywną, niezależną od klatryny drogę wprowadzania materiału do komórki. Przywrócenie lipidów eterowych lub dodanie ich w formie lizosomów ożywiło ten szlak CD44. Zakłócenie samego CD44 lub strawienie hialuronianu obniżało poziom żelaza w komórce, co potwierdza, że ta zależna od eterów droga stanowi główną bramę żelazową w tych komórkach nowotworowych.
Jak miększe błony zmieniają zachowanie komórek
Dlaczego lipidy eterowe mają tak duże znaczenie dla CD44, a nie dla klasycznego receptora żelaza? Odpowiedź leży w fizyce. Korzystając z precyzyjnych narzędzi wyciągających maleńkie pętelki z powierzchni komórki, autorzy wykazali, że błony bogate w etery mają niższe napięcie i są łatwiejsze do odkształcenia. Po usunięciu lipidów eterowych napięcie błony wzrosło, a lipidy upakowały się ściślej, co sprawiło, że błona stała się sztywniejsza. Zmiany te silnie utrudniały formy endocytozy zależne od elastycznych, przypominających tratwy fragmentów błony — dokładnie tego typu, którego używa CD44 — podczas gdy pobieranie zależne od klatryny pozostało w dużej mierze nienaruszone. Lipidy eterowe pomagały także stabilizować „rafty lipidowe”, maleńkie uporządkowane wyspy w błonie, gdzie skupia się CD44 zanim zostanie wciągnięte do wnętrza. Krótko mówiąc, lipidy eterowe dostrajają fizyczny krajobraz błony, sprzyjając pobieraniu żelaza przez CD44.
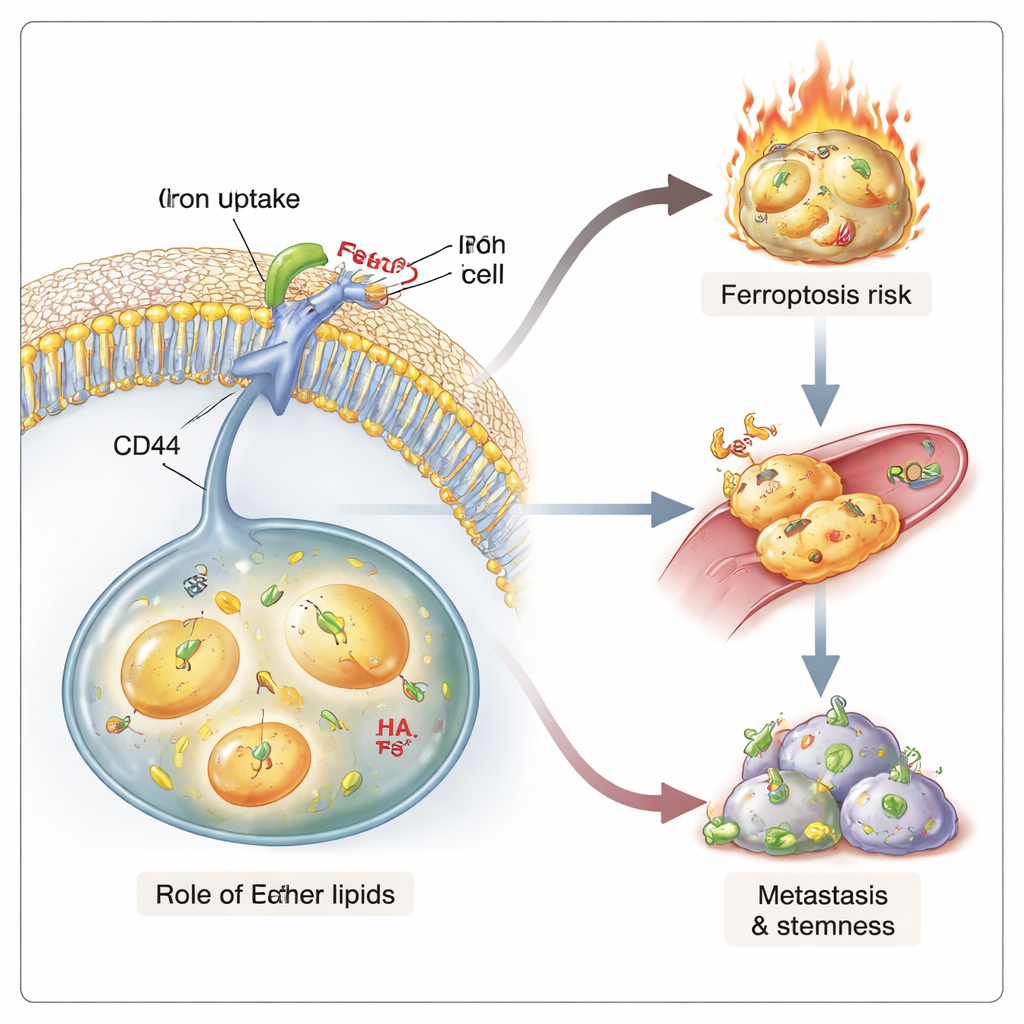
Napędzając zarówno rozprzestrzenianie, jak i autodestrukcję
Wysokie poziomy żelaza i niskie napięcie błony łączą się z cechami, które czynią nowotwory zabójczymi: zdolnością do zasiewania nowych guzów i przetrwania terapii. W trójwymiarowych modelach mikro‑naczyniowych komórki bogate w lipidy eterowe łatwiej przeciskały się z struktur przypominających naczynia krwionośne — wczesny etap przerzutów. U myszy komórki nowotworowe pozbawione eterów tworzyły mniej przerzutów, chociaż ich guzy pierwotne rosły w podobnym tempie. Komórki te wykazywały też obniżoną „macierzystość”, mierzoną zmniejszoną zdolnością do tworzenia mammosfer w hodowli oraz inicjowania guzów w implantach przy rozcieńczeniach ograniczających. Jednocześnie komórki bogate w etery, z wyższym ładunkiem żelaza i bardziej utlenialnymi lipidami, były bardziej podatne na ferroptozę po zastosowaniu specyficznych leków lub sygnałów odpornościowych. Tym samym lipidy eterowe tworzą stan o podwójnym ostrzu: wspierają agresywne, przypominające komórki macierzyste zachowanie, jednocześnie czyniąc te same komórki szczególnie podatnymi na zabicie poprzez uszkodzenia lipidów zależne od żelaza.
Dlaczego to ma znaczenie dla przyszłych terapii przeciwnowotworowych
Dla osób niezaznajomionych z tematem kluczowym przesłaniem jest to, że nie wszystkie komórki nowotworowe są równie niebezpieczne, a ich zewnętrzne błony pomagają określić zarówno ich zagrożenie, jak i podatność. Lipidy eterowe przekształcają powierzchnię komórki tak, że żelazo może napływać przez wyspecjalizowane „drzwi”, napędzając przerzutowe, przypominające komórki macierzyste typy, ale też ładując je składnikami ich własnej destrukcji. Terapie, które zmieniają produkcję lipidów eterowych, zakłócają pobieranie żelaza oparte na CD44 lub precyzyjnie wywołują ferroptozę, mogłyby selektywnie atakować te trudne do leczenia populacje komórek nowotworowych, oszczędzając tkanki prawidłowe. Ujawniając, jak mało znana klasa tłuszczów łączy fizykę błony, metabolizm metali i los komórki, to badanie otwiera nową ścieżkę ku inteligentniejszym, bardziej precyzyjnym interwencjom przeciwnowotworowym.
Cytowanie: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
Słowa kluczowe: lipidy eterowe, komórki macierzyste nowotworu, pobieranie żelaza, ferroptoza, przerzuty