Clear Sky Science · pl
Odkrycie i fenotypowanie transkryptów niekodujących w całym genomie A. fumigatus ujawnia lncRNA związane z wrażliwością na leki przeciwgrzybicze
Dlaczego pleśń w naszych domach ma znaczenie
Większość z nas postrzega pleśń jako uciążliwość na chlebie lub w wilgotnych kątach, ale jeden pospolity grzyb, Aspergillus fumigatus, odpowiada za ponad dwa miliony zgonów rocznie — więcej niż malaria i HIV razem wzięte. Lekarze dysponują wąskim arsenałem leków przeciwgrzybiczych, by kontrolować tego patogena, a oporność na te leki szybko rośnie. W tym badaniu zbadano ukrytą warstwę genomu grzyba — długie RNA niekodujące, zwane lncRNA — które nie kodują białek, a mimo to mogą wpływać na to, jak grzyb reaguje na leczenie. Zrozumienie tych „milczących” elementów genetycznych może otworzyć nowe sposoby przewidywania, monitorowania, a w końcu przeciwdziałania oporności na leki przeciwgrzybicze.
Ukryte wiadomości w DNA grzyba
Klasycznie geny postrzegano jako odcinki DNA kodujące białka, które są wykonawcami funkcji komórkowych. W ciągu ostatniej dekady naukowcy odkryli, że rozległe obszary genomu są transkrybowane do cząsteczek RNA, które nigdy nie stają się białkami. Te długie RNA niekodujące wciąż mogą wpływać na zachowanie komórek, w tym na ich odpowiedź na leki. Choć lncRNA zostały zmapowane u ludzi i drożdży, w patogennych pleśniach takich jak A. fumigatus były w dużej mierze nieznane. Autorzy postanowili to zmienić, budując katalog tych tajemniczych transkryptów obejmujący cały genom i pytając, czy któryś z nich przesuwa równowagę między wrażliwością a opornością na leki.
Słuchając grzyba pod atakiem leków
Aby wykryć lncRNA, zespół wystawił A. fumigatus na działanie sześciu różnych związków przeciwgrzybiczych, w tym powszechnie stosowanych azoli atakujących błonę komórkową grzyba, a następnie sekwencjonował wszystkie powstające RNA. Przy użyciu własnej ścieżki bioinformatycznej zmontowali dziesiątki tysięcy transkryptów i systematycznie odfiltrowali wszystko, co odpowiadało znanym genom kodującym białka lub krótkim RNA „podstawowej obsługi”. Po wielokrotnych rundach filtrowania i ręcznej kuracji uzyskali zestaw wysokiego zaufania 1 089 nowych długich RNA niekodujących rozmieszczonych w całym genomie. Większość znajdowała się między znanymi genami lub nakładała się na nie w przeciwnym kierunku, a łącznie zwiększyły one odsetek genomu grzyba uznanego za aktywnie transkrybowany z około dwóch trzecich do ponad czterech piątych.
Skorelowane odpowiedzi i zachowane „hotspoty”
Porównując, jak te lncRNA zmieniały się pod wpływem różnych dawek leków, badacze zauważyli, że grzyb nie wykorzystuje ich losowo. Zamiast tego lncRNA układały się w około 15 odmiennych wzorców odpowiedzi, niektóre wspólne dla wielu leków, inne specyficzne dla określonych terapii. Na przykład leki uderzające w podobne ścieżki biochemiczne zwykle wywoływały nakładające się sygnatury lncRNA, podczas gdy inhibitor syntezy białek wywołał wiele unikalnych odpowiedzi. Wiele lncRNA leżało bardzo blisko genów już znanych z wpływu na wrażliwość na azole, takich jak te zaangażowane w pobieranie żelaza czy biosyntezę ergosterolu — kluczowego składnika błon komórkowych grzyba. W kilku przypadkach pobliski lncRNA i gen reakcji na leki były jednocześnie w górę lub w dół, co sugeruje, że te elementy niekodujące mogą pomagać koordynować kluczowe programy przetrwania.
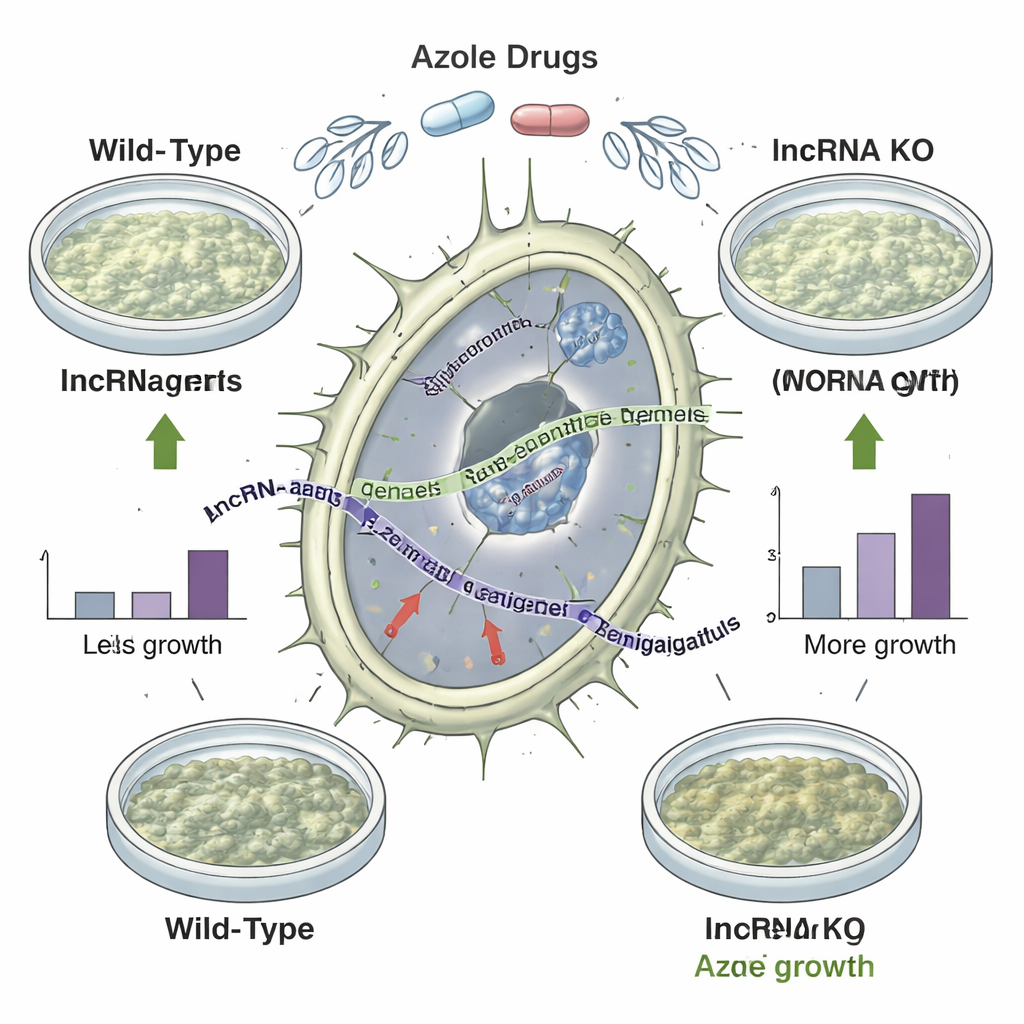
Usuwanie „milczących” genów zmienia wrażliwość na leki
Katalogowanie lncRNA to jedno; udowodnienie ich znaczenia to coś innego. Zespół usunął 92 wybrane regiony lncRNA z genomu grzyba i porównał, jak mutanty rosły pod różnymi stresami, w tym w wysokiej temperaturze, przy niskim poziomie żelaza oraz podczas ekspozycji na trzy różne azole. Sześćdziesiąt mutantów wykazało zmiany kondycji specyficzne dla warunków, a 35 faktycznie rosło lepiej niż szczep wyjściowy w obliczu azoli. Jeden wyróżniający się szczep z delecją wykazał poprawę wzrostu przy wszystkich testowanych azolach, nie będąc przy tym po prostu efektem zwiększonej aktywności pobliskich genów kodujących białka, co mocno sugeruje, że brakujące lncRNA samo w sobie ograniczało tolerancję na leki. Analiza wielu izolatów klinicznych i środowiskowych o znanych profilach wrażliwości na leki wykazała również, że obecność lub brak określonych genów lncRNA korelowała z tym, jak łatwo dany szczep był hamowany przez azole.
Co to oznacza dla walki ze śmiertelnymi zakażeniami grzybiczymi
Dla osób niezwiązanych z tą dziedziną kluczowy przekaz jest taki, że części genomu grzyba kiedyś odrzucane jako „śmieci” aktywnie kształtują, jak niebezpieczny może być A. fumigatus i jak skuteczne są przeciwko niemu nasze leki. Tworząc pierwszą kompleksową mapę długich RNA niekodujących w tym ważnym patogenie i powiązując dziesiątki z nich z mierzalnymi zmianami w odpowiedzi na leki, praca ta otwiera nową klasę markerów genetycznych i potencjalnych celów. W dłuższej perspektywie lncRNA mogą pomóc wyjaśnić, dlaczego niektóre szczepy są naturalnie trudniejsze do leczenia, ukierunkować projekt skuteczniejszych diagnostyk i inspirować terapie, które rozbrajają oporność nie przez bezpośrednie zabijanie grzyba, lecz przez wyciszanie milczących regulatorów, które pomagają mu przetrwać.
Cytowanie: Weaver, D., Qi, T., Chown, H. et al. Genome-wide discovery and phenotyping of non-coding transcripts in A. fumigatus reveals lncRNAs with a role in antifungal drug sensitivity. Nat Commun 17, 1832 (2026). https://doi.org/10.1038/s41467-026-68543-9
Słowa kluczowe: Aspergillus fumigatus, oporność na leki przeciwgrzybicze, długie RNA niekodujące, leki azolowe, genomika grzybów