Clear Sky Science · pl
Wchłanianie polisacharydów z wiązaniami 1,3 i 1,4 w komórkach jelitowych zależy od endocytozy zależnej od klatryny/dynaminy 1/Rab5
Dlaczego duże cukry mają większe znaczenie, niż sądziliśmy
Wiele leków i suplementów diety opartych na cukrach roślinnych i grzybowych (polisacharydach) jest przyjmowanych w postaci tabletek lub proszków. Przez dekady naukowcy zakładali, że te długie, silnie hydrofilowe łańcuchy cukrowe są po prostu za duże, by przejść przez ścianę jelita i dotrzeć do krwiobiegu w niezmienionej postaci. To badanie obala ten dogmat, pokazując, że kilka typów polisacharydów może faktycznie przenikać przez komórki jelitowe, korzystając z wysoko zorganizowanego systemu wnikania komórkowego — otwierając nowe możliwości dla doustnych „leków cukrowych”.
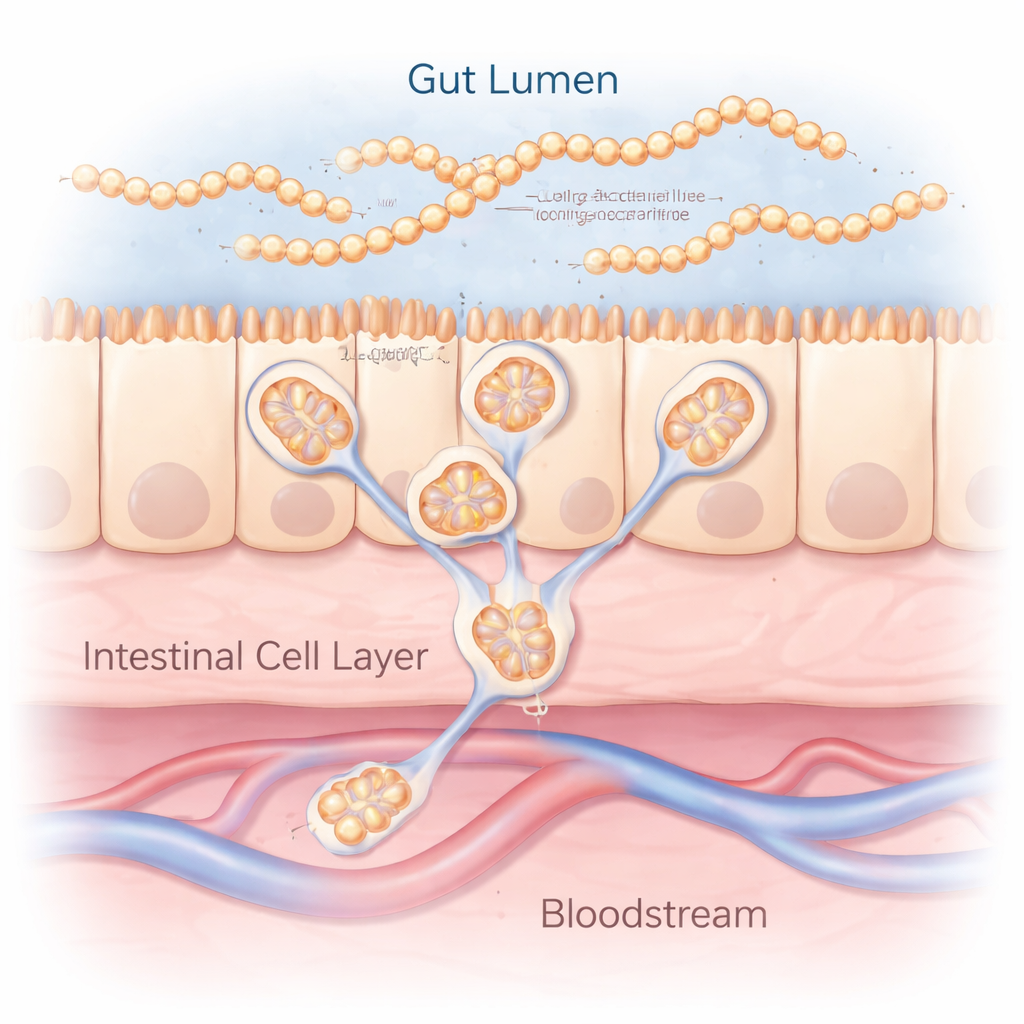
Długie łańcuchy cukrowe, które łamią zasady
Polisacharydy to długie łańcuchy prostych cukrów i są jednym z czterech głównych składników budulcowych życia, obok białek, tłuszczów i DNA. Już stanowią podstawę dziesiątek leków, od środków przeciwzakrzepowych, takich jak heparyna, po preparaty wspierające stawy, jak siarczan chondroityny. Większość z nich podawana jest jednak dożylnie, ponieważ ich masywna wielkość i silne powinowactwo do wody uważano za przeszkodę w doustnym wchłanianiu. Autorzy podważają ten pogląd, badając panel naturalnych polisacharydów o różnych typach wiązań i ładunkach elektrycznych, w tym pochodny z grzybów beta-glukan (GFPBW1) oraz pochodny z roślin alfa-glukan (WGE) stosowane jako związki modelowe.
Przejście przez ścianę jelita bez rozpadu
Pierwsze eksperymenty polegały na sprawdzeniu, czy te duże cukry mogą przenikać przez warstwę komórek o cechach jelitowych hodowanych na membranie. Przy użyciu chemicznych znaczników i chromatografii stwierdzono, że kilka polisacharydów przemieszcza się przez warstwę komórek z zaskakująco wysoką wydajnością. Co ważne, ich „odciski palców” przed i po transporcie były niemal identyczne, co sugeruje, że łańcuchy nie musiały być rozdrabniane na małe fragmenty, aby przeniknąć. Naukowcy przeszli następnie do badań na żywych szczurach i myszach, podając doustnie znakowane wersje GFPBW1 i WGE. W próbkach krwi i w tkance wątroby wykryto niezmienione, znakowane polisacharydy — ponownie z jedynie minimalnymi zmianami rozmiaru — co dowodzi, że przynajmniej część tych dużych cząsteczek przetrwa trawienie, przekroczy wyściółkę jelita i wejdzie do krążenia.
Brama ładunku komórkowego: endocytoza zależna od klatryny
Jak tak duże cząsteczki przechodzą przez pojedyncze komórki jelitowe? Badanie wskazuje na drogę importu komórkowego zwaną endocytozą zależną od klatryny, proces zwykle wykorzystywany do internalizacji hormonów, składników odżywczych, a nawet wirusów. Pod mikroskopem napływające polisacharydy współlokalizowały się z klatryną, białkiem rusztowania, które kształtuje małe zagłębienia wpuklające się do wnętrza błony komórkowej. Gdy badacze blokowali klatrynę za pomocą środków chemicznych lub zmniejszali jej ciężki łańcuch (CLTC) przy użyciu narzędzi genetycznych, wchłanianie cukrów w hodowanych komórkach spadało gwałtownie. Myszy genetycznie zmodyfikowane tak, aby nie posiadały klatryny specyficznie w wyściółce jelita, wchłaniały znacznie mniej polisacharydu po podaniu doustnym. Testy wiązania fizycznego dodatkowo wykazały, że polisacharydy modelowe mogą przyłączać się bezpośrednio do klatryny, co wzmacnia hipotezę, że korzystają z tego systemu krytych dołków.
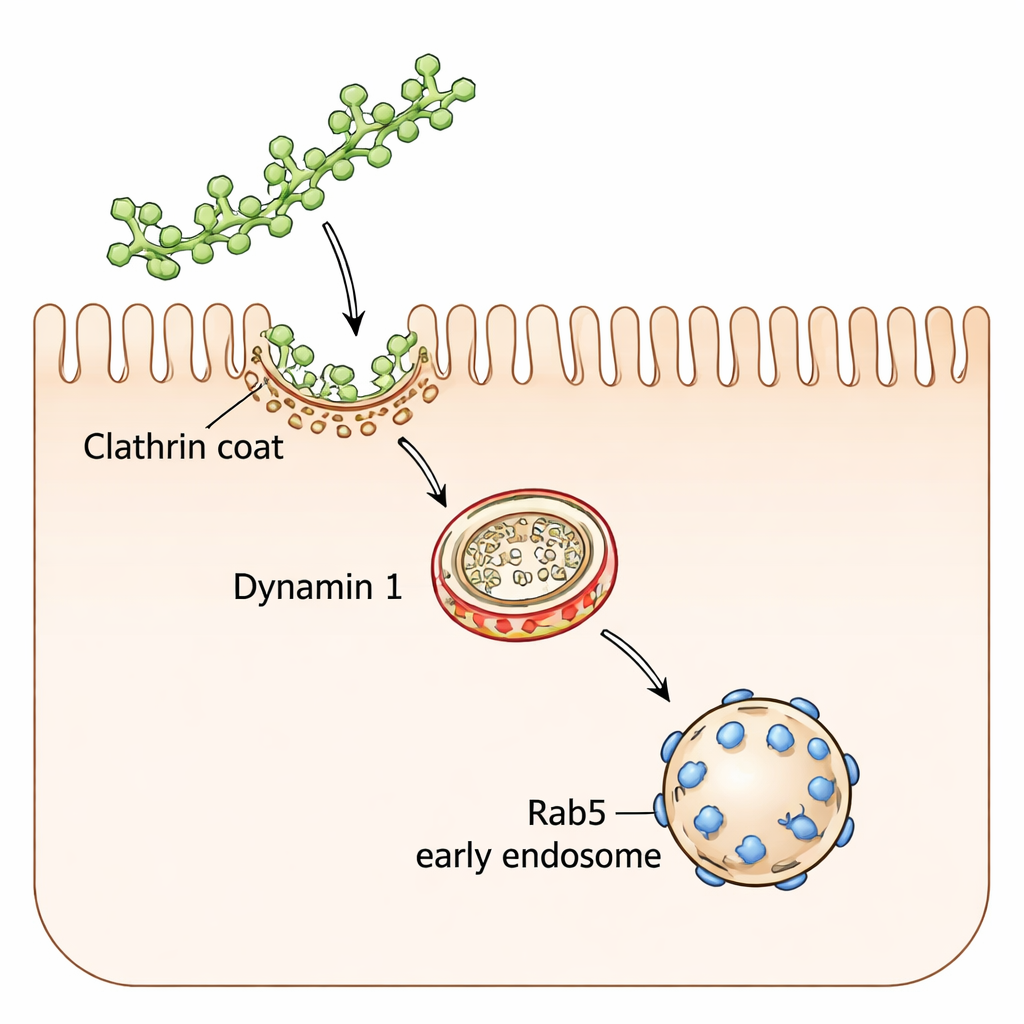
Kluczowi pomocnicy i sygnały wewnątrz komórki
Klatryna nie działała samotnie. Białko dynamina 1, które zaciska się jak pierścień odcinający pączkujące pęcherzyki, okazało się niezbędne: hamowanie lub wyciszanie dynaminy 1 ograniczało wejście polisacharydów, podczas gdy zwiększenie jej poziomów zwiększało wchłanianie. Kolejnym partnerem był Rab5 — regulator wczesnych endosomów, początkowych stacji sortujących komórki — który także był kluczowy. Internalizowane polisacharydy często współlokalizowały się z Rab5, a zwierzęta pozbawione Rab5 we wszystkich tkankach wykazywały znacznie zredukowane wchłanianie jelitowe. Po dostaniu się do wnętrza cukry przemieszczały się przez sieć przedziałów komórkowych, w tym wczesne endosomy, lizosomy (centra recyklingu komórkowego), aparat Golgiego i retikulum endoplazmatyczne, choć dokładna trasa różniła się między normalnymi komórkami jelitowymi a komórkami przypominającymi nowotworowe.
Swoiste receptory na powierzchni komórek jako „stacje dokujące” dla cukrów
Badanie ujawniło również warstwę selektywności. Niektóre receptory błonowe — białka wyczuwające sygnały poza komórką — były potrzebne dla określonych polisacharydów. Receptor immunologiczny Dectin-1 był ważny dla beta-glukanu GFPBW1, podczas gdy receptor dla czynników wzrostu BMPRIA odgrywał znaczącą rolę w pobieraniu WGE. Receptor naskórkowego czynnika wzrostu (EGFR) również wspierał wejście obu cukrów, choć bez zawsze wykrywalnego bezpośredniego wiązania fizycznego, co sugeruje bardziej złożone, pośrednie mechanizmy. Gdy te receptory były wyciszane, wchłanianie odpowiadających im polisacharydów malało; gdy były nadmiernie produkowane, wchłanianie wzrastało. Ponadto dwie główne ścieżki sygnalizacyjne wewnątrz komórek, Wnt/β-katenina i NF-κB, pomagały regulować gotowość komórek do internalizacji cukrów.
Co to oznacza dla przyszłych tabletek i proszków
Podsumowując, praca pokazuje, że niektóre duże, naturalne polisacharydy mogą być pobierane w niezmienionej formie z jelita do krwiobiegu za pomocą skoordynowanego systemu opartego na klatrynie, dynaminie 1, Rab5 i specyficznych receptorach błonowych. Dla osób niebędących specjalistami kluczowy komunikat brzmi: „za duże, by się wchłonąć” nie jest sztywną zasadą — nasze komórki jelitowe mają aktywne bramy, które potrafią importować niektóre złożone cukry. Zrozumienie tych bram i ich białkowych pomocników może ukierunkować projektowanie nowych, doustnie dostępnych leków i suplementów opartych na polisacharydach, które wiarygodnie docierają do celów w całym organizmie, potencjalnie eliminując konieczność wstrzyknięć w niektórych terapiach.
Cytowanie: Liao, W., Cao, D., Wang, Y. et al. 1,3-and 1,4-linked polysaccharides uptake in intestinal cells relies on clathrin/dynamin 1/Rab5-dependent endocytosis. Nat Commun 17, 1831 (2026). https://doi.org/10.1038/s41467-026-68542-w
Słowa kluczowe: wchłanianie polisacharydów, endocytoza jelitowa, klatryna dynamina Rab5, doustne leki węglowodanowe, wchłanianie beta-glukanu