Clear Sky Science · pl
Wysoce selektywna i praktyczna hydrogenacja funkcjonalizowanych (hetero)arenów
Od płaskich cząsteczek do trójwymiarowych bloków budulcowych
Współczesne leki, tworzywa sztuczne i wiele codziennych chemikaliów powstają z małych „klocków Lego” molekularnych. Większość z tych elementów ma postać płaskich pierścieni zwanych arenami, które chemicy cenią za łatwość syntezy i modyfikacji. Jednak poszukiwacze leków i naukowcy zajmujący się materiałami coraz częściej potrzebują kształtów bardziej trójwymiarowych, które często lepiej zachowują się w organizmach i poprawiają właściwości tworzyw. Artykuł opisuje nowe, praktyczne podejście do przekształcania płaskich pierścieni w precyzyjne struktury 3D przy użyciu odpornego katalizatora platynowego, otwierając prostszą drogę do leków następnej generacji i bezpieczniejszych dodatków do tworzyw.
Dlaczego kształt ma znaczenie w chemii molekularnej
Płaskie pierścienie aromatyczne występują wszędzie: w farmaceutykach, agrochemikaliach, witaminach i polimerach. Ich popularność sprawia, że są tanie i powszechnie dostępne. Natomiast ich „nasycone” odpowiedniki — pierścienie, z których usunięto wiązania podwójne — są znacznie mniej rozpowszechnione komercyjnie, mimo że dają istotne korzyści. Gdy pierścień staje się nasycony i trójwymiarowy, chemicy zyskują znacznie precyzyjniejszą kontrolę nad właściwościami, takimi jak dopasowanie leku do kieszeni białkowej czy sposób, w jaki tworzywo się zgina i zmiękcza. Na przykład poprzez regulację stosunku między dwiema lustrzanymi konfiguracjami 3D (zwanymi formami cis i trans) producenci polimerów mogą dopasować temperaturę przejścia szkła, która decyduje, czy materiał jest sztywny czy elastyczny w danej temperaturze.
Wyzwanie związane z nadaniem kształtu płaskim pierścieniom
Przekształcenie płaskiego pierścienia aromatycznego w trójwymiarowy pierścień nasycony brzmi prosto — wystarczy dodać wodór. W praktyce jest to bardzo trudne. Pierścienie aromatyczne są wyjątkowo stabilne, więc naruszenie ich „aromatyczności” wymaga dużej ilości energii. Jednocześnie rzeczywiste cząsteczki często niosą dodatkowe grupy funkcjonalne, takie jak estry czy amidy, które muszą pozostać nienaruszone. Katalizator musi więc spełniać trzy warunki jednocześnie: aktywować oporne pierścienie w łagodnych warunkach, ignorować inne wrażliwe fragmenty cząsteczki oraz układać dodawane atomy wodoru tak, by jedna forma 3D była wyraźnie preferowana. Istniejące systemy, które to potrafią, są zwykle skomplikowane, wrażliwe i trudne do odzyskania, co czyni je nieatrakcyjnymi dla zastosowań przemysłowych na dużą skalę.
Odporne cząstki platyny osadzone na znanym nośniku
Badacze opisują prosty katalizator heterogeniczny: drobne cząstki platyny osadzone na tlenku tytanu (Pt/TiO2). Dzięki temu materiałowi potrafią hydrogenować szeroką gamę wielo podstawionych arenów i heteroarenów — pierścieni zawierających także atomy takie jak azot czy tlen — w stosunkowo łagodnych warunkach temperatury i ciśnienia wodoru. Co ważne, reakcje silnie faworyzują jedną trójwymiarową konfigurację, często osiągając stosunek diastereomerów nawet 99:1 na korzyść formy cis. W odróżnieniu od wielu wcześniejszych systemów katalizator jest stały, łatwy do odfiltrowania i nadaje się do wielokrotnego użycia. Pozostawia też nietknięte delikatne grupy, takie jak estry, estry boronowe i amidy, co jest kluczowe, gdy pierścień jest częścią złożonego leku lub funkcjonalnego materiału.
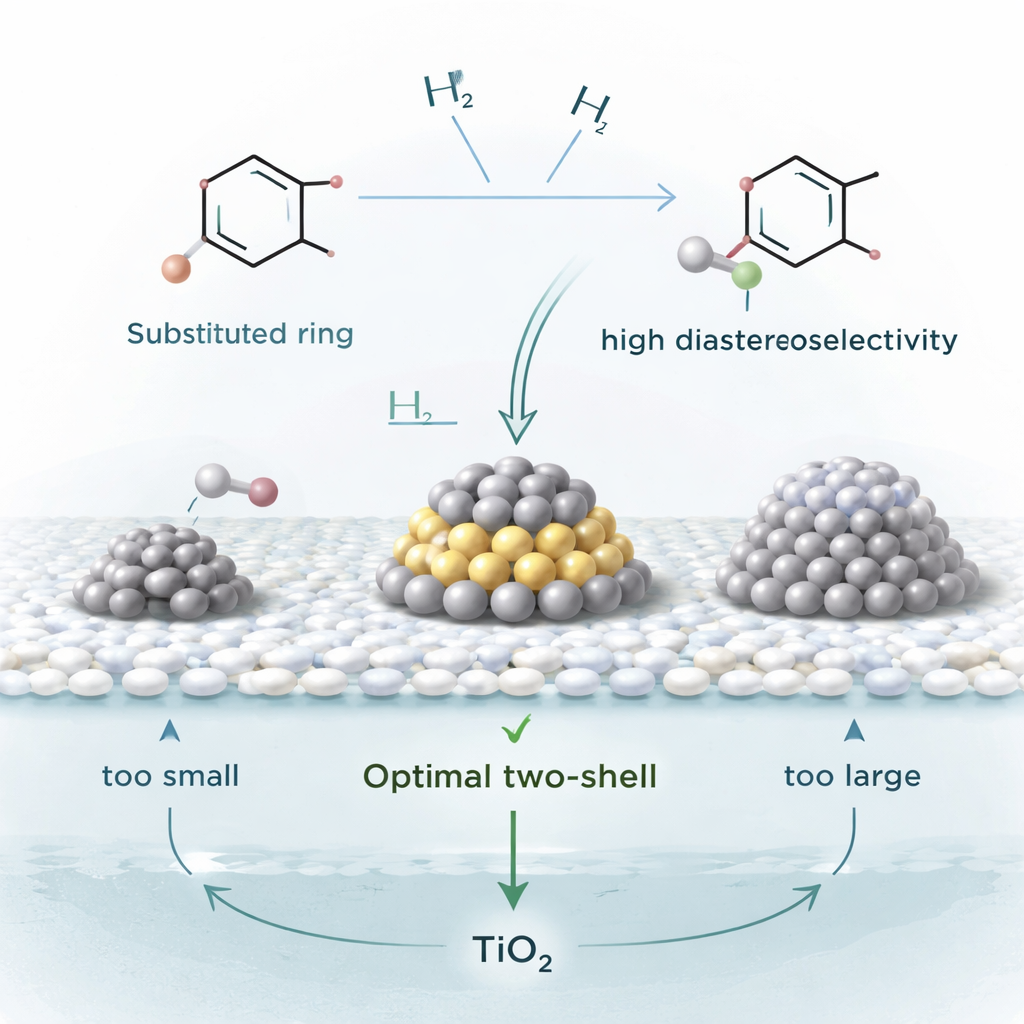
Analiza słodkiego punktu aktywności
Aby zrozumieć, dlaczego ten katalizator działa tak dobrze, zespół zbadał reakcję modelową: przemianę dimetylortoftalanu, powszechnego chemika przemysłowego, w jego nasycony odpowiednik. Przygotowując Pt/TiO2 o różnych zawartościach platyny i mierząc szybkości reakcji, odkryli, że najwyższa aktywność występuje, gdy cząstki platyny mają bardzo specyficzny, pośredni rozmiar. Obrazy z mikroskopii elektronowej i symulacje komputerowe wykazały, że cząstki o tzw. strukturze dwuwarstwowej — na tyle duże, by jednocześnie pomieścić płaski pierścień i wodór, ale nie tak duże, by pierścień wiązał się zbyt słabo — stanowią prawdziwy „słodki punkt”. Mniejsze klastry są blokowane przez silnie przylegający pierścień, podczas gdy znacznie większe cząstki nie chwytają pierścienia dostatecznie mocno, by tłumaczyć zaobserwowane zachowanie.
Od reakcji modelowych do produktów użytecznych w praktyce
Uzbrojeni w tę wiedzę, naukowcy sprawdzili zakres zastosowań katalizatora. Skutecznie przekształcili wiele różnych pochodnych benzenu oraz układów z pierścieniami połączonymi lub naprężonymi, zwykle uzyskując wysokie wydajności i silne preferencje dla produktów cis. Co istotne dla chemii medycznej, zastosowali też metodę do heteroarenów zawierających azot, które są blokami budulcowymi ważnych leków, w tym pośredników związanych z antybiotykiem moksifloksacyną. Aby pokazać znaczenie przemysłowe, przeprowadzili reakcję w skali kilogramowej, przekształcając komercyjny plastyfikator ftalanowy w alternatywę wolną od ftalanów w warunkach bezrozpuszczalnikowych, otrzymując niemal wyłącznie pożądaną formę cis i wykazując, że katalizator można wielokrotnie odzyskiwać.
Co to oznacza dla codziennej chemii
Mówiąc prosto, praca dostarcza chemikom solidne, wielokrotnego użytku narzędzie do przekształcania powszechnych płaskich pierścieni w bardziej trójwymiarowe, precyzyjnie zdefiniowane formy, bez długich, złożonych dróg syntezy. Wskazanie dokładnie, które struktury platynowe wykonują zasadniczą pracę, otwiera drogę do racjonalnego projektowania jeszcze lepszych katalizatorów. Bezzwłoczny wpływ może obejmować szybsze drogi do nowych kandydujących związków farmaceutycznych, bezpieczniejsze i lepiej dostrajane plastyfikatory oraz wydajniejsze wykorzystanie wodoru w syntezie chemicznej — wszystko to osiągalne za pomocą stosunkowo prostego katalizatora stałego, który dobrze wpisuje się w istniejące procesy przemysłowe.
Cytowanie: Qu, R., Jena, S., Xiao, L. et al. Highly selective and practical hydrogenation of functionalized (hetero)arenes. Nat Commun 17, 2015 (2026). https://doi.org/10.1038/s41467-026-68537-7
Słowa kluczowe: hydrogenacja arenów, katalizator platynowy, trójwymiarowe rusztowania molekularne, heteroareny, synteza plastyfikatorów