Clear Sky Science · pl
Interakcja pętli 3 sclerostyny z LRP4 w adipocytach wymagana przez sclerostynę do zaburzania ogólnoustrojowego metabolizmu lipidów i glukozy
Dlaczego kości mają znaczenie dla poziomu cukru we krwi
Większość ludzi myśli o kościach jako o martwym rusztowaniu, ale komórki kostne cicho uwalniają hormony, które komunikują się z resztą organizmu. To badanie ujawnia, jak jeden z takich białek kostnych, zwany sclerostyną, łączy dwa bardzo powszechne problemy u starszych kobiet: kruchość kości (osteoporozę) i cukrzycę typu 2. Odkrywając specyficzne „uściśnięcie dłoni” między sclerostyną a komórkami tłuszczowymi, naukowcy opisują sposób na wzmocnienie kości i poprawę kontroli glukozy i cholesterolu bez obciążania serca.
Sygnał z kości, który idzie nie tak
Sclerostyna to białko produkowane głównie przez komórki kostne. Normalnie hamuje tworzenie kości i, co nieco zaskakujące, pomaga także chronić naczynia krwionośne. Zespół skupił się na małym fragmencie tego białka, zwanym pętlą3, i sprawdził, czy odgrywa rolę w zaburzonym gospodarowaniu tłuszczami i cukrem. Stwierdzili, że kobiety z osteoporozą pomenopauzalną, które jednocześnie miały cukrzycę typu 2, jak również osoby niedawno zdiagnozowane z cukrzycą, miały wyższe stężenia sclerostyny we krwi niż porównywalne osoby bez cukrzycy. U myszy karmionych dietą wysokotłuszczową, symulującą stres metaboliczny, poziomy sclerostyny również rosły wraz ze wzrostem masy ciała, wyższymi poziomami lipidów we krwi i gorszą kontrolą glikemii. Te wzorce sugerowały, że nadmiar sclerostyny może być czymś więcej niż biernym obserwatorem w chorobie metabolicznej.
Rozplątywanie małej pętli o dużych skutkach
Aby zrozumieć, co robi pętla3, naukowcy stworzyli myszy, u których sclerostyna była zmieniona lub których fragment pętli3 został usunięty. Myszy nadprodukujące normalną sclerostynę odkładały więcej tłuszczu w białych tkankach tłuszczowych, miały większe komórki tłuszczowe, wyższe poziomy wolnych kwasów tłuszczowych w krążeniu oraz gorszą tolerancję glukozy i odpowiedź insulinową niż myszy kontrolne. Gdy pętla3 została genetycznie usunięta lub subtelnie zmutowana, te problemy ustępowały: poduszeczki tłuszczowe były mniejsze, komórki tłuszczowe zmniejszały się, poziom lipidów we krwi spadał, a gospodarka cukrowa ulegała poprawie. Co godne uwagi, podobne korzyści pojawiły się, gdy myszy leczono specjalnie zaprojektowanym lekiem przypominającym DNA (aptamerem), który wiąże się z pętlą3 i uniemożliwia jej działanie, bez zmiany ilości sclerostyny we krwi.
Jak komórki tłuszczowe „słyszą” sygnał z kości
Zespół następnie przyjrzał się z bliska komórkom tłuszczowym, aby zobaczyć, jak pętla3 przekazuje swój szkodliwy komunikat. Skoncentrowali się na białku-receptorze na powierzchni adipocytów zwanym LRP4, wcześniej znanym z udziału w działaniu sclerostyny na kości. W eksperymentach na hodowlach komórkowych pokazali, że pętla3 fizycznie wiąże się ze specyficzną częścią LRP4 na komórkach tłuszczowych. Ten kontakt wywoływał zmiany zwiększające zdolność komórek do syntezy i rozkładu tłuszczów oraz do pobierania większej ilości glukozy z krwi, prowadząc do przerośniętych, nadaktywnych adipocytów. Gdy naukowcy subtelnie zmienili kluczowe elementy LRP4 tak, by pętla3 nie mogła się już zakotwiczyć, lub dodali mały blokujący peptyd naśladujący miejsce wiązania LRP4, wpływ sclerostyny na gromadzenie tłuszczu i wychwyt glukozy został w znacznej mierze osłabiony. Zarówno w komórkach, jak i u myszy, zablokowanie tej interakcji pętla3–LRP4 przywracało bardziej normalny rozmiar komórek tłuszczowych i poprawiało tolerancję glukozy.
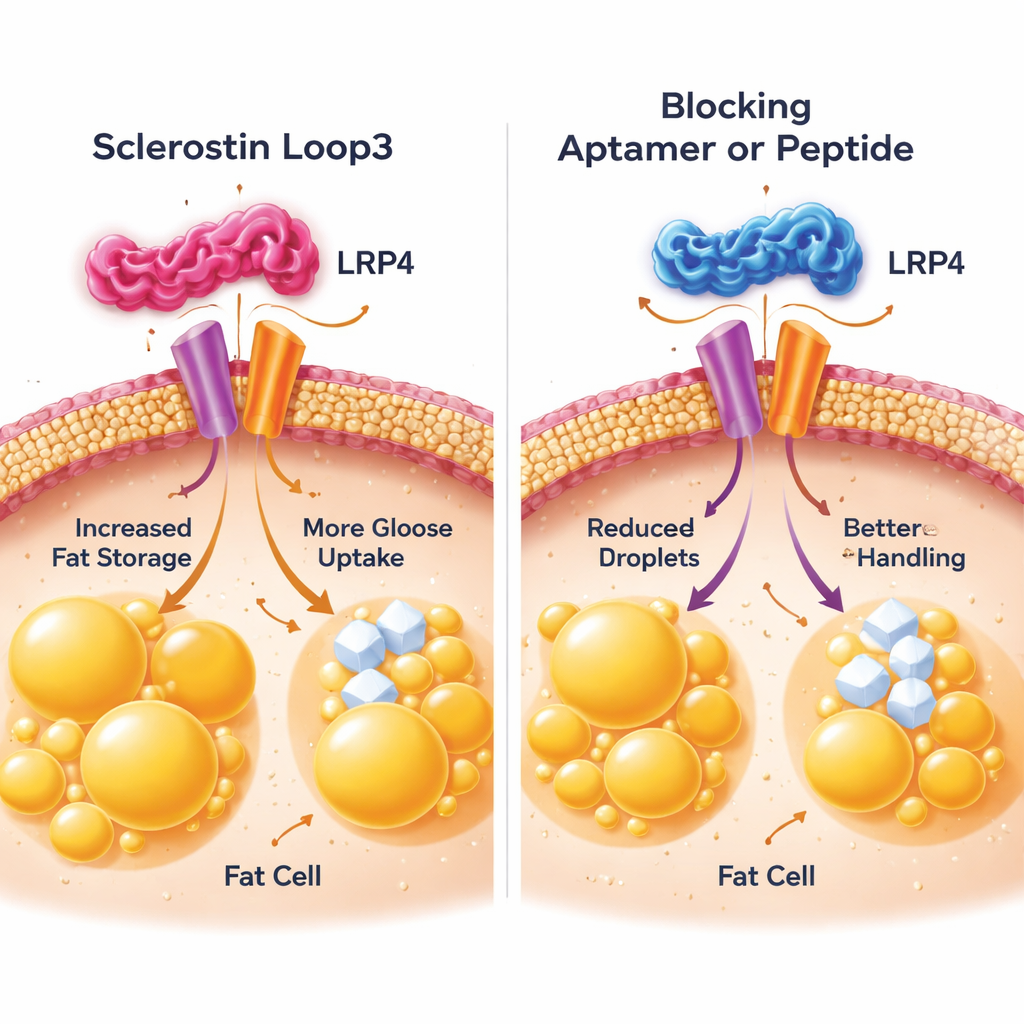
Mocniejsze kości, zdrowszy metabolizm
Istotnym problemem istniejących leków blokujących sclerostynę przy osteoporozie jest to, że choć zwiększają masę kostną i poprawiają metabolizm, organy regulacyjne ostrzegały o podwyższonym ryzyku poważnych problemów sercowo-naczyniowych. Wcześniejsze prace tego zespołu pokazały, że pętla3 jest kluczowa dla hamującego działania sclerostyny na tworzenie kości, ale nie dla jej właściwości chroniących serce. Tutaj autorzy dodatkowo wykazują, że celowanie w pętlę3 — zarówno poprzez modyfikacje genetyczne, jak i leki ukierunkowane na pętlę3 — poprawia ogólnoustrojowy metabolizm tłuszczów i cukrów w kilku modelach mysich, jednocześnie zwiększając masę i wytrzymałość kości. W przeciwieństwie do obecnych leków, ta strategia nie wywołała kompensacyjnego wzrostu innego inhibitora związanego z kośćmi, DKK1, który może osłabiać długoterminowe korzyści.
Co to może oznaczać dla pacjentów
Mówiąc dobitnie, badanie dowodzi, że bardzo mały fragment jednego hormonu kostnego pomaga napędzać zarówno złą kondycję kości, jak i chorobę metaboliczną, komunikując się bezpośrednio z komórkami tłuszczowymi. Przerywając rozmowę między segmentem pętla3 sclerostyny a receptorem LRP4 na adipocytach, może być możliwe zaprojektowanie terapii, które wzmocnią kości i znormalizują poziomy tłuszczów i cukrów we krwi, jednocześnie zachowując ochronne dla serca funkcje sclerostyny. Dla kobiet pomenopauzalnych, które często zmagają się jednocześnie z osteoporozą i cukrzycą typu 2, terapie ukierunkowane na pętlę3 mogłyby kiedyś zaoferować bezpieczniejszy, trwalszy sposób leczenia obu schorzeń naraz.
Cytowanie: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
Słowa kluczowe: sclerostyna, pętla3, LRP4, osteoporoza, cukrzyca typu 2