Clear Sky Science · pl
Kwas palmitynowy wywołujący palmitoilację B7H3 sprzyja ucieczce przed układem odpornościowym
Dlaczego to badanie ma znaczenie dla pacjentów z rakiem
Wiele osób słyszało, że nowe leki immunoterapeutyczne mogą pomóc układowi odpornościowemu zwalczać raka, jednak wielu pacjentów z powszechnym rakiem jelita grubego zyskuje z tego niewiele. To badanie odsłania ukryty trik biochemiczny, którego guzy jelita używają, by chronić się przed atakiem immunologicznym, i wskazuje nowy typ leku — mały peptyd — który mógłby zwiększyć skuteczność immunoterapii u tych pacjentów.
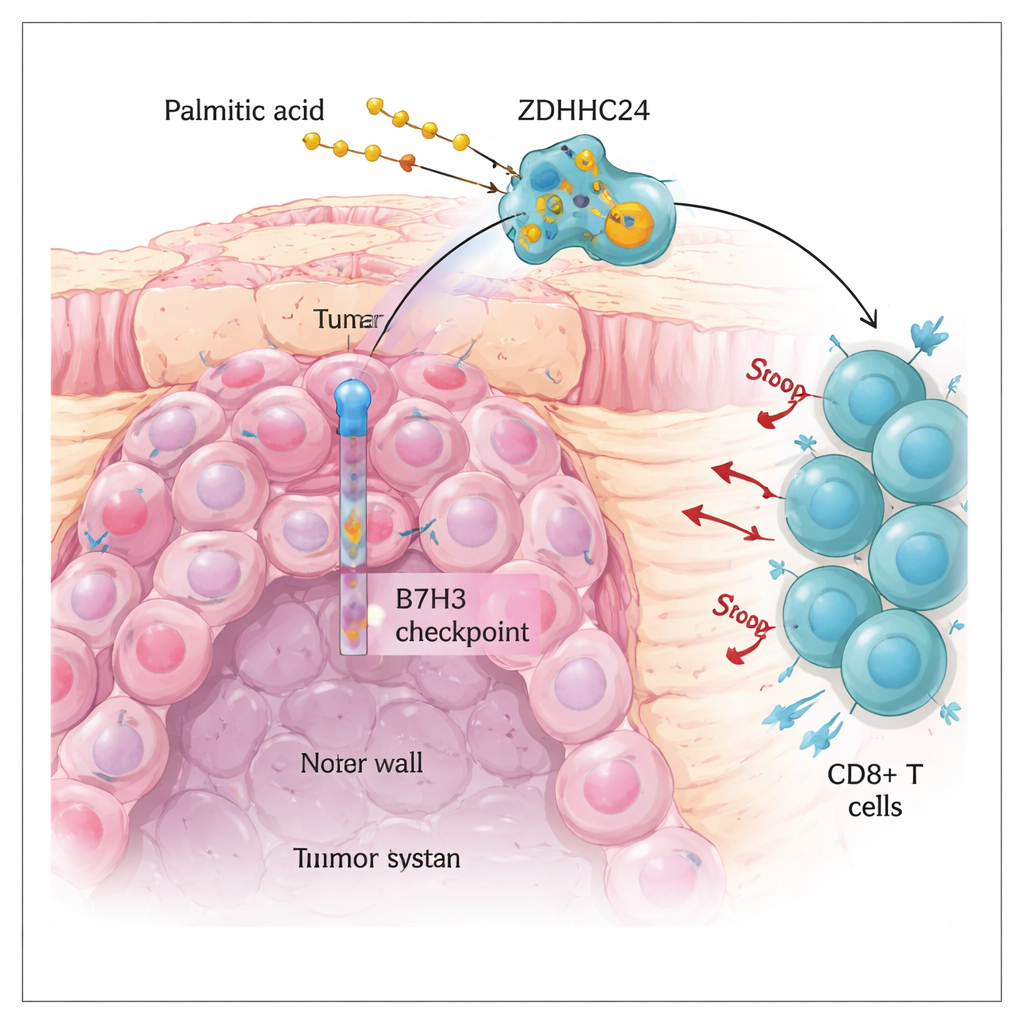
Bariera w obecnej immunoterapii raka jelita
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie. Leki immunoterapeutyczne uwalniające „hamulce” odporności, takie jak inhibitory PD‑1 i PD‑L1, zrewolucjonizowały leczenie u niewielkiej grupy pacjentów, których guzy mają wiele błędów DNA (tzw. guzy MSI‑H). Niestety większość raków jelita grubego jest stabilna mikrosatelitarnie (MSS) i słabo odpowiada na te terapie. Autorzy skupili się na innym białku‑hamulcu zwanym B7H3, które znajduje się na powierzchni komórek nowotworowych i tłumi aktywność komórek zabójczych, zwłaszcza limfocytów CD8+. Stwierdzili, że poziom białka B7H3 jest wyraźnie podwyższony w guzach MSS i wiąże się z gorszym przeżyciem, mimo że gen kodujący B7H3 nie wykazuje zwiększonej aktywności. Ta rozbieżność postawiła istotne pytanie: co utrzymuje tak wysoką obfitość białka B7H3 na komórkach nowotworowych?
Jak powszechny tłuszcz pomaga guzem się ukryć
Zespół podejrzewał, że metabolizm guza może stabilizować B7H3. Porównując aktywność genów i profile małych cząsteczek w guzach MSS i MSI‑H, odkryli różnice w wielu szlakach związanych z lipidami, a wyróżniającym się kwasem tłuszczowym okazał się kwas palmitynowy. Gdy w laboratorium eksponowali komórki raka jelita na różne produkty rozpadu tłuszczów, tylko kwas palmitynowy wywołał wyraźny wzrost poziomu białka B7H3. Dalsze eksperymenty wyjaśniły mechanizm: kwas palmitynowy bierze udział w procesie chemicznej modyfikacji zwanej palmitoilacją, w którym łańcuch tłuszczowy przyłączany jest do określonych miejsc w białkach. Ta modyfikacja, przeprowadzana przez enzym ZDHHC24 w pojedynczym reszcie cysteiny w B7H3, uczyniła B7H3 bardziej stabilnym i bardziej obfitym na powierzchni komórek nowotworowych.
Blokowanie drogi do „śmietnika” dla białka‑hamulca
Komórki zwykle usuwają niechciane lub uszkodzone białka za pomocą systemów przypominających recykling i wywóz śmieci. Badacze wykazali, że B7H3 jest głównie rozkładane przez komórkową ścieżkę „autofagii”, która używa receptora SQSTM1/p62 do znakowania ładunku do zniszczenia. Gdy B7H3 było palmitoilowane, wiązało się słabiej z tym receptorem i uchodziło przed degradacją autofagową, co prowadziło do utrzymująco się wysokiego poziomu białka‑hamulca. Gdy miejsce palmitoilacji zostało zmutowane tak, że nie mogło już nosić tłuszczowej „etykiety”, albo gdy usunięto enzym ZDHHC24, B7H3 było wydajniej kierowane do komórkowych „worków na śmieci” i rozkładane. U myszy guzy pozbawione palmitoilowanego B7H3 rosły wolniej, nie zmieniając swojej wewnętrznej szybkości wzrostu w organizmach z niedoborem układu odpornościowego, i wykazywały dramatycznie więcej limfocytów CD8+ oraz silniejszą aktywność zabijania guza. To pokazało, że ta modyfikacja działa głównie przez obezwładnianie odpowiedzi immunologicznej, a nie przez zmianę tempa podziałów komórkowych raka.
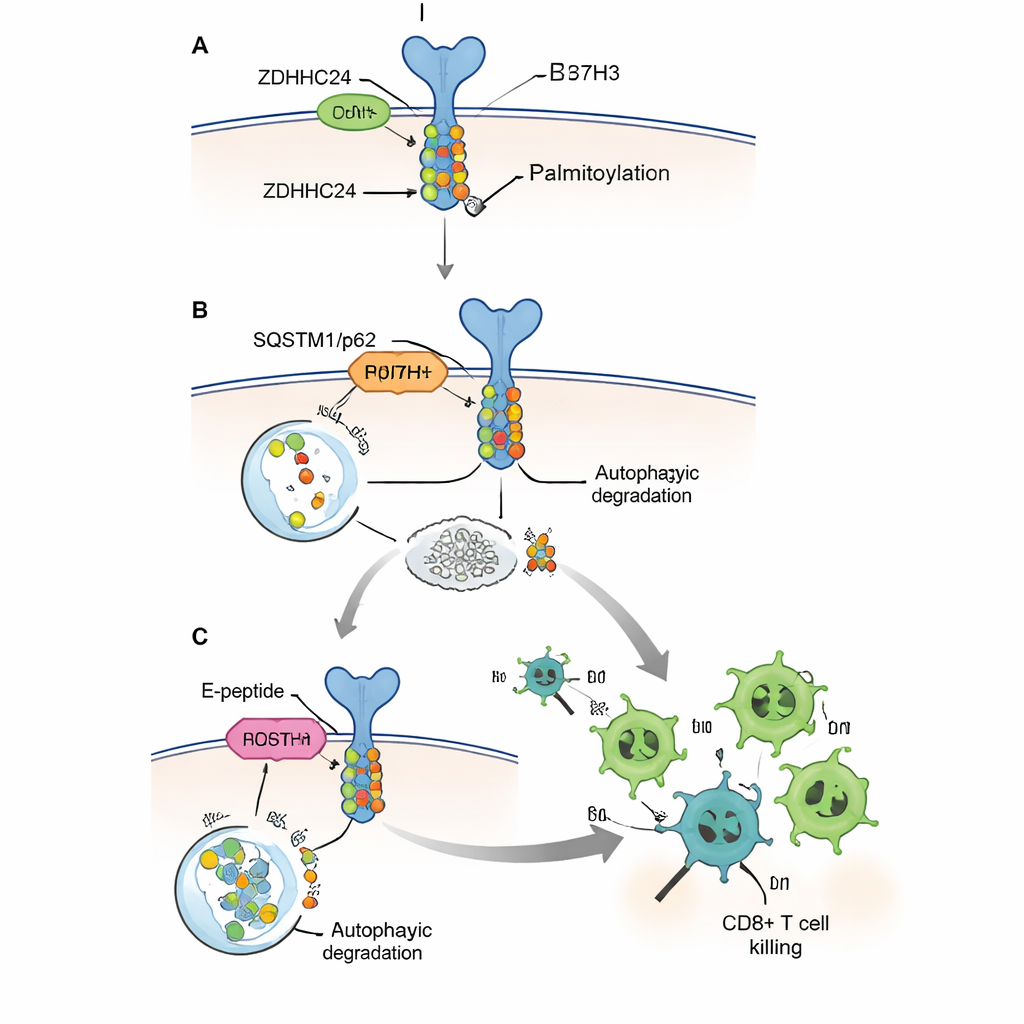
Ściszenie tarczy i wzmocnienie limfocytów T
Ponieważ całkowite wyeliminowanie ZDHHC24 lub B7H3 za pomocą metod genetycznych nie jest praktycznym rozwiązaniem u pacjentów, autorzy zaprojektowali krótki, przenikający do komórek peptyd, który nazwali peptydem E. Naśladuje on niewielki fragment białka B7H3, który normalnie wiąże się z ZDHHC24, działając jako wabik, który uniemożliwia enzymowi modyfikowanie prawdziwych cząsteczek B7H3. W hodowlach komórkowych peptyd E zmniejszał palmitoilację i poziomy białka B7H3, przywracał jego rozpoznanie przez maszynerię autofagową i umożliwiał ludzkim limfocytom CD8+ skuteczniejsze niszczenie komórek nowotworowych. W kilku modelach mysich, w tym u myszy humanizowanej niosącej ludzkie komórki odpornościowe i ludzkie nowotwory jelita, wstrzyknięcia peptydu E zmniejszały guzy, zwiększały liczbę limfocytów CD8+ w ich wnętrzu oraz nasilały produkcję kluczowych cząsteczek zabójczych, takich jak granzyme B i interferon‑gamma.
Nowy partner dla istniejącej immunoterapii
Na koniec badacze sprawdzili, czy ta strategia mogłaby działać razem ze standardowym blokowaniem PD‑1. W modelach mysich raka jelita zarówno sam peptyd E, jak i przeciwciało przeciw PD‑1 dawały pewną kontrolę nad guzem. Jednak połączenie obu terapii przyniosło znacznie silniejsze i dłużej utrzymujące się zahamowanie wzrostu nowotworu, w niektórych przypadkach powodując znikanie guzów i ponad dwukrotne wydłużenie średniego przeżycia w porównaniu do kontrolnych grup. Sugeruje to, że unieszkodliwienie „tarczy” B7H3 przez odcięcie jej tłuszczowego „kotwicznego” elementu może uzupełniać istniejące leki punktów kontrolnych działające na szlak PD‑1.
Co to oznacza dla przyszłego leczenia raka
Mówiąc prosto, badanie pokazuje, że powszechny tłuszcz pokarmowy, kwas palmitynowy, może zostać wykorzystany przez guzy jelita do chemicznego opancerzenia białka blokującego odporność (B7H3) i ułatwienia ukrywaniu się nowotworu. Blokując to pojedyncze chemiczne przyłączenie, autorzy byli w stanie zdjąć pancerz, pozwolić wewnętrznym systemom komórkowym usunąć B7H3 i ponownie udostępnić drogę dla limfocytów CD8+ do ataku. Choć sam peptyd E jest narzędziem eksperymentalnym we wczesnym stadium, praca wskazuje palmitoilację B7H3 — i jej enzym ZDHHC24 — jako obiecujące cele lekowe. Jeśli podobne środki okażą się bezpieczne i skuteczne u ludzi, mogłyby pewnego dnia przekształcić więcej raków jelita z „zimnych” guzów ignorujących immunoterapię w „gorące” guzy, które układ odpornościowy potrafi rozpoznać i zniszczyć.
Cytowanie: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Słowa kluczowe: immunoterapia raka jelita grubego, punkt kontrolny B7H3, metabolizm kwasu palmitynowego, palmitoilacja białek, odporność przeciwnowotworowa komórek CD8 T