Clear Sky Science · pl
Makrofagi pawia (zebrafish) przekształcają fizyczne sygnały rany w szybkie zwiększenie przepuszczalności naczyń
Jak maleńka ryba uczy nas o obrzęku rany
Kiedy zdrapiesz kolano, skóra wokół szybko staje się zaczerwieniona, spuchnięta i przecieka płynem. Ta błyskawiczna zmiana w pobliskich naczyniach krwionośnych jest kluczowa dla zwalczania infekcji i uruchomienia procesu naprawy, lecz to, jak organizm wyczuwa uszkodzenie i reaguje w ciągu sekund, było trudne do obserwacji na żywo. Dzięki przezroczystym larwom pawii i zaawansowanym metodom obrazowania na żywo, badanie to ujawnia, jak wyspecjalizowane komórki układu odpornościowego otaczające naczynia przekształcają fizyczny wstrząs rany w niemal natychmiastowe przeciekanie naczyń, dostarczając nowych informacji o zapaleniu, gojeniu, a nawet uszkodzeniach płuc u ludzi.
Obserwowanie, jak uraz rozprzestrzenia się w ciele
Naukowcy pracowali z młodymi pawimi, których przezroczyste ciała pozwalały śledzić pod mikroskopem działanie komórek i naczyń krwionośnych. Przetnęli koniuszek płetwy ogonowej i wypełnili krążenie świecącym barwnikiem, który pozostaje wewnątrz zdrowych naczyń. Gdy zranione ryby umieszczono ponownie w zwykłej wodzie słodkiej, nagły napływ wody do tkanek spowodował „szok osmotyczny” wokół rany. W ciągu minut pobliskie naczynia rozszerzyły się i zaczęły przeciekać fluorescencyjny barwnik do otaczających tkanek, naśladując obrzęk i sączenie, które występują przy ludzkich ranach. Przenosząc ryby między zwykłym a specjalnie zbilansowanymi roztworami soli lub cukru, zespół wykazał, że to szybkie zwiększenie przepuszczalności naczyń zależy w dużej mierze od zmian osmolarności, a nie tylko od mechanicznego rozerwania tkanek.
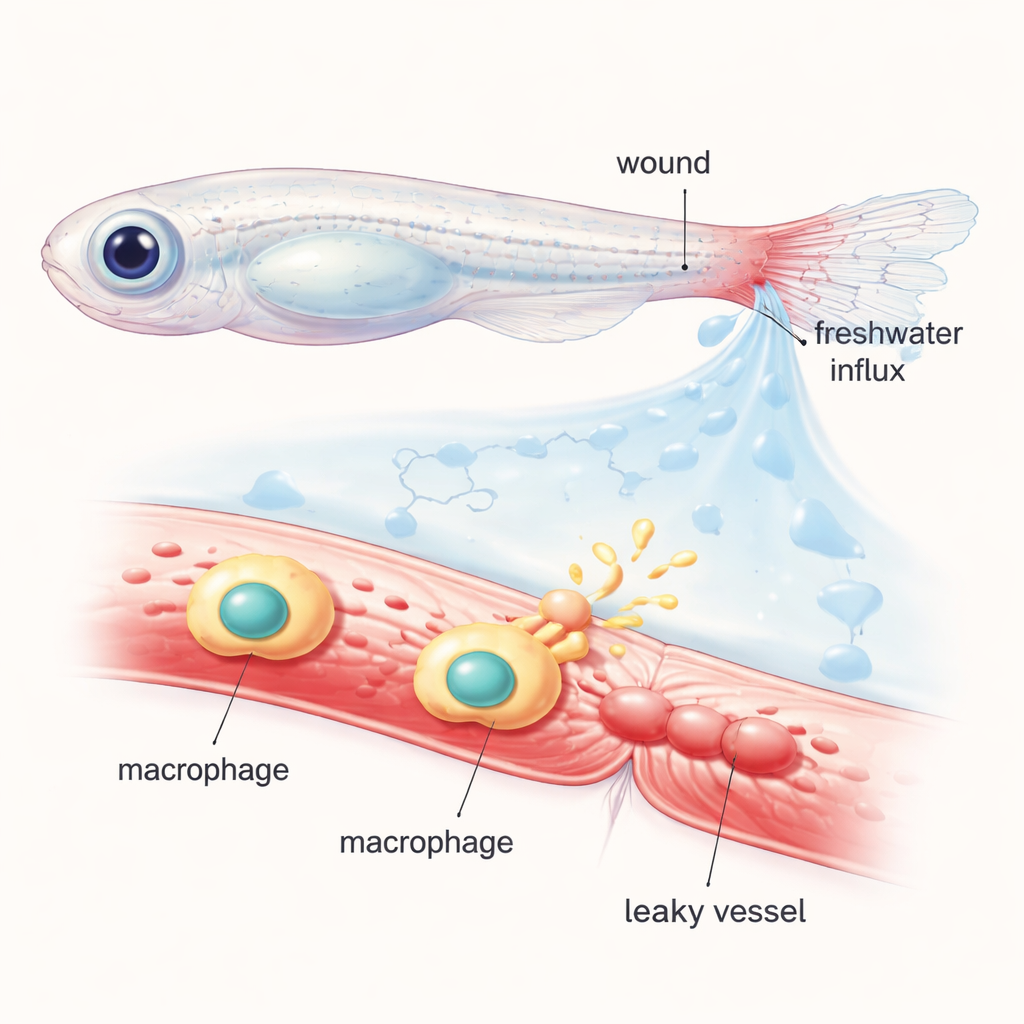
Śledzenie chemicznych przekaźników odpowiedzialnych za przeciek
Aby ustalić, które cząsteczki zamieniają fizyczny wstrząs w sygnał przecieku, naukowcy zbadali rodzinę tłuszczowych związków zwanych eikozanoidami, powstających z kwasu arachidonowego. Lipidy te są dobrze znane z ról w zapaleniu i przepływie krwi. Korzystając z mutantów genetycznych i leków, selektywnie wyłączali poszczególne enzymy w ścieżce eikozanoidowej. Zablokowanie kluczowego enzymu Alox5a (5-lipoksygenazy) lub jego partnera Lta4h zdecydowanie zmniejszyło ilość barwnika uciekającego z naczyń po szoku osmotycznym, nie hamując jednak samego zamykania rany. Natomiast ingerencja w inne powiązane enzymy miała niewielki efekt. Wskazuje to na konkretną gałąź ścieżki lipidowej jako główny mechanizm szybkiej odpowiedzi przeciekowej — działający niemal jak chemiczny zawór, który można otwierać lub zamykać na żądanie.
Zaskakująca rola komórek odpornościowych przylegających do naczyń
Krew zawiera różne typy komórek odpornościowych; u larw pawich głównymi graczami są neutrofile i makrofagi. Zespół zastosował sprytny zabieg genetyczny, by selektywnie zniszczyć albo neutrofile, albo makrofagi przed zranieniem. Usunięcie neutrofili niewiele zmieniało przeciekanie naczyń. Jednak gdy makrofagi zostały wyeliminowane, odpowiedź przeciekowa spadła o około połowę, co odzwierciedlało efekt blokowania ścieżki lipidowej Alox5a–Lta4h. Co ważne, te manipulacje nie zatrzymały szybkiego zamykania rany, pokazując, że rekrutacja leukocytów i przeciek naczyń mogą być częściowo kontrolowane niezależnie. Odkrycie to uczyniło makrofagi przynaczyniowe — makrofagi leżące ciasno wzdłuż zewnętrznej strony naczyń — kluczowymi tłumaczami między uszkodzeniem fizycznym a zachowaniem naczyń.
Od rozciągnięcia jądra do sygnału chemicznego
Jak te makrofagi przynaczyniowe wykrywają ranę, która może być oddalona? Odpowiedź tkwi w tym, jak ich jądra reagują na naprężenia mechaniczne. Gdy szok osmotyczny z rany rozchodzi się po pobliskiej tkance, napływ wody powoduje subtelne pęcznienie komórek i deformację jąder. Badacze znakowali mechanoczuły enzym cPla2 markerem fluorescencyjnym i wyrażali go specyficznie w makrofagach. Po zranieniu w normalnej wodzie słodkiej cPla2 szybko przemieszczał się na wewnętrzną powierzchnię błony jądrowej w makrofagach falą, która przetaczała się przez tkankę z prędkością około 50 mikrometrów na sekundę, odpowiadając rozprzestrzenianiu się rozpuszczonych soli. Ta translokacja zależała od warunków hipotonicznych i była dużo słabsza w roztworach izotonicznych. Makrofagi blisko naczyń wykazywały szczególnie ostre, odwracalne pulsacje wiązania cPla2 z jądrem, co z kolei uwalnia kwas arachidonowy do przekształcenia w lipidy wywołujące przeciek.
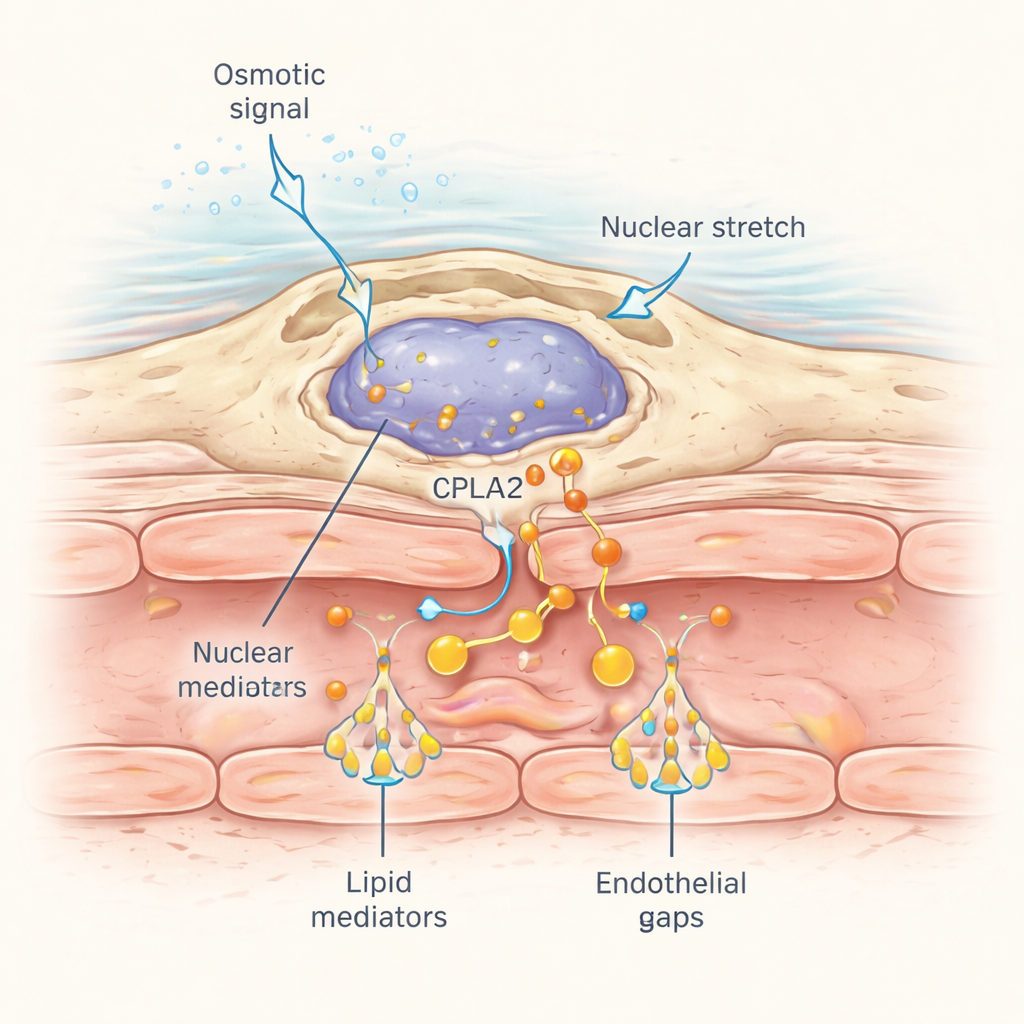
Dlaczego to ma znaczenie poza rybami
Mówiąc krótko, badanie pokazuje, że niektóre makrofagi działają jak fizyczni strażnicy: wyczuwają rozciągnięcie tkanek i błon jądrowych spowodowane zmianami osmotycznymi przy ranie, aktywują cPla2 na powierzchni jądra i szybko produkują lipidowe przekaźniki, które każą pobliskim naczyniom „otworzyć bramy”, pozwalając płynom i czynnikom odpornościowym napłynąć. Chociaż pawie żyją w słodkiej wodzie i napotykają unikalne wyzwania osmotyczne, podobne mechanoczułe ścieżki prawdopodobnie działają w ludzkich tkankach narażonych na zmiany ciśnień i przepływów, na przykład w płucach podczas wentylacji mechanicznej. Zrozumienie, jak rozciągnięcie jądra i sygnały lipidowe kontrolują przepuszczalność naczyń w czasie rzeczywistym, może ostatecznie pomóc w opracowaniu terapii precyzyjnie modulujących zapalenie — zarówno tłumiących szkodliwe przeciekanie w stanach takich jak ostre uszkodzenie płuc, jak i wzmacniających korzystne odpowiedzi przyspieszające naprawę tkanek.
Cytowanie: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Słowa kluczowe: gojenie ran, naczynia krwionośne, makrofagi, zapalenie, pawia (zebrafish)