Clear Sky Science · pl
Ultracienkie komórki ciekłe do czasowo-rozdzielczej kriomikroskopii elektronowej w skali mikrosekund
Obserwowanie białek w pracy w czasie rzeczywistym
Wiele maszyn utrzymujących komórki przy życiu zbudowanych jest z białek i często wiemy, jak wyglądają, gdy są „zamrożone” w jednym układzie. Jednak to, co naprawdę chcemy zobaczyć, to ich ruch podczas wykonywania funkcji. W tym badaniu przedstawiono nową metodę śledzenia tych ruchów na niezwykle krótkich skalach czasu — milionowych częściach sekundy — bez utraty wyjątkowo ostrej szczegółowości, jaką oferuje współczesna kriomikroskopia elektronowa (cryo‑EM).
Nowe okno na świat mikroskopijny
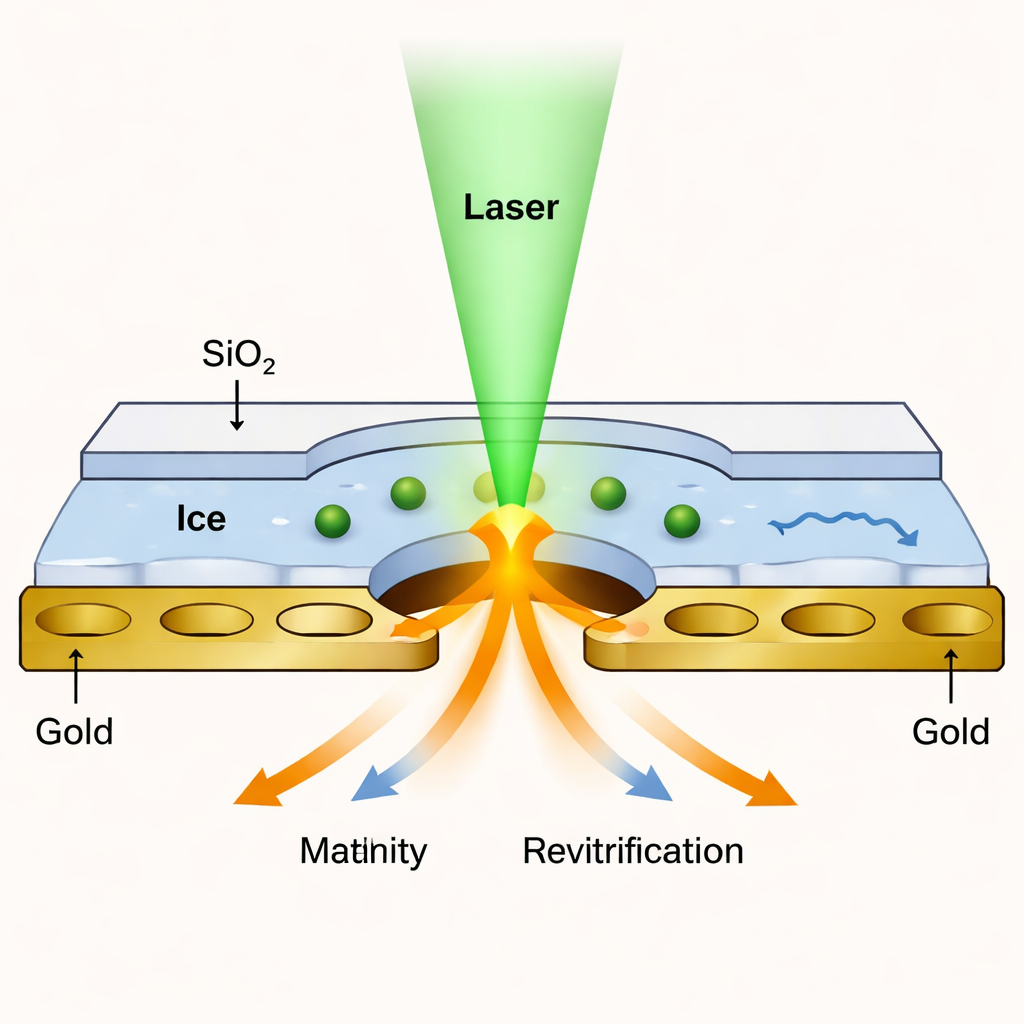
Cryo‑EM zrewolucjonizowała biologię strukturalną, obrazując błyskowo zamrożone białka z rozdzielczością niemal atomową. Tradycyjne metody jednak pokazują jedynie statyczne obrazy. Aby uchwycić ruch, badacze opracowali „czasowo-rozdzielczą cryo‑EM w skali mikrosekund”, w której laser krótko topi zamrożoną próbkę, pozwalając białkom się poruszyć, a następnie próbka jest szybko ponownie zamrażana, by je unieruchomić w nowych pozycjach. Problem polegał na tym, że maleńka cienka warstwa ciekła powstająca po roztopieniu lodu zwykle rozpada się po kilkudziesięciu mikrosekundach, co ogranicza czas obserwacji białek. Nowa praca rozwiązuje ten wąski gardełko przez zamknięcie próbki w ultracienkiej komórce ciekłej, utrzymując ją w stanie stabilnym wystarczająco długo, by obserwować wolniejsze, bardziej złożone ruchy.
Budowa ultracienkiej komórki ciekłej
Zespół stworzył coś w rodzaju nanoskładanki: roztwór białka jest zamrażany na standardowej perforowanej złotej siatce, po czym obie strony pokrywane są warstwami dwutlenku krzemu o grubości zaledwie około 1,4 nanometra — zaledwie kilka atomów. Te szklopodobne warstwy działają jak przezroczyste pokrywki, które zapobiegają odparowaniu cieczy, gdy laser topi lód. Krótkie impulsy laserowe ogrzewają zamkniętą próbkę do kontrolowanej temperatury, a następnie pozwalają jej ponownie zamarznąć w ciągu mikrosekund. Ponieważ membrany są tak cienkie, nadal przepuszczają wystarczająco elektronów, aby mikroskop mógł wytworzyć obrazy z niemal taką samą rozdzielczością jak w konwencjonalnej cryo‑EM — do około 1,7–1,8 angstroma dla testowego białka zwanego apoferrytyną.
Ostrzejsze widoki i bardziej wyrównane kąty
Ukrytym wyzwaniem w cryo‑EM jest to, że białka mają tendencję do przylegania do interfejsu powietrze–woda w cienkiej warstwie lodu, ustawiając się w podobnych orientacjach, co utrudnia rekonstrukcję pełnego widoku 3D. Powłoki z dwutlenku krzemu w tych komórkach ciekłych zmieniają powierzchnię z powietrze–woda na woda–ciało stałe i sprawiają, że jest ona bardziej przyjazna dla wody. W efekcie białka rzadziej przyczepiają się w jednej pozycji. Gdy autorzy testowali dużą maszynę komórkową, 50S podjednostkę rybosomu, stwierdzili, że rozkład kątowy cząstek stał się niemal idealnie równomierny, zasadniczo eliminując długo istniejący problem „preferowanej orientacji”, przy zachowaniu wysokiej rozdzielczości w końcowych rekonstrukcjach.
Strojenie czasu ruchu molekularnej dźwigni
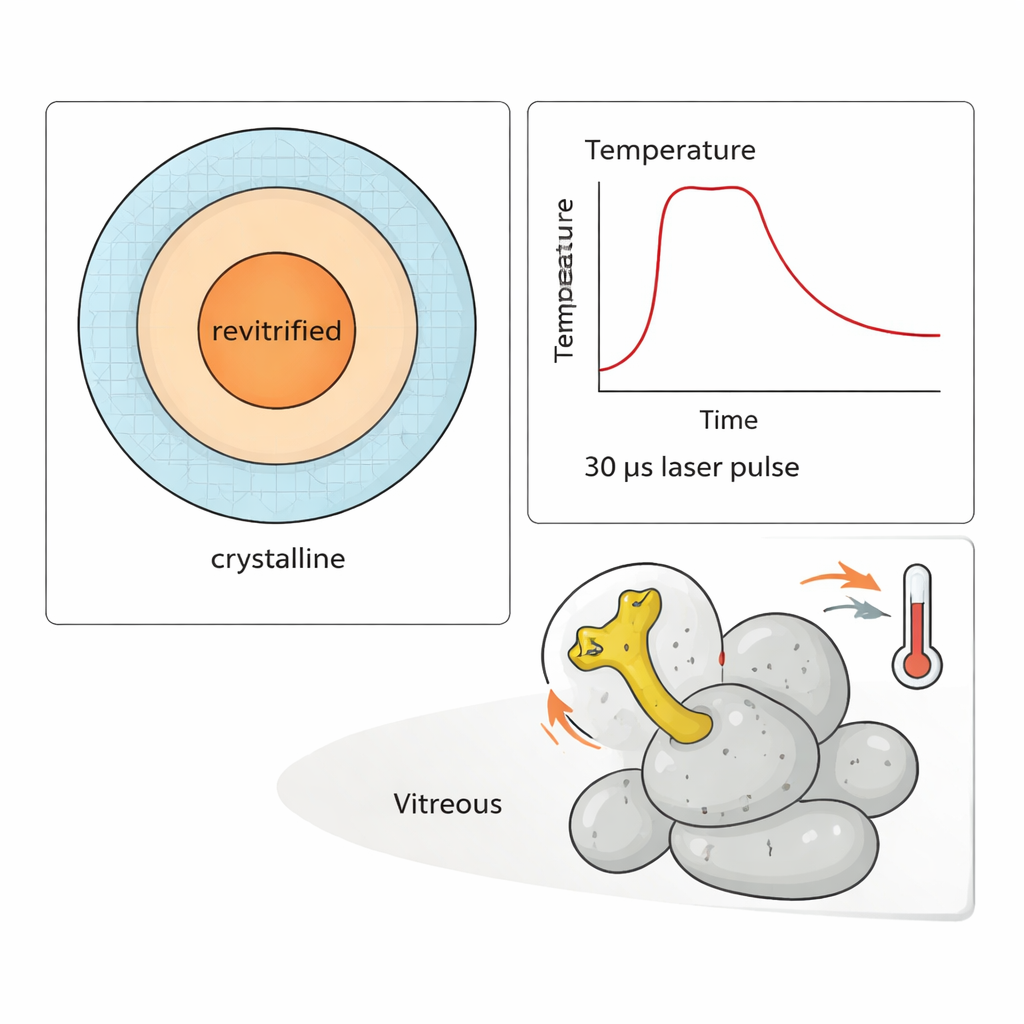
Aby zaprezentować możliwości metody, badacze przeprowadzili eksperyment „skoku temperaturowego” na podjednostce 50S. Elastyczne ramię tej cząstki, znane jako łodyga L1, kołysze się jak dźwignia podczas syntezy białka. Dostarczając serie impulsów laserowych trwających po 30 mikrosekund, mogli podgrzać próbkę do różnych temperatur przez okres do około 300 mikrosekund, a następnie ponownie ją zamrozić. Symulacje i pomiary, które regiony ponownie zestalają się jako szkło, pozwoliły oszacować temperaturę dla każdej obserwowanej cząstki. Analiza tysięcy obrazów wykazała, że amplituda ruchu łodygi L1 wyraźnie rośnie wraz z temperaturą — ale dopiero po upływie setek mikrosekund. We wczesnych chwilach rozkład konformacji nadal odzwierciedla stan wyjściowy w temperaturze pokojowej przed ponownym zamrożeniem.
Dlaczego ma to znaczenie dla przyszłej biologii
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że konstrukcja tej ultracienkiej komórki ciekłej znacząco wydłuża czas, przez jaki białka można obserwować w ruchu bez rozmycia detali strukturalnych. Przesuwa to czasowo-rozdzielczą cryo‑EM w skali mikrosekund z rejestrowania jedynie najszybszych zdarzeń ku badaniu wolniejszych, biologicznie istotnych przemieszczeń, takich jak opóźniona odpowiedź łodygi L1 na impuls cieplny. Przy dalszych udoskonaleniach podejście to może zbliżyć się do zakresu milisekund i dalej, a także oferuje nowe sposoby przygotowania próbek, zmniejszenia artefaktów obrazowania i wywoływania reakcji bezpośrednio na siatce. W praktyce oznacza to, że naukowcy robią coraz większe postępy w tworzeniu „molekularnych filmów”, które łączą kształty białek z ich rzeczywistymi funkcjami we wnętrzu żywych komórek.
Cytowanie: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Słowa kluczowe: czasowo-rozdzielcza kriomikroskopia elektronowa, dynamika białek, mikroskopia elektronowa komórek ciekłych, łodyga L1 rybosomu, ultracienkie membrany dwutlenku krzemu