Clear Sky Science · pl
Bioinspirowany hydrożel Janusa napędza regenerację zakażonego ścięgna Achillesa poprzez mechaniczno‑immunologiczne sterowanie czasowo‑przestrzenne
Dlaczego to ma znaczenie dla uszkodzonych ścięgien
Pęknięcia ścięgna Achillesa są powszechne zarówno u sportowców, jak i u osób starszych, a gdy rana zostaje zakażona przez bakterie, gojenie często przebiega źle: ścięgno może osłabnąć, zrastać się z tkankami otaczającymi albo nawet ponownie pęknąć. W tym badaniu przedstawiono nowy „inteligentny” opatrunek z hydrożelu, zainspirowany naturalną pochewką ścięgna, który można nałożyć na zakażone ścięgno podczas zabiegu. Ma on trzy zadania jednocześnie: mechanicznie chronić ścięgno, zabijać bakterie odporne na leki oraz łagodnie kierować odpowiedzią immunologiczną od szkodliwego zapalenia ku rzeczywistej regeneracji.
Dwustronny opatrunek inspirowany naturą
Zdrowe ścięgna leżą w śliskiej pochewce, która umożliwia im gładkie ślizganie się przy jednoczesnym mocnym umocowaniu. Chirurdzy mają trudność z odtworzeniem tego po zabiegu: materiały dobrze przyczepiające się do ścięgna często również przylegają do otaczających tkanek, powodując bolesne zrosty. Badacze skopiowali to naturalne połączenie „przyczepności i smarowania” za pomocą hydrożelu Janusa o nazwie HAPP@H-EXO. Jedna strona mocno chwyta powierzchnię ścięgna dzięki odwracalnym wiązaniom chemicznym i wiązaniom wodorowym, zapewniając solidne wsparcie mechaniczne. Przeciwległa strona została zaprojektowana, wykorzystując zabieg przypominający liść lotosu, tak aby była hydrofobowa i o niskim współczynniku tarcia, dzięki czemu pobliskie tkanki nie przylegają. Powstaje w ten sposób ochronna rękawica, która porusza się wraz ze ścięgnem, jednocześnie przeciwdziałając powstawaniu blizn z otoczeniem. 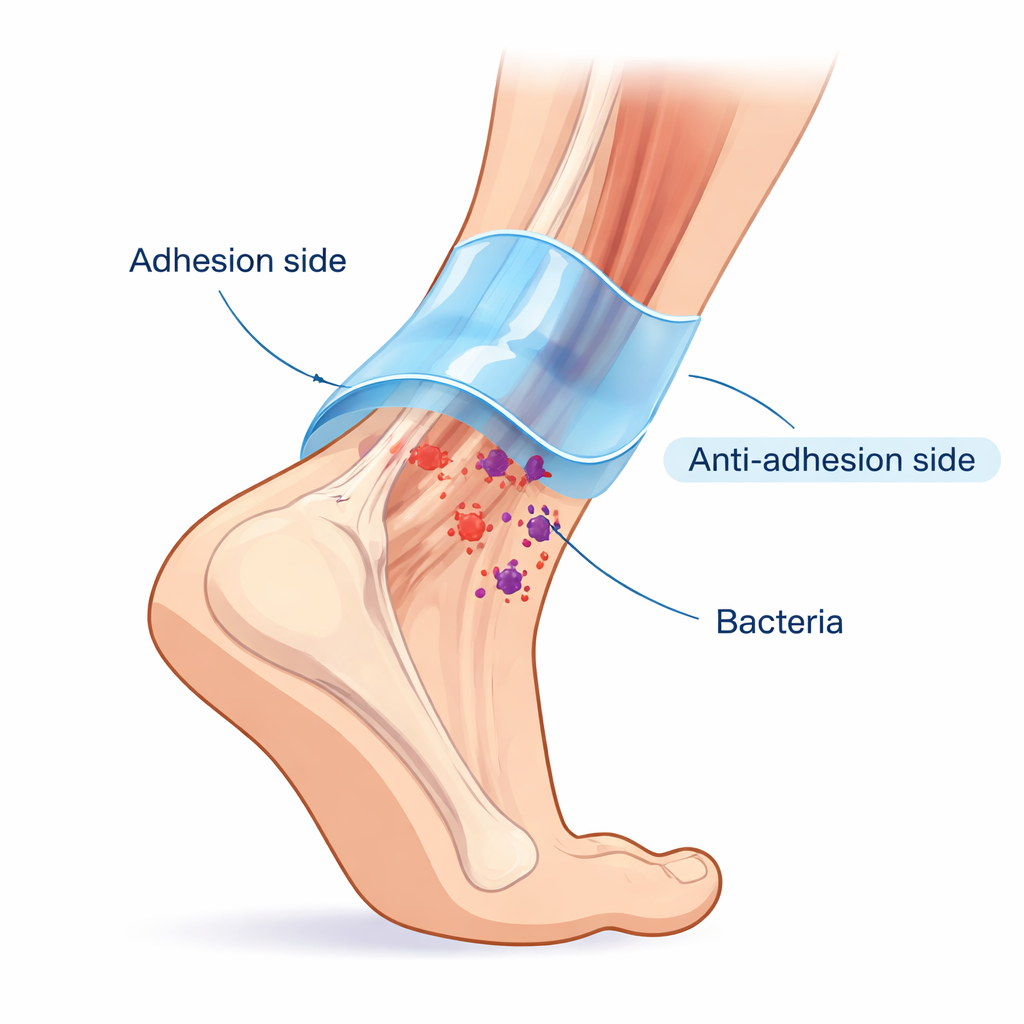
Zaprojektowany, by dzielić obciążenie i wytrzymać powtarzające się naprężenia
W przeciwieństwie do wielu miękkich żeli, ten materiał jest przeznaczony do pracy w surowym środowisku mechanicznym: każdy krok napina i rozluźnia ścięgno Achillesa. Zespół połączył sztywną, trwale usieciowaną sieć z drugą, dynamiczną siecią, która może się przeorganizowywać pod wpływem naprężeń. Testy wykazały, że hydrożel rozciąga się i ściska bez rozrywania, utrzymuje wytrzymałość przez co najmniej 100 cykli obciążenia i rozładowania oraz zużywa niewiele energii, co oznacza, że spręża się z powrotem zamiast ulegać trwałej deformacji. Symulacje komputerowe sugerowały, że owinięty wokół zaszytego ścięgna żel rozprowadza wysokie naprężenia z punktów szwu ku krawędziom ścięgna, zmniejszając ryzyko nowego pęknięcia w miejscu naprawy. U zwierząt przekładało się to na naprawione ścięgna, których wytrzymałość i sztywność zbliżały się do parametrów tkanki normalnej.
Chwytanie bakterii i przeciwdziałanie oporności
Zakażenie bakteryjne jest główną przyczyną niepowodzeń napraw ścięgien, szczególnie gdy wywołują je szczepy wielolekoodporne, takie jak MRSA. Zamiast polegać na tradycyjnych antybiotykach, hydrożel fizycznie wychwytuje i zabija bakterie. Jedna składowa, grupa fenyloboroksyowa, rozpoznaje bogate w cukry struktury na ścianach komórkowych bakterii i tworzy z nimi odwracalne wiązania, wyciągając bakterie z otaczającego płynu. Inny składnik, polimer o dodatnim ładunku, destabilizuje błony bakterii, powodując ich pękanie. W testach laboratoryjnych żel szybko zabijał MRSA, powszechne Staphylococcus i E. coli, rozkładał odporne biofilmy i utrzymywał działanie antybakteryjne przez dni i wiele cykli użycia, nie prowokując powstania oporności wobec mechanizmów wychwytywania ani zabijania. 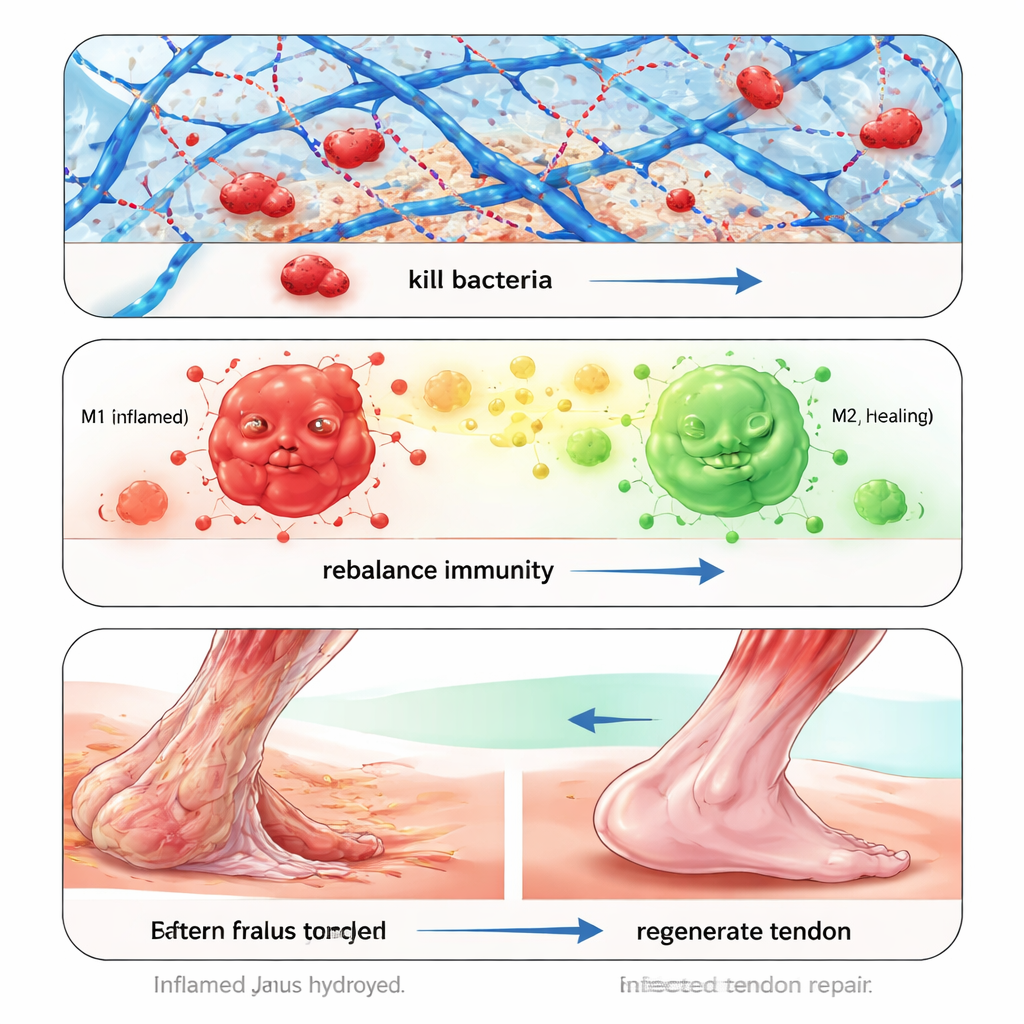
Kierowanie układem odpornościowym i odbudowa tkanki
Nawet po usunięciu bakterii zakażone ścięgna często pozostają w stanie stresu oksydacyjnego i przewlekłego zapalenia, co blokuje normalną naprawę. Aby temu zaradzić, badacze załadowali hydrożel maleńkimi pęcherzykami membranowymi — egzosomami — wydzielanymi przez komórki macierzyste ścięgna hodowane w warunkach niskiego stężenia tlenu. Te „hipoksyczne” egzosomy są bogate w sygnały przeciwzapalne i proregeneracyjne. Chemia żelu sprawia, że egzosomy uwalniają się szybciej w kwaśnej, zapalnej fazie wczesnej oraz wolniej, gdy warunki normalizują się. W eksperymentach komórkowych żele z egzosomami zmniejszały szkodliwe reaktywne formy tlenu, przywracały funkcję mitochondriów, wspierały tworzenie naczyń krwionośnych i przesuwały komórki odpornościowe z profilu zapalnego (M1) ku profilowi sprzyjającemu gojeniu (M2). Analizy genowe wskazywały na tłumienie szlaku NF-κB, centralnego regulatora zapalenia.
Od zakażonego pęknięcia do funkcjonalnego powrotu
W modelach szczurzych i króliczych pęknięć Achillesa celowo zakażonych MRSA, zastosowanie hydrożelu Janusa podczas zabiegu niemal wyeliminowało żywe bakterie w miejscu urazu w ciągu tygodnia. W kolejnych tygodniach leczone ścięgna wykazywały mniej uszkodzeń oksydacyjnych, niższe poziomy markerów zapalnych i więcej sygnałów pro‑gojenia niż nieleczone kontrole. Mikroskopia ujawniła lepiej ułożone, grubsze włókna kolagenowe, więcej naczyń krwionośnych oraz ekspresję kluczowych białek związanych ze dojrzałością ścięgna. Co istotne, zewnętrzna, nieprzywierająca strona żelu zapobiegała przyleganiu ścięgna do okolicznych tkanek, co potwierdziły badania obrazowe i oględziny makroskopowe. Zwierzęta leczone wersją z egzosomami odzyskiwały bardziej normalny chód i większą zdolność ścięgna do przenoszenia obciążeń, co wskazywało nie tylko na naprawę strukturalną, lecz także na przywrócenie funkcji.
Co to może znaczyć dla pacjentów
Praca pokazuje pojedynczy, biomimetyczny materiał, który zintegrowanie zajmuje się wsparciem mechanicznym, kontrolą zakażeń i równowagą immunologiczną. Łącząc dwustronny projekt fizyczny z chemią wychwytującą bakterie oraz kontrolowanym uwalnianiem egz0somów regeneracyjnych, hydrożel Janusa pomagał zakażonym ścięgnom Achillesa u zwierząt goić się mocniej, z mniejszą ilością blizn i lepszą mobilnością. Choć nadal potrzebne są badania kliniczne u ludzi, podejście to sugeruje przyszłość, w której złożone urazy tkanek miękkich, zwłaszcza skomplikowane przez infekcje oporne na leki, mogłyby być leczone „inteligentnymi” opatrunkami chirurgicznymi, aktywnie koordynującymi proces gojenia.
Cytowanie: Li, J., Wang, Z., Yang, W. et al. Bionic Janus hydrogel drives infected Achilles tendon regeneration via mechano-immune spatiotemporal steering. Nat Commun 17, 1805 (2026). https://doi.org/10.1038/s41467-026-68514-0
Słowa kluczowe: naprawa ścięgna Achillesa, opatrunek hydrożelowy, zakażenie oporne na leki, regeneracja tkanek, modulacja układu odpornościowego