Clear Sky Science · pl
Siły mechaniczne z międzykomórkowego samozszywania peptydów napędzają tworzenie sferoidów
Budowanie miniaturowych tkanek w laboratorium
Naukowcy ścigają się, by stworzyć miniaturowe wersje ludzkich tkanek, które zachowują się jak ich naturalne odpowiedniki. Te żywe modele pozwalają bezpieczniej testować leki przeciwnowotworowe i przybliżają nowe terapie dla cukrzycy i innych chorób. W badaniu przedstawiono sprytny sposób skłaniania komórek do formowania realistycznych trójwymiarowych skupisk, z własnymi prymitywnymi sieciami „przypominającymi naczynia krwionośne”, które poprawiają dostarczanie składników odżywczych i funkcję.
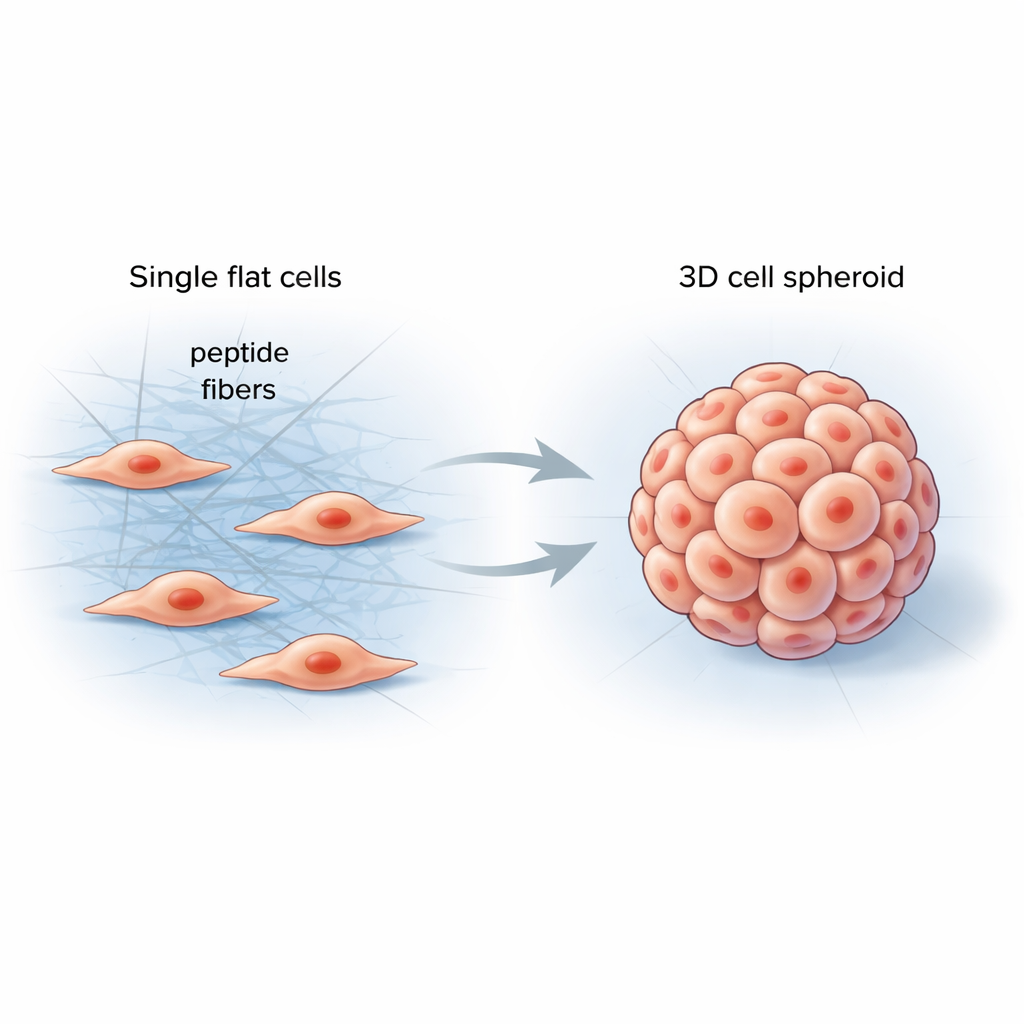
Pomaganie komórkom w odczuwaniu otoczenia
W naszym ciele komórki żyją w miękkim, a jednocześnie uporządkowanym środowisku zwanym macierzą zewnątrzkomórkową — sieci białek, która podtrzymuje tkanki i nieustannie przekazuje komórkom sygnały mechaniczne. Konwencjonalne materiały laboratoryjne mają trudności z naśladowaniem tej złożoności, często dając płaskie warstwy komórek, które zachowują się bardzo inaczej niż prawdziwe organy czy guzy. Badacze postawili sobie zadanie zaprojektowania prostego, programowalnego materiału, który tworzyłby się bezpośrednio między komórkami, usztywniał ich otoczenie w kontrolowany sposób i skłaniał je do bardziej naturalnych trójwymiarowych kształtów.
Inteligentne peptydy, które składają się między komórkami
Zespół stworzył krótkie fragmenty białek, zwane peptydami, które mogą łączyć się w długie, cienkie włókna po zetknięciu z określonymi enzymami na powierzchni komórek. Gdy peptydy dodano do komórek nowotworowych, początkowo pozostawały nieaktywne, niczym przejrzysty roztwór. Gdy enzymy komórek odcięły część cząsteczki, peptydy szybko samoorganizowały się w włóknistą sieć otaczającą i łączącą sąsiednie komórki. Ta nowa sieć włókien zmieniła lokalne siły mechaniczne, zachęcając komórki do wzajemnego przyciągania się, przebudowy wewnętrznego rusztowania i gromadzenia się w kuliste sferoidy 3D zamiast rozprzestrzeniania się w warstwie.
Z klastrów komórkowych do sieci przypominających naczynia
Aby przybliżyć model do prawdziwej tkanki, naukowcy wprowadzili następnie ludzkie komórki śródbłonka — te, które normalnie wyścielają naczynia krwionośne — wraz z drugim peptydem niosącym mały „znacznik adresowy” przyciągający te komórki. Razem oryginalne i zmodyfikowane peptydy utworzyły wspólne nanowłókniste rusztowanie. Komórki śródbłonka wykorzystały to rusztowanie do wyrastania w rurkowate wypustki, które oplatały i penetrowały sferoidy, tworząc struktury przypominające kapilary. Gdy badacze przepuszczali fluorescencyjne cząsteczki podobne do cukrów wokół tych struktur, zaobserwowali znacznie głębsze przenikanie do jądra sferoidu w porównaniu z sferoidami pozbawionymi wewnętrznych rur, co pokazało wyraźną poprawę transportu składników odżywczych i sygnałów.
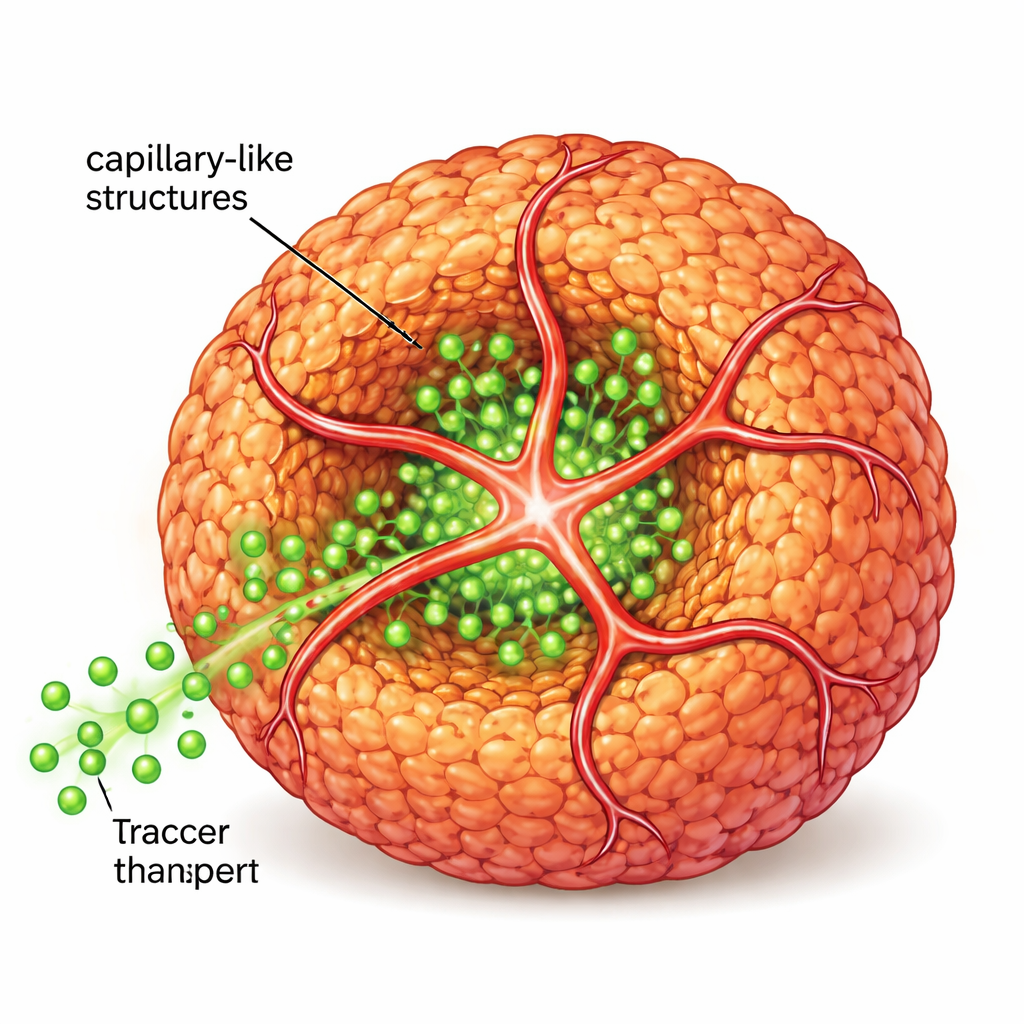
Bliżej prawdziwych guzów i funkcjonujących wysp trzustkowych
Profilowanie aktywności genów ujawniło, że sferoidy nowotworowe zawierające struktury przypominające kapilary bardziej przypominały próbki guzów pacjentów z glejakiem niż tradycyjne płaskie hodowle czy sferoidy bez unaczynienia. U myszy sferoidy z tymi prymitywnymi sieciami naczyniowymi rozwijały się w większe, bardziej unaczynione guzy, co wskazuje, że model in vitro odzwierciedla kluczowe cechy zachowania nowotworu. Tę samą strategię zastosowano do komórek beta trzustki, które normalnie żyją w silnie unaczynionych wyspach i wydzielają insulinę w odpowiedzi na glukozę. Gdy sferoidy komórek beta wyposażono w struktury przypominające kapilary za pomocą systemu peptydowego i komórek śródbłonka, wykazywały one znacznie silniejsze, lepiej wyregulowane uwalnianie insuliny, co sugeruje potężne narzędzie dla badań nad cukrzycą i medycyną regeneracyjną.
Dlaczego to ma znaczenie dla przyszłych terapii
Pozwalając prostym peptydom samoorganizować się między żywymi komórkami, praca ta oferuje ogólny przepis na budowanie miniaturowych, unaczynionych tkanek, które czują się i funkcjonują bardziej jak te w organizmie. Powstałe sferoidy lepiej odzwierciedlają guzy pacjentów i funkcjonujące wyspy, co czyni je cennymi do testowania leków, badania mechanizmów chorób i projektowania nowych terapii opartych na komórkach. Dla osób niezajmujących się specjalistycznie kluczowy wniosek jest taki, że nadanie hodowanym w laboratorium komórkom „odpowiedniego odczucia” i drobnych sieci przypominających naczynia może dramatycznie poprawić ich wierność wobec tkanek ludzkich, potencjalnie przyspieszając drogę od badań podstawowych do skutecznych terapii.
Cytowanie: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Słowa kluczowe: inżynieria tkankowa, modele nowotworowe, angiogeneza, organoidy, samozszywanie peptydów