Clear Sky Science · pl
Przerywany post hamuje guzy napędzane przez Tp53 poprzez regulację metioniny i m6A zależną od mikrobioty jelitowej
Dlaczego danie odpoczynku jelitom może spowolnić śmiertelne guzy mózgu
Glejak wielopostaciowy to jeden z najbardziej agresywnych nowotworów mózgu, a obecne terapie — operacja, radioterapia i chemioterapia — często jedynie nieznacznie wydłużają życie pacjentów. To badanie stawia proste, lecz istotne pytanie o dalekosiężnych konsekwencjach dla codziennego życia: czy sposób odżywiania się, a konkretnie przerywany post, może zmienić bakterie jelitowe i chemię krwi na tyle, by w istotny sposób spowolnić rozwój wybranych nowotworów mózgu?
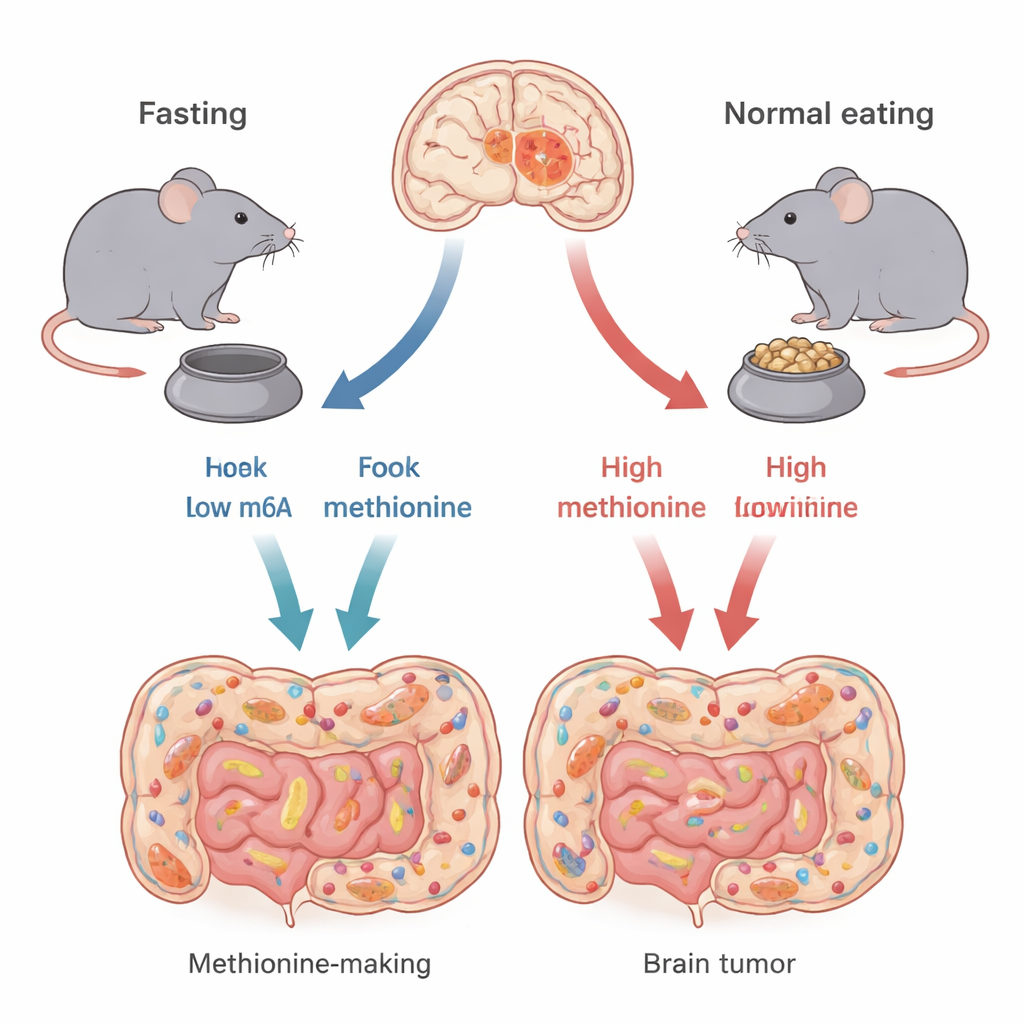
Różne odmiany „tego samego” raka mózgu
Glejaki nie są identyczne. Autorzy skupiają się na dwóch głównych typach genetycznych, zdefiniowanych przez zmiany w genach TP53 i CDKN2A. Te geny kontrolują wzrost i śmierć komórek. Na modelach mysich wiernie odzwierciedlających każdy podtyp ludzki, badacze pokazują, że przerywany post — 24 godziny bez jedzenia, a potem 24 godziny z jedzeniem — nie działa jednakowo na wszystkie guzy. Myszy z guzami typu TP53 żyły dłużej i miały mniejsze guzy podczas postu, natomiast u myszy z guzami typu CDKN2A korzyści były niewielkie. To sugeruje, że skuteczność postu może w dużym stopniu zależeć od genetycznego „okablowania” guza.
Od wzorca jedzenia, przez bakterie, po chemię mózgu
Zespół badał dalej, jak post wywołuje ten selektywny efekt. Ponieważ całkowita ilość jedzenia była taka sama między grupami, kluczową różnicą był czas jedzenia. Ten czynnik silnie przekształcił mikrobiotę jelitową — rozległe społeczności bakterii w jelicie. U myszy z typem TP53 poddanych postowi obniżyła się obfitość określonych grup bakterii efektywnie wytwarzających aminokwas metioninę, takich jak niektóre szczepy Alistipes i Prevotella. Ponieważ metionina jest niezbędnym budulcem, którego zwierzęta muszą pozyskiwać z diety lub od mikrobioty, ta mikrobowa zmiana oznaczała mniejszy przepływ metioniny z jelita do krwi, a ostatecznie do mózgu.
Jak jeden składnik odżywczy reguluje sygnały napędzające raka
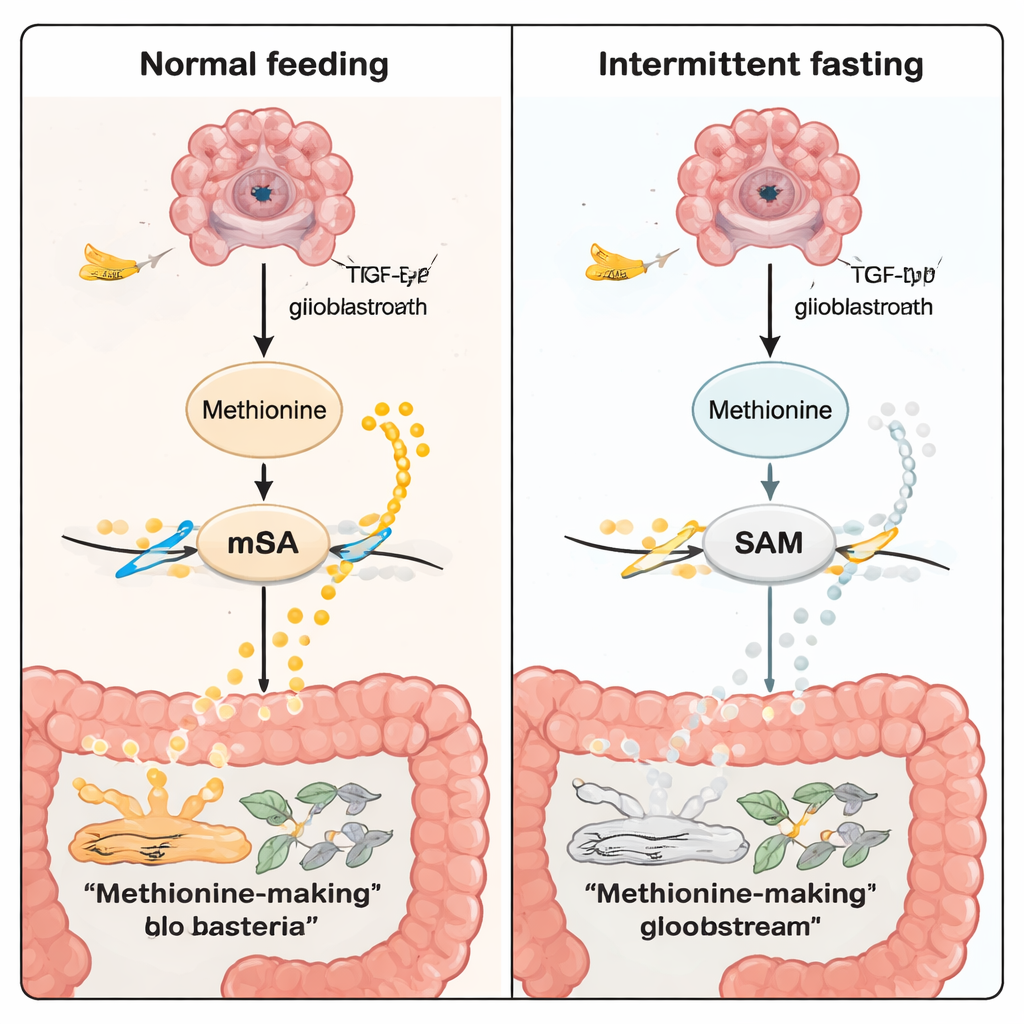
Metionina to nie tylko składnik odżywczy; jest również surowcem do syntezy S-adenozylometioniny (SAM), uniwersalnego „donora” grup metylowych w komórce. SAM zasila chemiczne znakowanie RNA zwane m6A. Te znaczniki pomagają kontrolować poziom ekspresji niektórych genów. W modelu guza TP53 post obniżył poziomy metioniny i SAM we krwi oraz w obszarach nowotworowych mózgu. Stosując wielowarstwowe analizy omiksowe — standardowe sekwencjonowanie RNA, profilowanie RNA na poziomie pojedynczych komórek oraz przestrzenne mapy aktywności genów i metabolitów — badacze odkryli mniej znaków m6A na kluczowych RNA związanych z rakiem podczas postu. Jednym z ważnych celów był TGFB2, gen w ścieżce sygnalnej TGF-β, znanej z napędzania wzrostu i inwazji guza. Przy poście enzym METTL3 (który zapisuje znaczniki m6A) i TGFB2 były obniżone, a sygnalizacja TGF-β osłabła.
Dowodzenie przyczynowości za pomocą ukierunkowanych interwencji
Aby wyjść poza korelacje, naukowcy przeprowadzili eksperymenty „ratunkowe”. Zablokowali METTL3 lekiem albo przenieśli mikrobiotę z myszy na poście do myszy karmionych normalnie i zaobserwowali spowolnienie wzrostu guza nawet bez postu — co wspiera tezę, że zarówno mikrobiota, jak i mechanizmy m6A są kluczowymi elementami. Odwrotnie, gdy myszy na poście otrzymały dodatkową metioninę lub lek zwiększający oznakowanie m6A, ich guzy rosły podobnie jak u myszy karmionych normalnie, a korzyść w przeżyciu zniknęła. Co ważne, zakłócenie mikrobioty szerokospektralnymi antybiotykami zniwelowało wiele zmian związanych z postem, podkreślając, że społeczność jelitowa jest centralnym węzłem w tym łańcuchu zdarzeń.
Co to znaczy dla ludzi i przyszłych terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że nie wszystkie nowotwory, a nawet wszystkie glejaki, zareagują jednakowo na strategię żywieniową jak przerywany post. W glejakach typu TP53 post zdaje się „komunikować” z mózgiem przez jelita: przekształca mikrobiotę, co z kolei obniża produkcję metioniny, redukuje chemiczne znakowanie RNA i wycisza silne sygnały wzrostu w komórkach nowotworowych. Chociaż prace te prowadzone są na myszach i wymagają ostrożnego przełożenia na praktykę kliniczną, wskazują na przyszłość, w której proste wzorce stylu życia, terapie oparte na mikrobiocie jelitowej i leki celujące w ścieżki metioniny lub m6A mogłyby być dostosowane do genetycznego podtypu guza danego pacjenta.
Cytowanie: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Słowa kluczowe: przerywany post, glejak, mikrobiom jelitowy, metabolizm metioniny, modyfikacja RNA m6A