Clear Sky Science · pl
Jednoczesna oksydacja siarczków i redukcja siarczanów dla wewnątrzkomórkowej homeostazy redoks w warunkach silnej kwasowości
Dlaczego oczyszczanie toksycznych gazów wymaga sprytnych mikroorganizmów
Wiele gałęzi przemysłu emituje siarkowodór — trujący gaz o zapachu zgniłych jaj, który może korodować urządzenia, zanieczyszczać powietrze i zagrażać pracownikom. Do jego oczyszczania inżynierowie coraz częściej wykorzystują mikroby przekształcające siarczki w bezpieczniejsze formy siarki. Artykuł ujawnia nieoczekiwaną strategię mikrobiologiczną: nowo rozpoznany gatunek Mycobacterium, który jednocześnie prowadzi dwa zwykle sprzeczne szlaki chemiczne, aby szybko odtruwać siarkowodór i jednocześnie chronić się przed uszkodzeniami wewnątrzkomórkowymi, nawet w warunkach skrajnej kwasowości.
Pojedynek w cyklu siarki
W przyrodzie cykl siarki napędzają dwa przeciwne procesy. Niektóre mikroby utleniają siarczki (najbardziej zredukowaną, toksyczną postać) do mniej szkodliwych produktów, takich jak siarka elementarna czy siarczany, zyskując przy tym energię. Inne idą w przeciwnym kierunku, redukując siarczany z powrotem do siarczków, by móc budować niezbędne składniki komórkowe, takie jak aminokwasy zawierające siarkę. Ponieważ te reakcje się znoszą, biologowie przypuszczali, że pojedyncza komórka unika jednoczesnego prowadzenia obu — wydawałoby się to marnotrawne, niczym jednoczesne ogrzewanie i chłodzenie domu przy otwartych oknach. 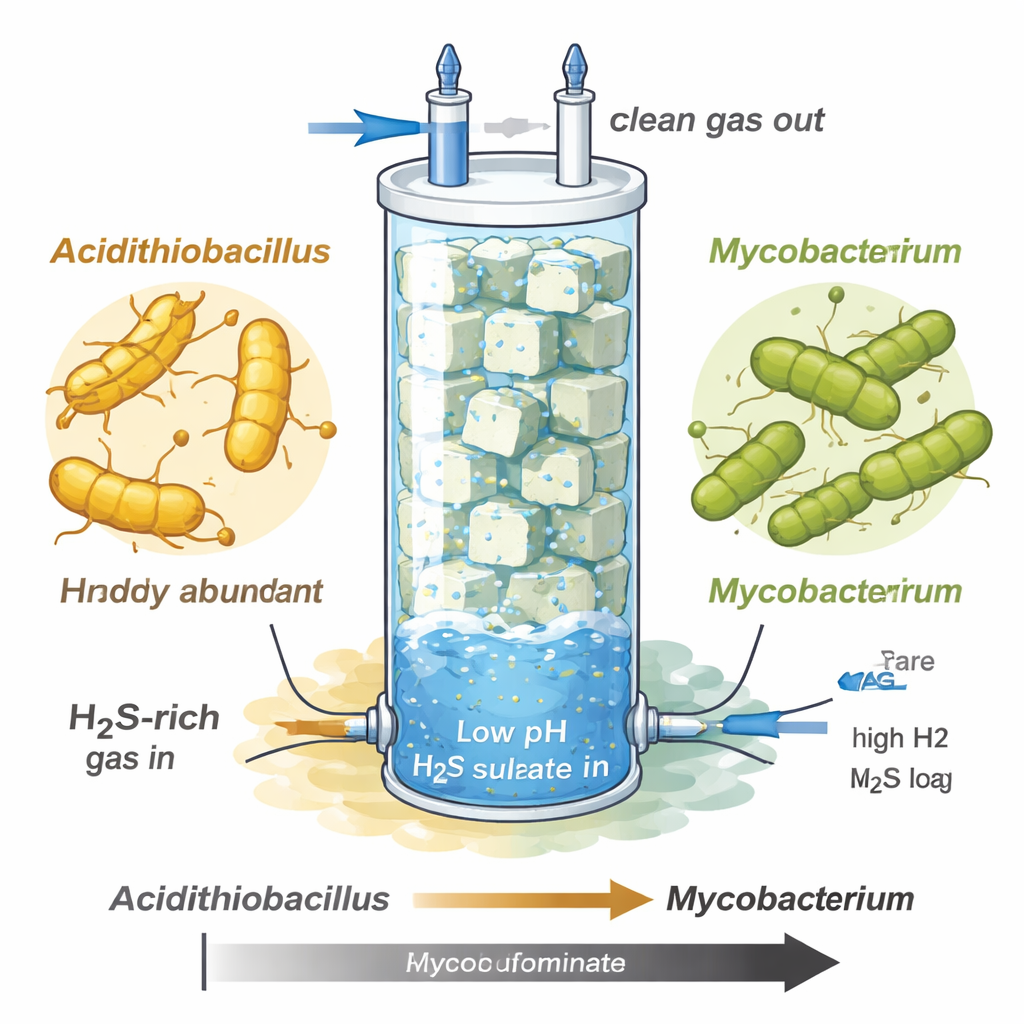
Odnaleźć przetrwańca w ekstremalnym reaktorze
Badacze analizowali filtr biopłuczkowy — wysoki szklany słup wypełniony kostkami pianki — zaprojektowany do usuwania siarkowodoru ze strumieni gazów podobnych do surowego biogazu czy gazu ziemnego. Zwiększając obciążenie siarkowodorem i utrzymując układ w bardzo kwaśnym środowisku (pH około 1–1,5), zaobserwowali dramatyczne zmiany w społeczności mikroorganizmów. Początkowo dominował znany utleniacz siarczków, Acidithiobacillus, który przemieniał dużą część siarkowodoru w siarczany, lecz później załamał się pod ekstremalnym stresem siarkowodorowym. Na jego miejsce wkroczył uprzednio nieopisany gatunek Mycobacterium, oznaczony jako MAG-M116, który przejął niemal całą społeczność, mimo że we wczesnej, łagodniejszej fazie rósł wolniej.
Mikrob łamiący zwykłe zasady
Analizy genetyczne i białkowe wykazały, że MAG-M116 ma nietypowy układ metaboliczny. Posiada kluczowy enzym, sulfide:quinone oxidoreductase, który utlenia siarczek jedynie do postaci stałej — siarki elementarnej — gromadzącej się jako drobne cząstki. Równocześnie mikroorganizm dysponuje pełnym zestawem genów do asymilacyjnej redukcji siarczanów, szlaku pobierającego siarczany do wnętrza komórki i redukującego je w celu syntezy aminokwasów, takich jak cysteina i metionina. Przy wysokim stężeniu siarkowodoru oba szlaki były aktywne jednocześnie. Utlenianie siarczku napędzało dopływ elektronów do maszynerii energetycznej komórki, podczas gdy redukcja siarczanów pochłaniała część tego przepływu elektronów, łącząc obie „strony” cyklu siarki w jednej komórce.
Przekształcenie „marnotrawnego” cyklu w zawór bezpieczeństwa
Prowadzenie obu szlaków jednocześnie teoretycznie mogłoby wydawać się bezcelowe — palenie energii bez zysku. Zespół pokazuje jednak, że dla MAG-M116 działa to jako zawór bezpieczeństwa na nadmiar elektronów. Utlenianie dużych ilości siarczku uwalnia falę elektronów do łańcucha oddechowego komórki, co może prowadzić do wycieku i powstawania reaktywnych form tlenu (ROS) — szkodliwych cząsteczek atakujących DNA, białka i błony. Aktywna redukcja siarczanów do aminokwasów przekierowuje 10–14% tych elektronów do pracy konstrukcyjnej, ograniczając narastanie nadmiernie zredukowanego, skłonnego do przeciekania stanu. Eksperymenty porównujące warunki z obecnością i bez siarczanów wykazały, że aktywna redukcja siarczanów zmniejszała produkcję ROS nawet o około 60% i zapobiegała kumulacji zredukowanych kofaktorów, które w przeciwnym razie napędzałyby uszkodzenia oksydacyjne. 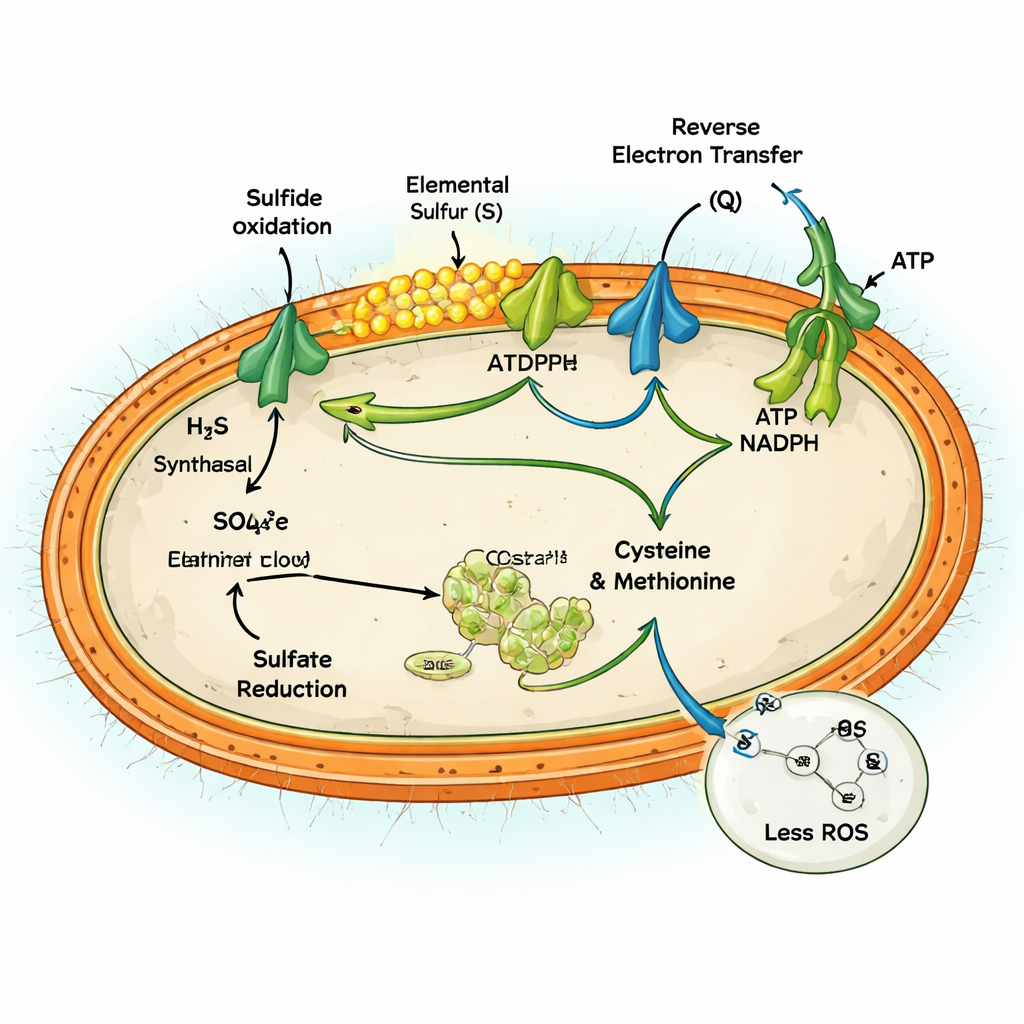
Od toksycznego gazu do użytecznych produktów
W późniejszych etapach pracy reaktora, gdy MAG-M116 stał się dominujący, niemal cały dopływający siarkowodór był przekształcany w stałą siarkę elementarną, zamiast w siarczany. Równocześnie badacze wykryli rosnące stężenia cysteiny i metioniny w fazie ciekłej, co sugeruje, że mikroorganizm uwalniał nadmiar siarko‑bogatych aminokwasów do otoczenia. To połączenie — stabilna siarka elementarna i wartościowe organiczne związki siarki — przekształca niegdyś niebezpieczne zanieczyszczenie w mieszankę odzyskiwalnych produktów przydatnych w rolnictwie, materiałach i systemach energetycznych.
Co to znaczy dla zdrowia i technologii
Dla odbiorcy niebędącego specjalistą kluczowy wniosek jest taki, że to Mycobacterium rozwiązało podwójny problem: potrafi oczyścić duże ilości toksycznego gazu, jednocześnie utrzymując wewnętrzną chemię w równowadze. Robi to, prowadząc reakcji siarkowe typu „push–pull”, które zwykle są rozdzielane, używając pozornie marnotrawnego cyklu jako wbudowanej amortyzacji nadmiaru elektronów i szkodliwych rodników tlenowych. Odkrycie to nie tylko sugeruje nowe podejścia do projektowania odpornych bioreaktorów niskopH do usuwania siarkowodoru i siarczanów, lecz także wskazuje, że pokrewne mikroby, w tym chorobotwórcze gatunki Mycobacterium, mogą stosować podobne triki, by przetrwać ataki oksydacyjne w organizmie człowieka.
Cytowanie: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Słowa kluczowe: cykl siarki, siarkowodór, Mycobacterium, homeostaza redoks, biodesiarkowanie