Clear Sky Science · pl
Identyfikacja peptydów przeciwdrobnoustrojowych z pradawnych mikrobiomów jelitowych
Wykopując pradawne wskazówki, by zwalczać współczesne zarazki
Wraz ze wzrostem oporności na antybiotyki na całym świecie lekarze coraz częściej nie mają jak leczyć groźnych zakażeń. To badanie przyjmuje nietypowe podejście do problemu: nie szuka odpowiedzi w zaawansowanych laboratoriach chemicznych, lecz w skamieniałych szczątkach ludzkich odchodów — pradawnych „kapsułach czasu” jelit — aby odkryć naturalne molekuły zwalczające zarazki, które mogą być skuteczne także wobec współczesnych bakterii.
Pradawne mikroby jako ukryte apteczki
Długo przed pojawieniem się nowoczesnej medycyny jelito człowieka było już polem bitwy, gdzie pożyteczne mikroby i najeźdźcze zarazki rywalizowały o przestrzeń i pokarm. Wiele przyjaznych bakterii jelitowych wytwarza peptydy przeciwdrobnoustrojowe — krótkie fragmenty białek, które tworzą dziury w komórkach bakterii lub w inny sposób je unieszkodliwiają. Współczesne badania skupiały się głównie na dzisiejszych mikrobiomach w poszukiwaniu tych zabójców zarazków. Jednak nasze obecne społeczności jelitowe ewoluowały w towarzystwie stosowania antybiotyków i nowoczesnego stylu życia, co dało patogenom wiele okazji do rozwinięcia oporności. Natomiast pradawne społeczności jelitowe, zachowane w wysuszonych odchodach zwanych koprolitami, powstały w świecie bez lekarsko przepisywanych antybiotyków. To czyni je obiecującym źródłem „zapomnianych” mechanizmów obronnych, których współczesne patogeny mogły jeszcze nie opanować.
Lekki narzędzie AI do odczytywania skamieniałego DNA
Aby zbadać tę pradawną aptekę, badacze stworzyli nowe narzędzie komputerowe o nazwie AMPLiT (AMP Lightweight Identification Tool). Zamiast wymagać potężnych superkomputerów, AMPLiT działa wydajnie na zwykłym laptopie, zachowując jednocześnie wysoką dokładność. Przeszukuje ogromne zbiory danych DNA z próbek mikrobiomu i wskazuje krótkie sekwencje, które prawdopodobnie kodują peptydy przeciwdrobnoustrojowe. Zespół dopracował konstrukcję AMPLiT tak, aby mogła przetwarzać miliony fragmentów uszkodzonego, wiekowego DNA w ciągu kilku godzin, skracając czas trenowania o około 80% w porównaniu z wcześniejszymi metodami, a jednocześnie utrzymując niemal najlepszą w klasie skuteczność w wykrywaniu obiecujących kandydatów.
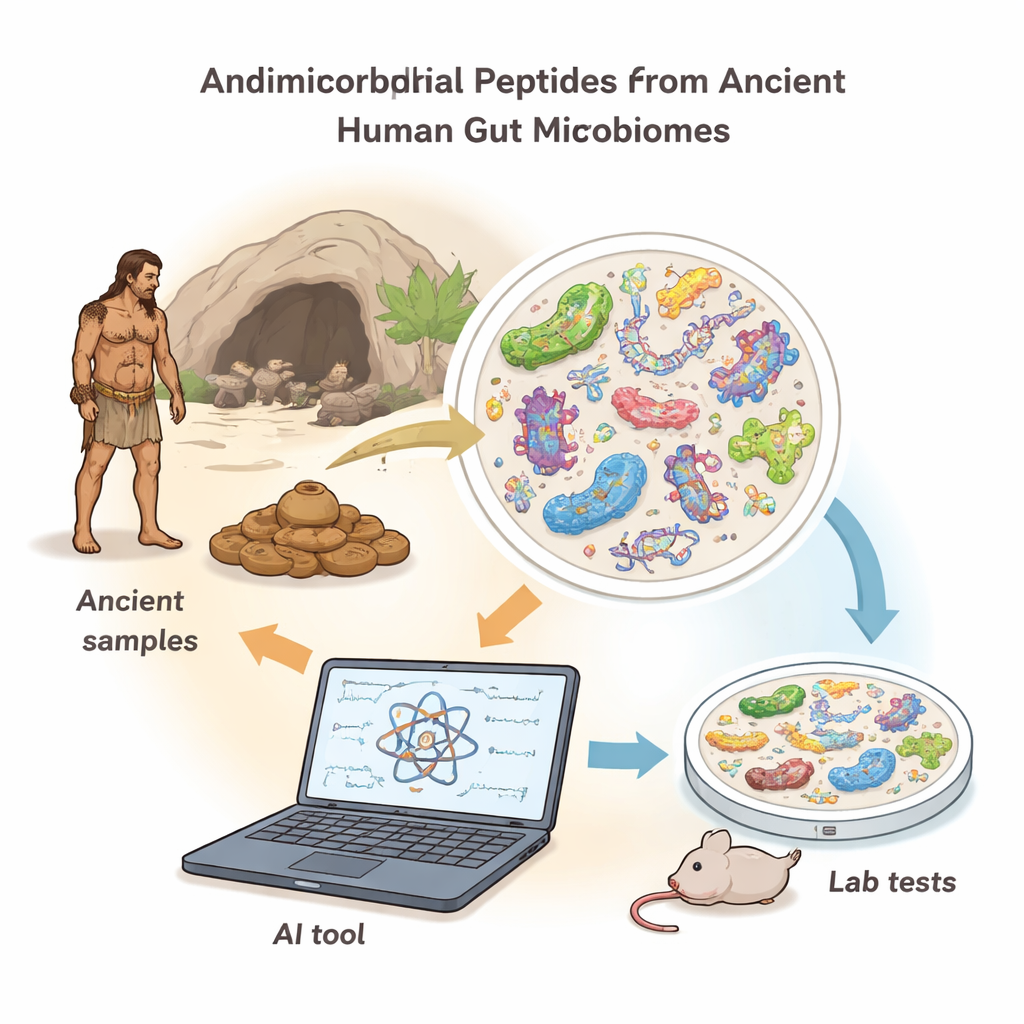
Wskrzeszanie zabójców zarazków od pradawnego mieszkańca jelit
Przy użyciu AMPLiT naukowcy przeanalizowali DNA jelitowe siedmiu starożytnych ludzi, którzy żyli 1 000–2 000 lat temu w Ameryce Północnej. Po usunięciu zanieczyszczeń środowiskowych i skupieniu się na krótkich, praktycznych długościach peptydów, narzędzie przewidziało setki tysięcy potencjalnych sekwencji przeciwdrobnoustrojowych. Surowszy zestaw filtrów — obecność w wielu osobnikach, właściwości chemiczne i niskie przewidywane toksyczne działanie — zawęził to do 41 kandydatów o wysokim zaufaniu, z których 40 dało się zsyntetyzować w laboratorium. Testy przeciwko bakteriom Gram-dodatnim i Gram-ujemnym (dwóm głównym grupom obejmującym wiele powszechnych patogenów) wykazały, że 36 z 40 peptydów spowolniło lub zatrzymało wzrost bakterii przy stosunkowo niskich dawkach — niezwykle wysoki odsetek sukcesu dla tego typu odkryć.
Zaskakująca gwiazda: zanikający sprzymierzeniec jelit
Około dwie trzecie najbardziej aktywnych peptydów pochodziło od jednej bakterii jelitowej: Segatella copri, bliskiego krewnego mikroba wcześniej klasyfikowanego jako Prevotella copri. Ten gatunek był liczny w pradawnych jelitach i nadal występuje u osób o bardziej tradycyjnej, mniej uprzemysłowionej diecie, lecz jest obecnie rzadki w wielu populacjach miejskich i zachodniego typu. Śledząc położenie genów kodujących peptydy w genomie Segatella, zespół odkrył, że większość z nich to w rzeczywistości fragmenty większych, codziennych genów „porządkowych”, które mikroorganizm najwyraźniej zaadaptował na broń — efektywny ewolucyjny trik. Wiele z tych pradawnych peptydów wygląda znacząco inaczej niż te w nowoczesnych bazach danych, co sugeruje, że reprezentują one naprawdę nowe projekty chemiczne, a nie tylko drobne wariacje znanych antybiotyków.
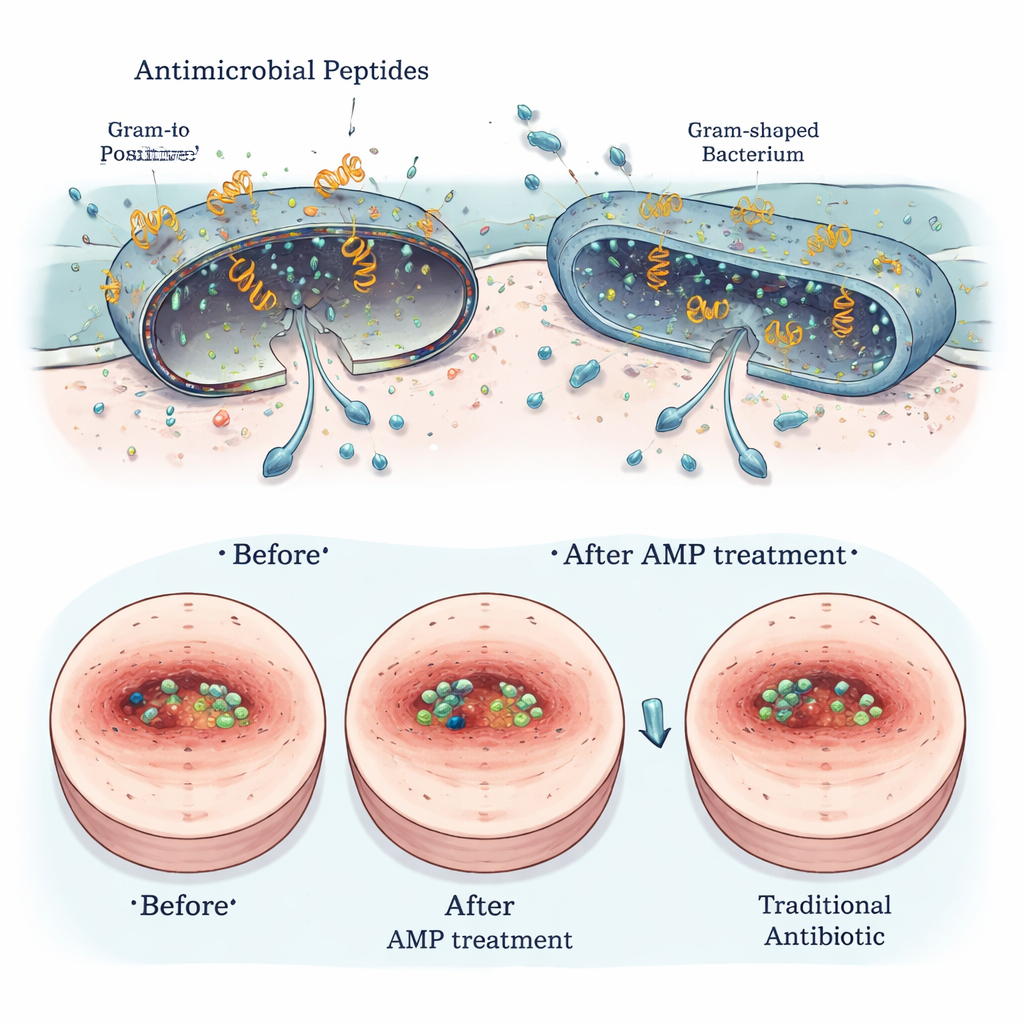
Bezpieczne dla gospodarzy, trudne dla zarazków — i obiecujące w leczeniu ran
Kilka z najbardziej obiecujących peptydów Segatella przetestowano pod kątem bezpieczeństwa i przydatności w praktyce. W hodowlach laboratoryjnych powodowały one niewielkie lub żadne uszkodzenia czerwonych krwinek i jedynie łagodne efekty, jeśli w ogóle, na komórki przypominające komórki jelitowe człowieka. Mikroskopia wysokiej rozdzielczości wykazała, że peptydy fizycznie uszkadzają zewnętrzne błony szkodliwych bakterii, jednocześnie oszczędzając komórki ssaków. W modelach zainfekowanych ran u gryzoni wybrane peptydy stosowane na skórę zmniejszały obciążenie bakteryjne, przyspieszały zamykanie ran i łagodziły objawy zapalenia, osiągając wyniki porównywalne z uznanyymi antybiotykami, takimi jak wankomycyna i polimyksyna B, szczególnie wobec bakterii Gram-dodatnich, jak Staphylococcus aureus.
Co to oznacza dla przyszłych leków
Dla osoby niezajmującej się specjalistycznie tematem przekaz jest prosty: mikroby jelitowe naszych przodków mogą skrywać plany nowych antybiotyków, które nadal działają przeciwko dzisiejszym, trudnym do leczenia zakażeniom. To badanie pokazuje, że dzięki inteligentnym, wydajnym narzędziom AI, takim jak AMPLiT, naukowcy mogą wydobywać z pradawnego DNA peptydy przeciwdrobnoustrojowe, które są zarówno silne, jak i stosunkowo łagodne dla komórek ludzkich. Choć przed przekształceniem tych molekuł w leki czeka wiele etapów, praca sugeruje, że przywrócenie „zagubionych” mikrobów sprzymierzonych, takich jak Segatella copri — lub przynajmniej zapożyczenie ich molekularnej broni — może pomóc uzupełnić kurczący się arsenał przeciwko opornym bakteriom.
Cytowanie: Chen, S., Yuan, Y., Wang, Y. et al. Identification of antimicrobial peptides from ancient gut microbiomes. Nat Commun 17, 1788 (2026). https://doi.org/10.1038/s41467-026-68495-0
Słowa kluczowe: peptydy przeciwdrobnoustrojowe, pradawny mikrobiom, Segatella copri, oporność na antybiotyki, poszukiwanie w metagenomach