Clear Sky Science · pl
Celowanie w kaskadę UFL1–AKT hamuje postęp potrójnie ujemnego raka piersi
Dlaczego to badanie ma znaczenie
Potrójnie ujemny rak piersi (TNBC) jest jedną z najgroźniejszych postaci raka piersi, ponieważ nie ma receptorów hormonalnych ani receptorów wzrostu, które są celem wielu nowoczesnych leków. Pacjenci często otrzymują jedynie chemioterapię konwencjonalną, która może przestać działać w miarę pojawiania się oporności guzów. To badanie odsłania wcześniej ukryty molekularny „silnik”, który pomaga komórkom TNBC rosnąć i opierać się chemoterapii, oraz proponuje nowy typ leku, który bezpośrednio zakłóca działanie tego mechanizmu.
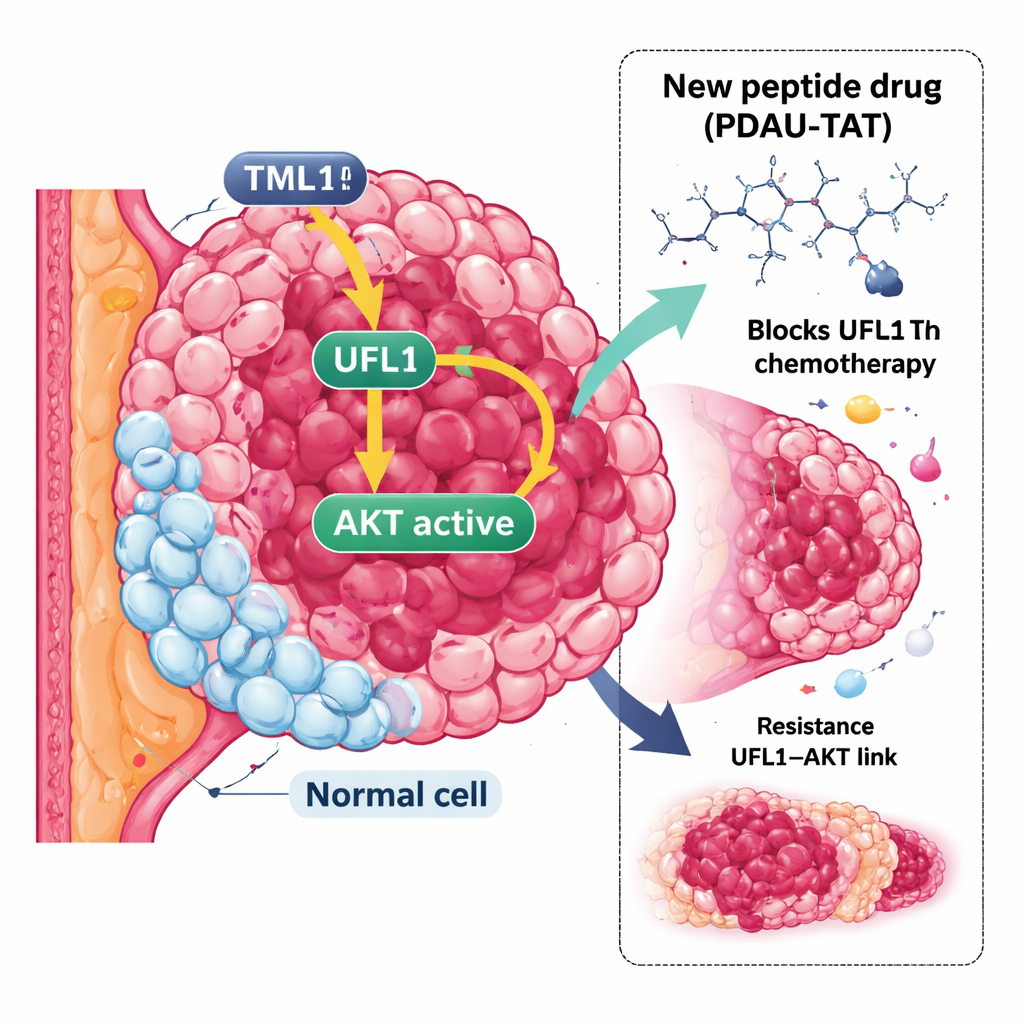
Uparta postać raka piersi
TNBC definiuje brak trzech typowych markerów: receptora estrogenowego, receptora progesteronowego oraz receptora HER2. Bez tych markerów wiele skutecznych terapii celowanych po prostu nie ma zastosowania. Zamiast nich stosuje się standardowe leki, takie jak cisplatyna czy doksorubicyna, lecz guzy TNBC często wykazują oporność lub szybko adaptują się do tych terapii i częściej dają przerzuty. To stwarza pilną potrzebę nowych strategii, które wyjdą poza utarte tropy i poszukają innych słabości w systemach kontrolnych guza.
Niewielkie, mało znane białko o dużym znaczeniu
Naukowcy skupili się na UFL1, białku przyłączającym niewielki znacznik zwany UFM1 do innych białek w procesie zwanym UFMylacją. Ten system znakowania został odkryty stosunkowo niedawno, a jego rola w nowotworach była dotąd niejasna, a czasem sprzeczna. Analiza danych pacjentów i próbek guza wykazała, że UFL1 jest wyraźnie podwyższone w TNBC w porównaniu z prawidłową tkanką piersi. Redukcja poziomów UFL1 w liniach komórkowych TNBC i w modelach guza u myszy spowalniała rozmnażanie komórek nowotworowych i znacznie zwiększała ich wrażliwość na chemioterapię, co sugeruje, że UFL1 pełni w tym kontekście rolę wspierającą nowotwór.
Powiązanie UFL1 z nadrzędnym przełącznikiem wzrostu
Dogłębną analizą badacze odkryli, że UFL1 bezpośrednio wiąże się z AKT, centralnym białkiem sygnalizacyjnym, które napędza wzrost komórkowy, przeżycie i metabolizm i jest często nadaktywne w nowotworach. W TNBC AKT bywa nadmiernie aktywny nawet przy braku typowych mutacji w górze kaskady. Zespół wykazał, że UFL1 chemicznie znakuję AKT w trzech określonych miejscach, co ułatwia jego aktywację przez partnerów aktywujących i chroni przed enzymami, które normalnie go wyłączają. Komórki pozbawione UFL1 lub wyrażające zmodyfikowaną wersję AKT, która nie może otrzymać tych znaczników, wykazywały dużo niższą aktywność AKT, wolniejszy wzrost i większą podatność na chemioterapię zarówno w hodowlach komórkowych, jak i w modelach zwierzęcych.
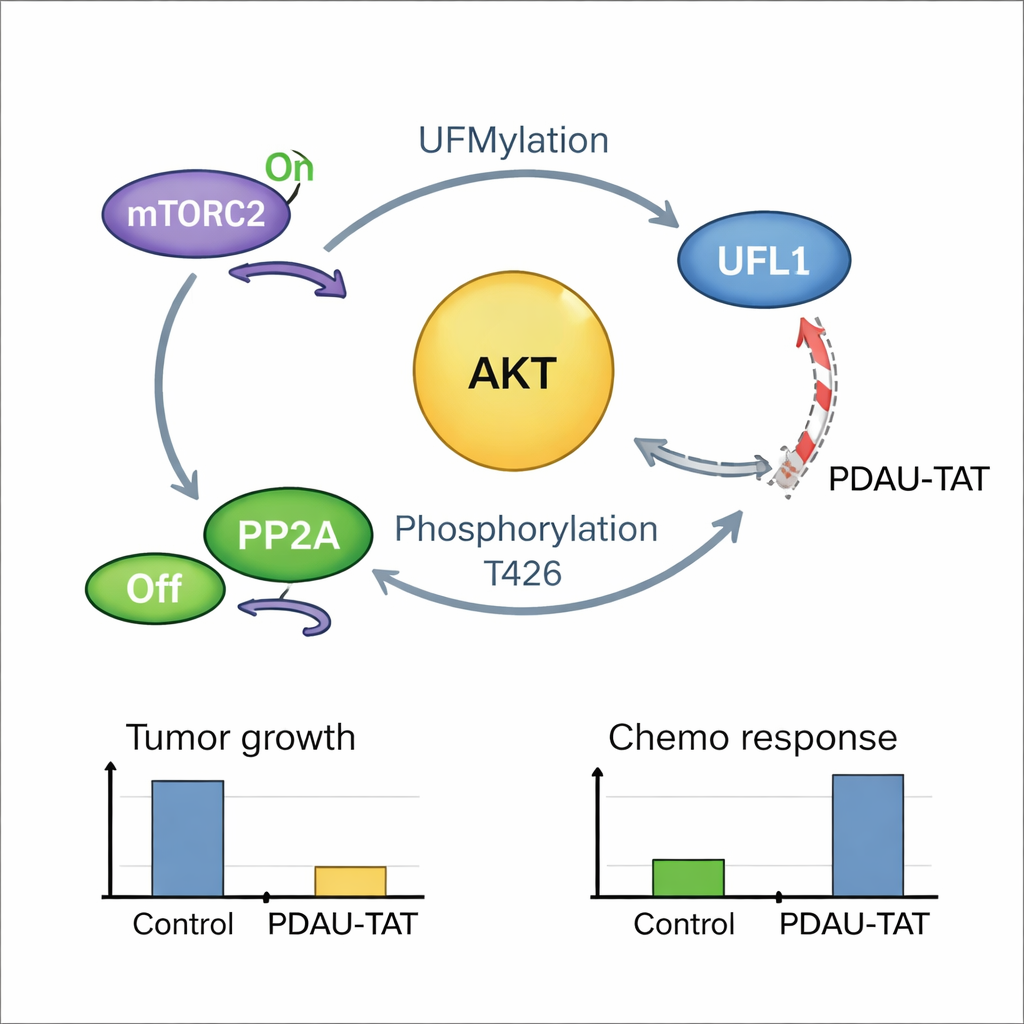
Samo-wzmacniająca się pętla nowotworowa i sposób jej przerwania
Okazało się, że powiązanie jest jeszcze silniejsze: gdy AKT zostaje aktywowany, oddziałuje zwrotnie i modyfikuje UFL1 w jednym kluczowym miejscu, zwiększając aktywność UFL1 wobec AKT i innych celów. Powstaje dodatnie sprzężenie zwrotne, w którym UFL1 aktywuje AKT, a aktywny AKT wzmacnia działanie UFL1. Próbki guzów pacjentek wykazały, że wysokie poziomy zmodyfikowanego UFL1 silnie korelują z wysokimi poziomami aktywnego AKT, co potwierdza istnienie tej pętli w chorobie ludzkiej. Aby wykorzystać tę słabość, zespół zaprojektował krótki peptyd penetrujący komórki, nazwany PDAU-TAT, który naśladuje mały fragment UFL1 i wsuwa się między UFL1 a AKT. Peptyd ten przerywa ich interakcję, zmniejsza aktywację AKT, spowalnia wzrost guza i zwiększa wrażliwość komórek TNBC oraz guzów pochodzących od pacjentów na chemioterapię, i to bez widocznych uszkodzeń głównych narządów u myszy.
Co to może znaczyć dla pacjentów
Mówiąc prosto, badacze odkryli ukrytą mapę połączeń wewnątrz komórek TNBC: UFL1 i AKT utworzyły samo-pogłębiającą się pętlę, która utrzymuje sygnały wzrostu w pozycji „włączonej” i pomaga guzom opierać się leczeniu. Stworzenie małego peptydu, który wślizguje się w tę pętlę i rozłącza UFL1 z AKT, pokazuje prawdopodobną nową metodę osłabienia guzów TNBC przy jednoczesnym oszczędzaniu komórek normalnych, które mają zazwyczaj niższe poziomy UFL1. Choć prace są jeszcze na etapie przedklinicznych, wskazują na nową klasę terapii celowanych, skierowanych nie na typowe receptory, lecz na połączenia białko–białko, które napędzają niektóre z najbardziej agresywnych raków piersi.
Cytowanie: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Słowa kluczowe: potrójnie ujemny rak piersi, szlak sygnalizacyjny AKT, UFMylacja, UFL1, peptydowa terapia przeciwnowotworowa