Clear Sky Science · pl
Pozytywne sprzężenie zwrotne UFL1–AKT przyspiesza rozwój raka piersi poprzez zwiększenie syntezy lipidów
Dlaczego komórki nowotworowe tak bardzo dbają o tłuszcze
Komórki raka piersi, jak wszystkie szybko dzielące się komórki, potrzebują stałego dopływu materiału budulcowego do tworzenia nowych błon i cząsteczek sygnałowych. Tłuszcze, czyli lipidy, są kluczową częścią tego zapasu. Badanie odkrywa, jak mało poznany system białkowy przestawia komórki nowotworowe w tryb „produkcyjnego przyspieszenia lipidów”, wspierając wzrost nowotworów i uchylanie się przed leczeniem. Zrozumienie tego ukrytego źródła paliwa może otworzyć nowe drogi do spowolnienia lub „zagłodzenia” raka piersi.
Ukryta modyfikacja białka o dużych konsekwencjach
Nasze komórki nieustannie regulują działanie swoich białek za pomocą drobnych chemicznych znaczników. Jeden z takich znaczników, zwany UFM1, jest przyłączany przez enzym o nazwie UFL1. UFM1‑owanie (UFMylacja) wiązano z naprawą DNA i reakcją na stres, ale jego rola w nowotworach była niejasna. Autorzy pokazują, że UFL1 jest znacznie bardziej aktywny w ludzkich guzach piersi niż w prawidłowej tkance piersiowej, we wszystkich głównych podtypach. Pacjenci, których guzy wykazują wyższy poziom UFL1, mają zwykle gorsze przeżycie. Gdy badacze zmniejszali poziom UFL1 w komórkach raka piersi lub w guzach mysich, wzrost nowotworu spowalniał, dzielenie się komórek malało, a śmierć komórek rosła, co sugeruje, że UFL1 działa jak czynnik sprzyjający rakowi.
Jak centrum sygnałowe zostaje przestawione na tryb produkcji tłuszczu
Aby zrozumieć, jak UFL1 wspiera guzy, zespół poszukiwał jego partnerów molekularnych i znalazł kluczowe białko kontrolujące sygnalizację — AKT1. AKT1 jest centralnym przełącznikiem, który sygnalizuje komórkom wzrost i syntezę lipidów. Badanie wykazuje, że UFL1 fizycznie wiąże się z AKT1 i ozdabia go znacznikami UFM1 w kilku określonych miejscach. Ta modyfikacja zmienia konformację AKT1, rozluźniając wewnętrzny „hamulec”, który zwykle utrzymuje go w spoczynku. Ponadto ułatwia przemieszczanie AKT1 do błony wewnątrzkomórkowej — retikulum endoplazmatycznego — gdzie inne enzymy mogą go w pełni aktywować przez fosforylację. Bez oznaczeń UFM1 w tych miejscach aktywacja AKT1 jest znacznie utrudniona.
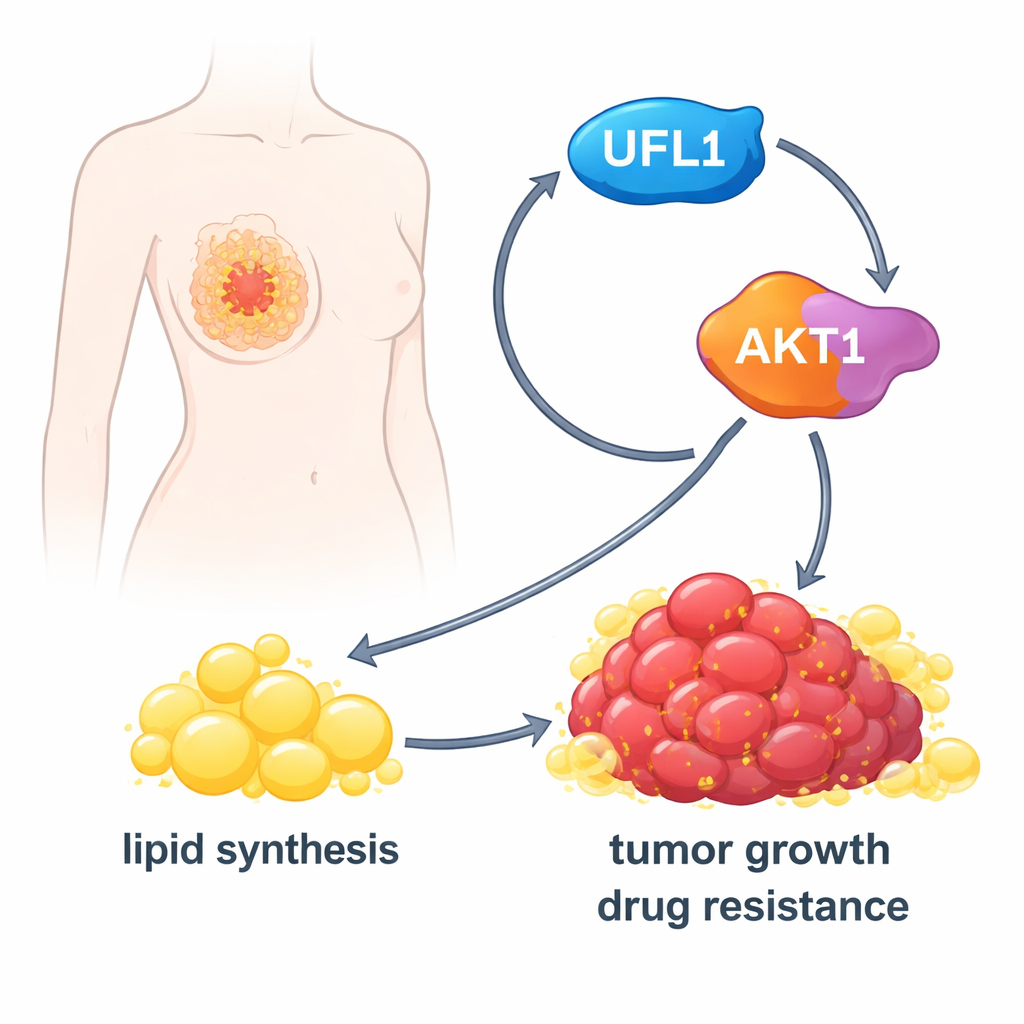
Włączenie fabryki tłuszczu w komórce nowotworowej
Po aktywacji AKT1 naciska komórki do zwiększenia produkcji tłuszczów. Zwiększa aktywność kluczowego enzymu metabolicznego ACLY i podnosi poziomy głównych regulatorów, takich jak SREBP1, które uruchamiają wiele genów związanych z syntezą lipidów. W hodowlach komórek raka piersi UFL1 powodował nagromadzenie kropli tłuszczu, wolnych kwasów tłuszczowych i cholesterolu. Usunięcie UFL1 wyraźnie zmniejszało te zapasy lipidów, zarówno w hodowlach komórkowych, jak i w guzach rozwijanych u myszy. Dostarczenie dodatkowych kwasów tłuszczowych z zewnątrz mogło w dużej mierze przywrócić wzrost komórek nowotworowych pozbawionych UFL1, co wskazuje, że głównym efektem UFL1 jest zabezpieczenie wystarczającej ilości lipidów do podtrzymania ekspansji guza.
Samo-wzmacniające się sprzężenie, które napędza wzrost guza
Niespodziewanie związek między UFL1 a AKT1 działa w obie strony. Naukowcy odkryli, że aktywny AKT1 z kolei fosforyluje UFL1 w określonym miejscu. Ta modyfikacja dodatkowo zwiększa zdolność UFL1 do znakowania AKT1 UFM1, tworząc dodatnie sprzężenie zwrotne: UFL1 aktywuje AKT1, a AKT1 aktywuje UFL1. Mutacje albo w miejscach UFM1 na AKT1, albo w miejscu fosforylacji na UFL1 przerywają to sprzężenie. U myszy guzy z tymi mutantami słabo rosły, zawierały mniej lipidów i wykazywały więcej obumierających komórek. W próbkach od pacjentów z rakiem potrójnie ujemnym wyższe poziomy aktywnego UFL1 i aktywnego AKT1 często współwystępowały, co podkreśla, że to sprzężenie działa także w rzeczywistych guzach.
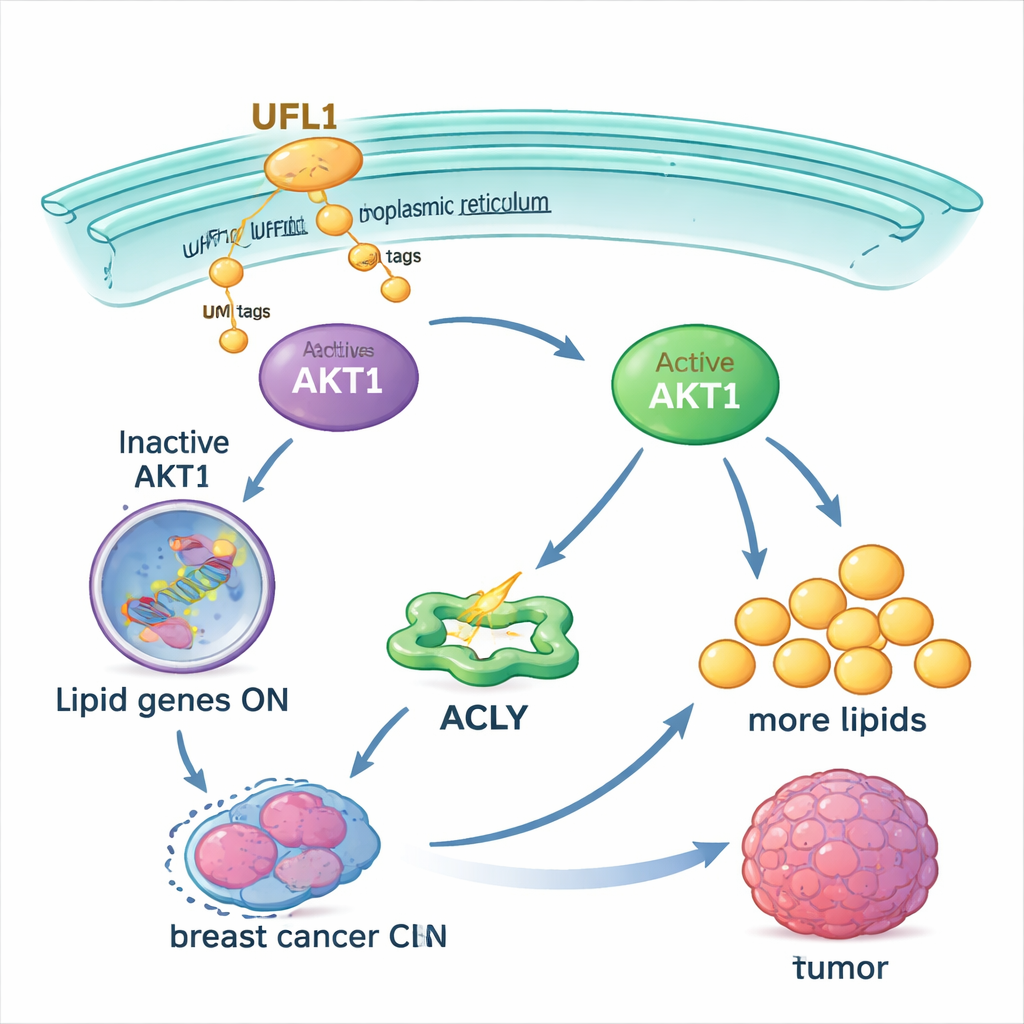
Osłabianie pętli, by zwiększyć skuteczność terapii
Ponieważ wiele prób lekowych już celuje w AKT, autorzy sprawdzili, czy blokowanie UFMylacji może uczynić te terapie skuteczniejszymi. W komórkach raka piersi małocząsteczkowy inhibitor UFMylacji i inhibitor AKT każdy z osobna obniżały aktywność AKT1 i gromadzenie lipidów, ale zastosowanie obu jednocześnie działało znacznie lepiej niż każdy z nich osobno. Połączenie to także spowalniało wzrost guzów i zmniejszało zawartość tłuszczu w guzach mysich bez zauważalnej utraty masy ciała u zwierząt. Blokada UFMylacji dodatkowo zwiększała wrażliwość komórek nowotworowych na standardowe chemioterapeutyki, takie jak cisplatyna i etopozyd, które często zawodzą, gdy AKT jest silnie aktywny.
Co to oznacza dla pacjentów
Dla czytelnika niebędącego specjalistą badanie pokazuje, że niektóre raki piersi uzbrajają się w samo-wzmacniające pętle, które zasilają zarówno ich wzrost, jak i zaopatrzenie w lipidy. UFL1 i AKT1 działają razem jak dwa jednocześnie wciśnięte pedały: jeden oznacza, drugi sygnalizuje, a wspólnie napędzają produkcję lipidów i ekspansję guza. Znalezienie leków, które zakłócą to sprzężenie — przez blokowanie UFMylacji, AKT1 lub ich interakcji — może w przyszłości pozwolić na spowolnienie wzrostu guza i zwiększenie skuteczności istniejących terapii, szczególnie w agresywnych typach raka piersi.
Cytowanie: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Słowa kluczowe: rak piersi, metabolizm lipidów, szlak AKT, UFMylacja, terapia celowana